Bonsoir,
J’aurais besoin d’aide avec la lettre b de numéro. (La réponse est en rouge.)

Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
Voici ma démarche pour la lettre a :
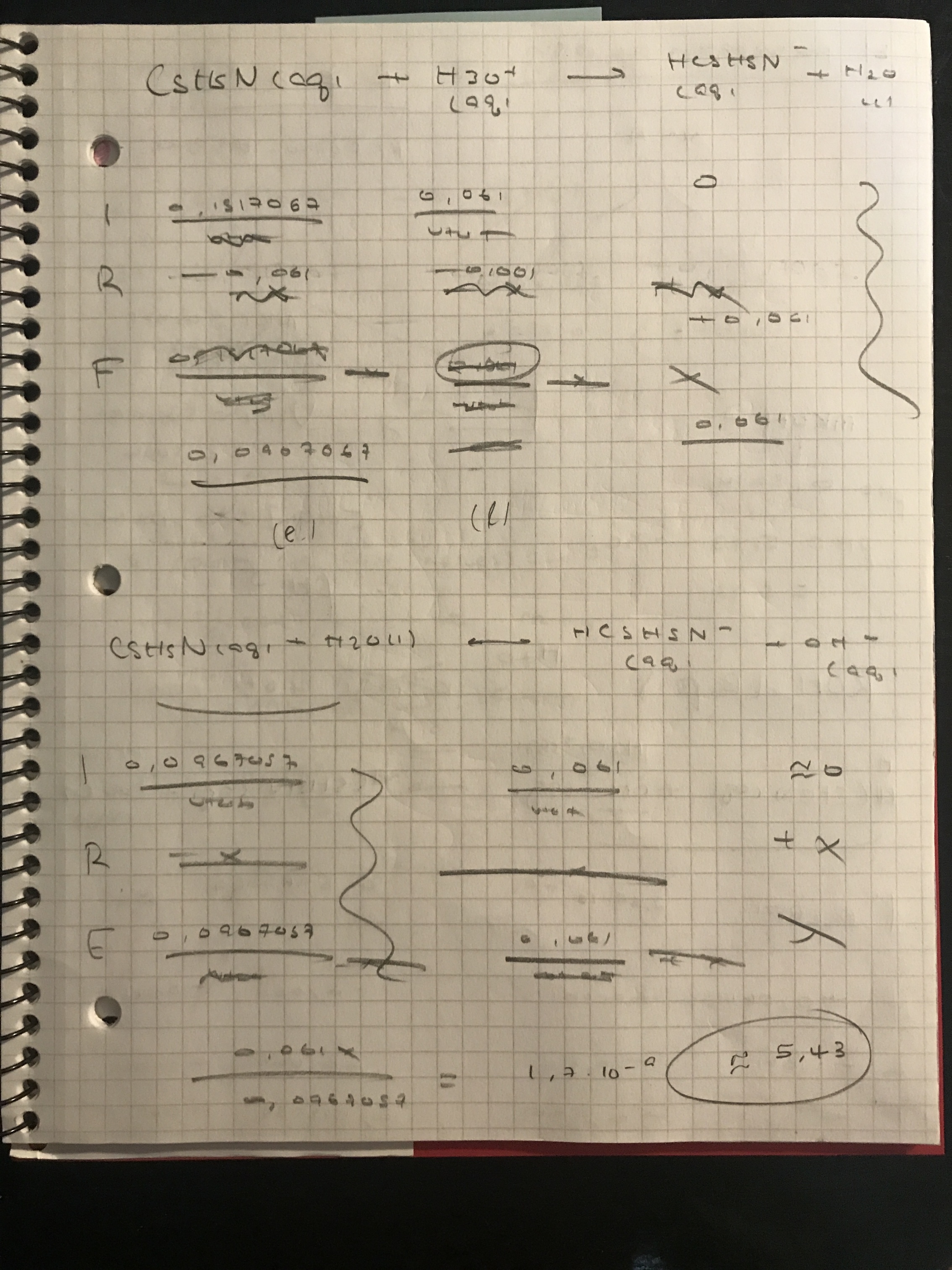
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
Voici ce que j’ai tenté pour la lettre b :

Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
Merci et bonne soirée! ;)
OrAutonome2754









Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut !
Pour le a), tu peux penser que la réaction est complète. Ainsi, la première étape est de calculer le nombre de mole de produits. Il ne faut pas oublier qu'un acide fort implique une dissociation complète : \(n_{HCl}=n_{H^+}\).
À partir de là, tu trouver le nombre de mole de \(H^+\) restant et sa concentration pour ensuite calculer le pH.
Pour b), on te donne le pH final (\(5,40+0,50=5,90\)). Tu peux donc calculer la concentration en \(H^+\) finale et trouver la variation en nombre de mole qui représente le nombre de mole de \(OH^-\) qui a réagit avec les protons.
La seconde portion du b) te demande des démarches similaires pour arriver à la réponse.
Bonne continuation !
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!