Secondaire 5 • 1a
Bonjour,
J'ai besoin d'aide en chimie
Le problème à résoudre : Calculez la quantité d’air nécessaire pour la durée totale de plongée du plongeur choisi. Comparez votre réponse avec la quantité d’air que votre plongeur consommerait à la surface pour cette même période de temps.
Les donnés :
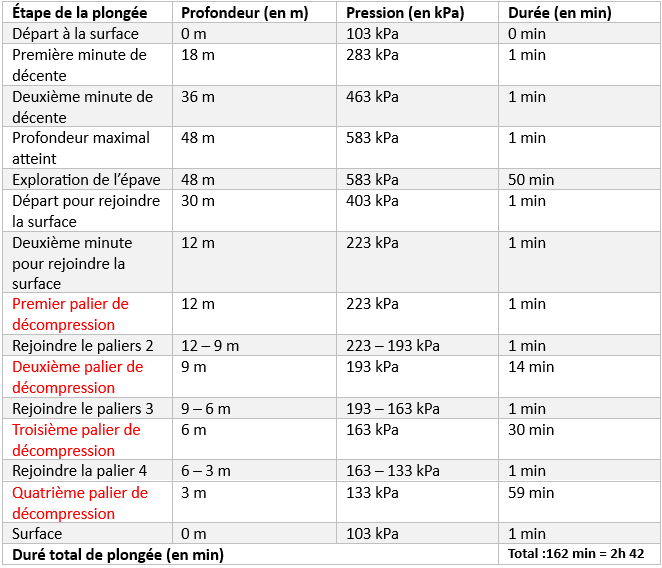
Mon tableau :
Ma question :
Je dois faire quoi pour trouver la quantité de mol durant la plongée et la quantité de mol durant un moment fictif si il était en surface pour ensuite faire une comparaison entre les deux résultat.
Ma théorie :
Je pense que le plongeur demandera plus d'air sous l'eau que en surface.
Svp aidé moi, à l'aide...
PS : Dire la raison du refus de ma question serai apprécier.
Merci









Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut !
Le problème semble complexe. Tout tourne autour de l'utilisation de la loi des gaz parfaits.
La première étape semble être le calcul de la quantité d'air dont le plongeur aura de besoin à la surface. Pour ce faire, tu peux utiliser la pression atmosphérique et la température de l'eau comme étant celle de l'atmosphère autour du plongeur. Pour le volume, on te donne le temps et le débit d'air.
Pour la prochaine quantité d'air, tu dois y aller étape par étape. Il commence sa plongée en descendant de 18 mètres. Cela lui prend une minute à une pression de 283 kPa. Avec ce temps, tu peux trouver le volume. Et avec la pression et la température, tu peux calculer la consommation d'air en mole qu'à pris cette minute de descente.
Tu fais pareillement avec les autres étapes de descente et monté pour calculer la consommation totale d'air.
Je te laisse essayer par toi-même et si tu as d'autres questions, n'hésite pas !
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!