Secondaire 5 • 1a
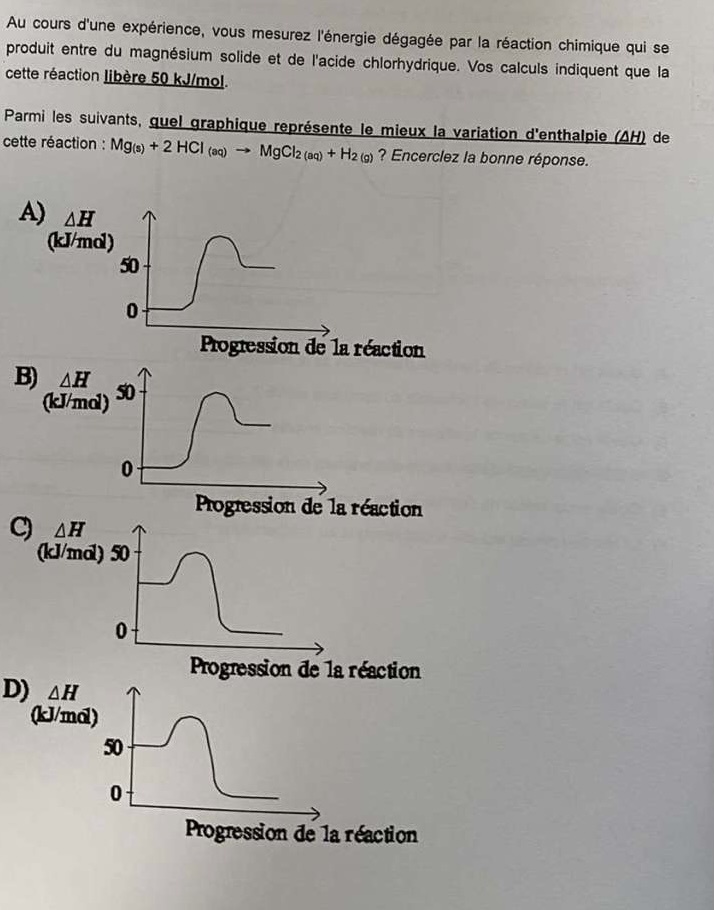
J’ai besoin d’un petit coup de main car j’hésite entre la réponse C) et D). Puisque ça dit que ça libère 50kj/mol, et non que l’enthalpie des produits tout court est de 50kj/mol, je crois que c’est C).






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Merci pour ta question!
Tu es sur la bonne piste, mais la bonne réponse est D). En effet, lorsqu'on dit que la réaction libère 50 kJ/mol, on fait référence au fait que sa variation d'enthalpie (∆H) est de 50 kJ/mol.
La variation d'enthalpie mesure la différence entre l'enthalpie des produits et des réactifs, et non la différence d'enthalpie entre les réactifs et le complexe activé (sommet de la courbe).
Bref, pour que la variation d'enthalpie égale 50 kJ, il faut que les réactifs soient à 50 kJ et les produits à 0 kJ.
N'hésite pas si tu as d'autres questions!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!