Secondaire 5 • 2a
Bonjour,
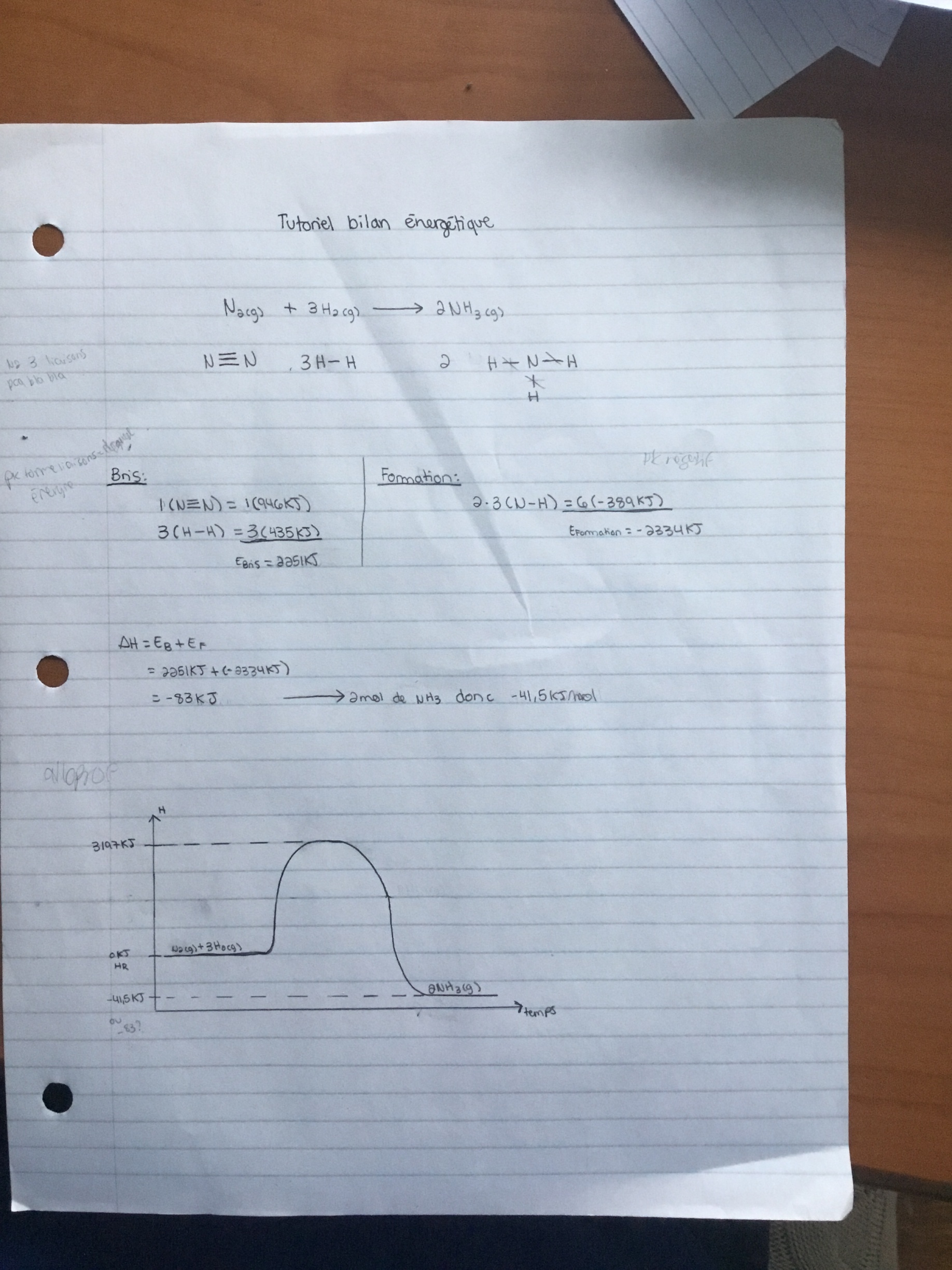
J'ai quelques questions sur ce que j’ai fait.
- Est-ce que ce que j’ai fait est bon?
- J’ai oublié pourquoi l’énergie de formation est négative.
- Pour le deltaH, puisque j’ai 2 moles de NH3, j’ai oublié si je dois faire x2 ou diviser par 2
- Pourquoi quand on forme des liaisons, de l’énergie se dégage?
Merci beaucoup!






Explication vérifiée par Alloprof
Cette explication a été vérifiée par un membre de l’équipe d’Alloprof.
Si les énergies libéré et nécessaire au bris et aux liaison dont bonne, alors ta démarche est bonne.
Une énergie négatif veut dire qu'il y a eu dégagement d'énergie. Si la valeur est négative, cela veut dire dégagement d'énergie.
Delta H correspond à la réaction complète, donc ce n'est pas nécessaire de divisé ou multiplier par 2. Tu peux le garder tel quel.
Tu ne dois pas voir cela comme formation de liaison = dégagement d'énergie.
Le dégagement d'énergie survient lorsque les atomes/molécule deviennent plus stable. Lors d'une réaction chimique, s'il y a un dégagement d'énergie, cela veut dire que le tout devient plus stable.
Dans ce cas 2*NH3 est plus stable que N2 + 3 H2
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!