Bonjour,
dans le problème #2, pourquoi il faut utiliser PV= nRT pour trouver le nombre de mol de He? moi, dans ma démarche j'ai utiliser le produit croisé car c'est à température de la pièce, à 25 degré non? pourquoi ma méthode est mauvaise?
merci!

Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.

Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
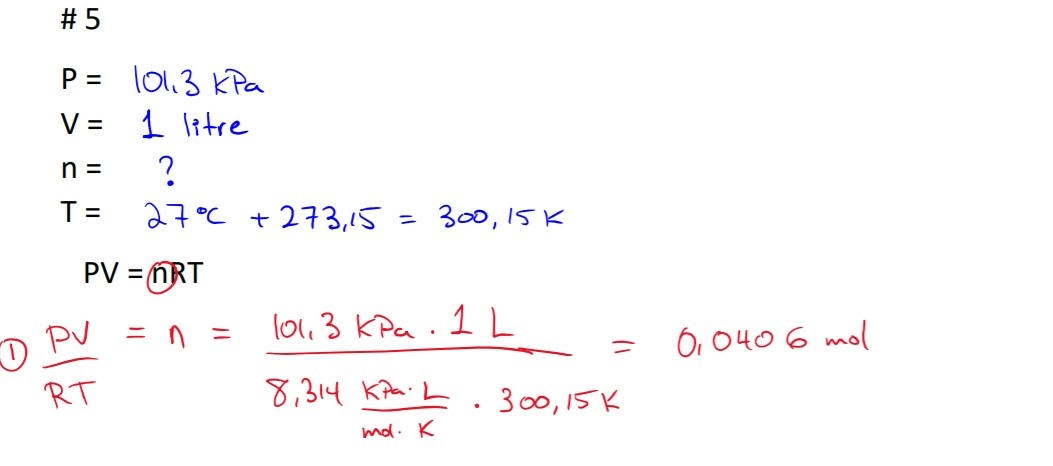
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
voici ci joint une partie du corrigé.


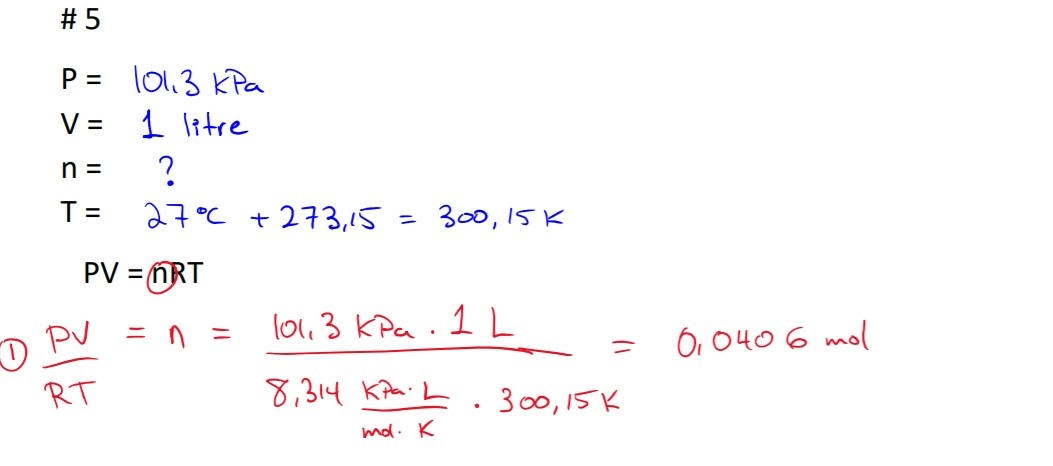






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour Shy Owl!
Merci de faire appel à nos services 😉
Premièrement l'image du corrigé insérée dans ta question ne semble pas correspondre au problème 2. Il est donc possible que ceci ait été mélangeant!
Ensuite, dans cette situation, tu n'avais pas toute les informations nécessaires pour effectuer un produit croisé, tandis qu'avec la loi des gaz parfait, il était possible de déterminer le nombre de moles d'hélium. En effet, le volume, la température et la pression sont donnés, ce qui te permet d'utiliser cette formule.
Pour réviser la loi des gaz parfaits, tu peux consulter le lien suivant:
J'espère que cela t'aidera!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!