Bonjour,
Je suis en secondaire 5 et j'ai de la difficulté avec une pratique de laboratoire en chimie. Voici mon problème:
Déterminer la masse molaire d’un gaz inconnu afin de l'identifier parmi les 3 gaz suivants: N2, CO2 et H2.
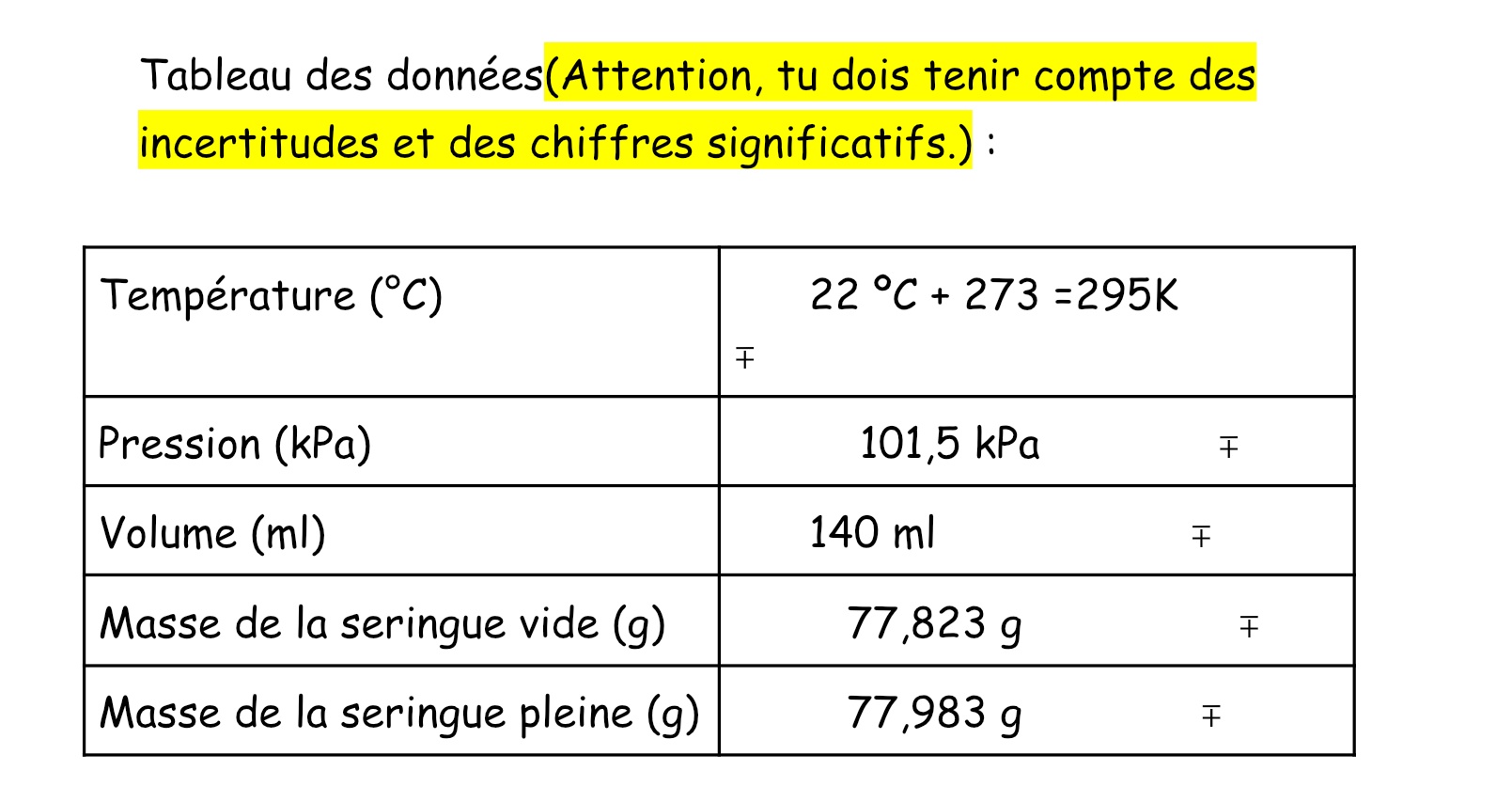
Matériel: une balance, un baromètre électronique, une seringue, le bouchon de la seringue et un ballon remplie du gaz inconnu.
Protocole: 1)remplir la seringue à sa capacité maximal (140ml) avec l'air ambiant. 2)peser à l'aide de la balance, la masse de la seringue vide. 3)noter le résultat. 4) remplir la seringue du gaz inconnu en insérant le tuyau relié au ballon dans le bouchon de la seringue. 5) retirer rapidement le tuyau. 6) insérer le bouchon à l'ouverture de la seringue. 7) peser la masse de la seringue contenant le gaz inconnu. 8)noter le résultat
Tableau des données: (image)
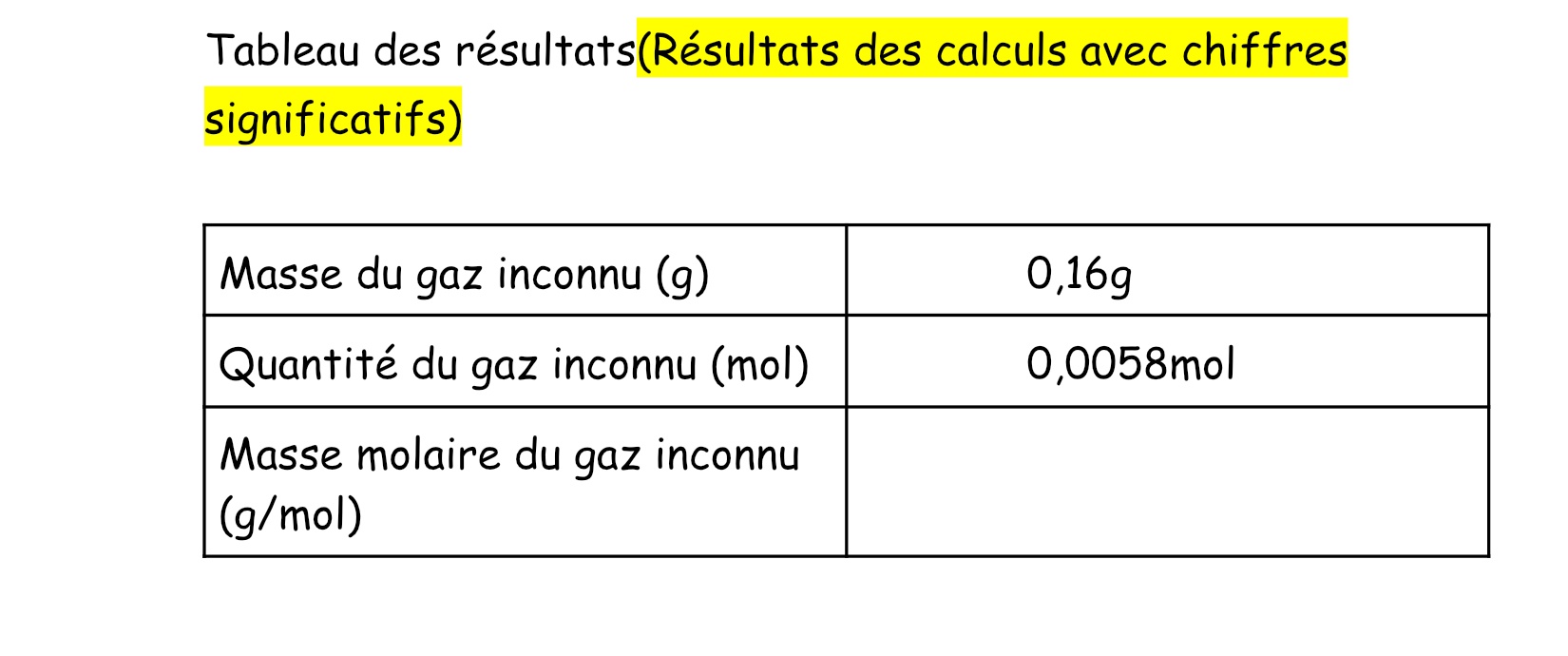
Tableau des résultats: (image)
Conversion des unités:
- masse de la seringue pleine - masse seringue vide = masse gaz inconnu
77,983g - 7,823g = 0,16g
- calcul du nombre de mol à l'aide de la formule (PV=nRT)
N=PV/RT = 101,5 kPa x 0,14L / 8,314 x 295K
N= 0,0058 mol
- calcul de la masse molaire du inconnu
M= m/n
M= 0,16g x 0,0058 mol
M= 0,000928 g/mol
Masse de N2= 28,01 g
Masse de CO2= 44,0095 g
Masse de H2= 2.02 g
Je devrais donc avoir une des trois masse qui correspond à 0,000928 g, mais il n'y en a pas. Je ne comprend pas mon erreur. Est-ce que vous pourriez m'aider?
Merci






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut !
Ton erreur est plus simple que ce que tu penses. Voici la formule pour la masse molaire :
$$ M=\frac{m}{n} $$
Donc, tu devais diviser la masse par le nombre de mole au lieu de les multiplier. Je t'invite à essayer de nouveau et si tu as besoin de plus de détails sur ola masse molaire, je t'invite à visiter cette fiche alloprof :
Si tu as d'autres question, n'hésite pas !
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!