Bonjour, je rencontre quelque difficultés a faire mon rapport de lab (Voir les information du titrage ci-bas). On nous demande de calculer la molarité exacte de l'acide acétique avec la pH expérimentale de la solution. Nous n'avons pas la concentration d'acide ni son Ka (on doit le calculer a chaque étape). On sait qu'on peut calculer la concentration de H3O+ en faisant 10 exp -ph. on sait également qu'au point d'équivalence le n d'Acide = n de base. Mais on comprend pas c'est quoi le lien entre le ph et la molarité ni comment liés toutes ces informations.
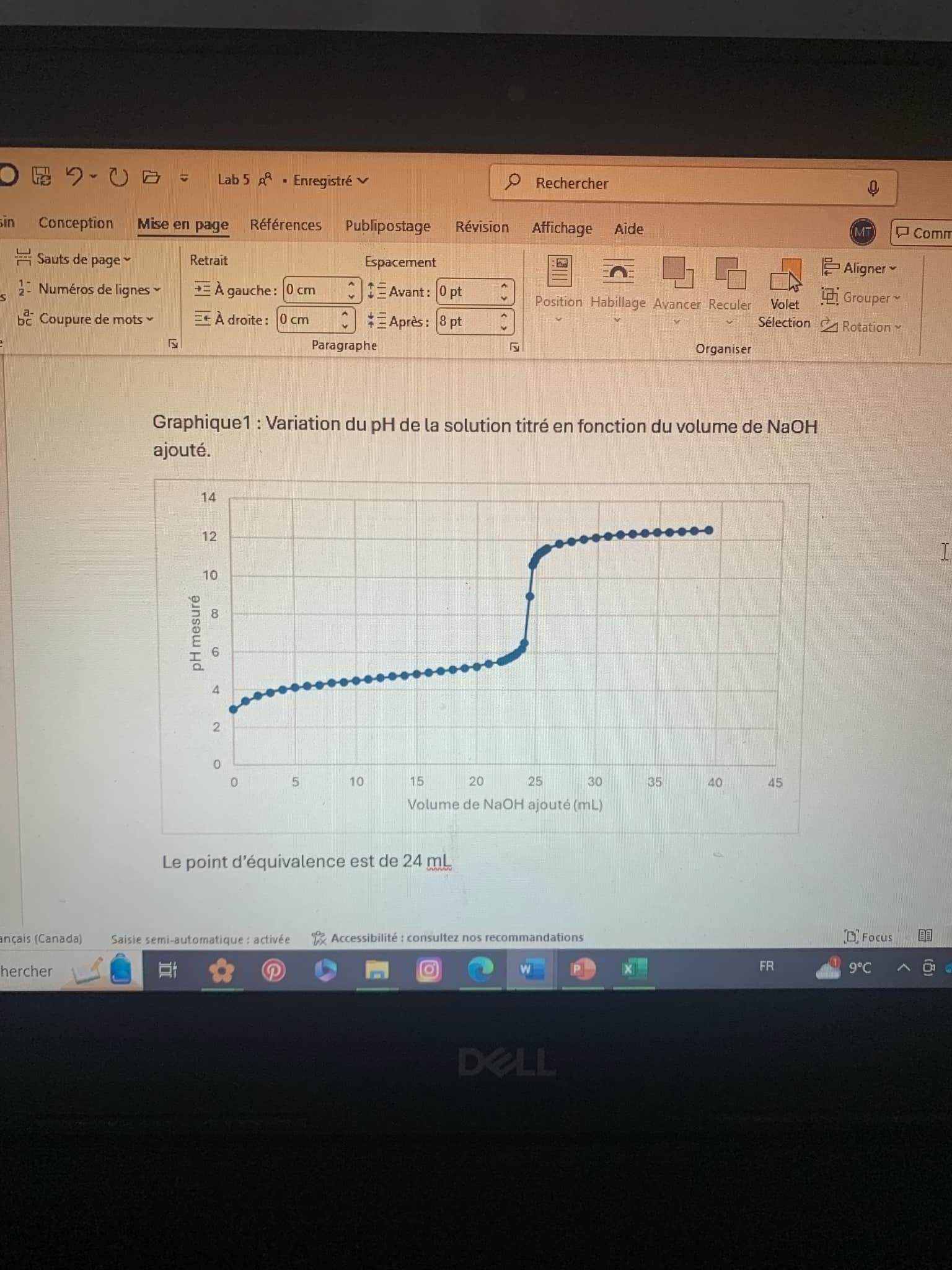
Alors, nous avons fait un titrage avec de l'acide acétique a concentration inconnu (dilué), avec du NaOH 0,1M. Le pH initiale de l'acide était de 2,93, au demi équivalence 4,64 (12ml de NaOH) au point d'équivalence 6,52 (24ml de NaOH). Nous avons ensuite dilué 10 ml d'acide acétique avec 90 ml d'eau.







Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!