Bonsoir :)
J'ai des GRANDES confusions sur certains concepts qui se portent sur les lois simples des gaz, les-voici:
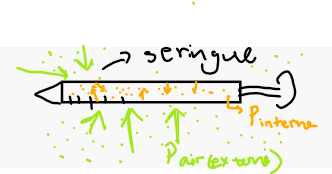
1) Comme vous pouvez le voir dans le problème ci-dessous qui se porte sur la relation entre le volume et la pression, on dit qu'une seringue contient 25 ml de gaz à la pression atmosphérique.
Cependant, je ne comprends vraiment pas comment est-ce que la pression des molécules de gaz enfermées à l'intérieur de la seringue peut être égal à la pression atmosphérique? La pression atmosphérique se passe à l'extérieur du récipient, alors comment ça se fait-il que mes molécules de gaz dans le seringue aient cette même pression de 101,3 kPa?
2) Je ne comprends AUCUNEMENT lorsque mon prof répète cet énoncé: '' Si la pression augmente dans un contenant non-rigide, son volume augmente jusqu'à ce que la pression à l'intérieur soit égale à la pression externe''. Il l'associait souvent avec un objet gonflable comme un pneu ou un ballon. Pouvez-vous m'expliquer d'une manière détaillée pourquoi et comment est-ce que cet équilibre de fonctionne dans le cas d'un pneu et d'un ballon ?
Je sais qu'avec vos explications, le tout va s'éclaircir.
Merci beaucoup :D







Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Merci pour ta question!
Dans la première situation, je pense que la seringue a la même pression atmosphérique juste, car il s'agit de la situation initiale. Même si la pression atmosphérique extérieure n'interagit pas avec le gaz dans la seringue, rien n'empêche ce gaz d'avoir la même pression!
Pour ta seconde question, je pense que tu dois toujours t'imaginer la pression comme étant causée par des milliards de collisions par seconde entre les molécules de gaz et les parois du volume. En effet, rappelle-toi que, si les particules de gaz à l'intérieur du volume gonflable frappent plus fort que celle à l'extérieur, l'objet gonflable va nécessairement gonfler!
Cette fiche du site d'Alloprof explique la pression des gaz :
Alloprof aide aux devoirs | Alloprof
https://www.alloprof.qc.ca/fr/eleves/bv/chimie/la-pression-des-gaz-c1059N'hésite pas si tu as d'autres questions!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!
Fiche
La loi des gaz parfaits gaz parfaits parfaits loi des gaz volume pression constante gaz parfait zéro absolu 0 K molécule température nombre de molécules mole constante des gaz parfaits loi générale des gaz ...
| Secondaire 5
Fiche
La loi des pressions partielles (loi de Dalton) pression mélange pression partielle partielle pression totale totale partiel John Dalton Loi de Dalton volume nombre de mole La loi des pressions partielles (loi de D...
| Secondaire 5
Fiche
La pression des gaz la pression d'un gaz manomètre pression atmosphérique manomètre à bout fermé La pression des gaz | Secondaire | Alloprof La pression (kPa) peut se mesurer à l'aide d'un baromètre. L...
| Secondaire 5