Secondaire 5 • 1a
Bonsoir!
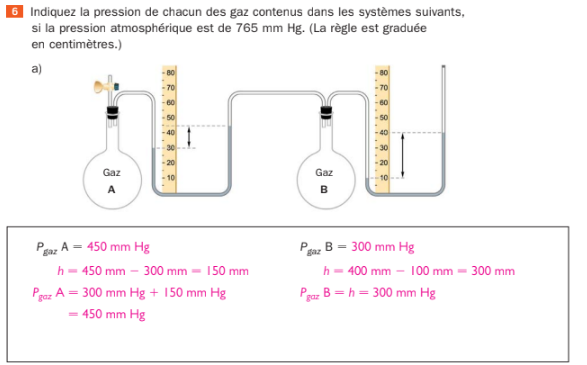
Ci-dessous, j'insère une photo du corrigé d'un problème sur la pression:
Je ne comprends pas la démarche!
Pourquoi est-ce que la formule de "P gaz A" = 300 mm Hg + 150 mm?? Pourquoi travaille-t-on avec le 300 mm Hg, alors que, dans un manomètre fermé, la pression du gaz devrait être égal à la hauteur du mercure?
Est-ce que cette règle change dans des cas où 2 gaz sont connectés comme dans l'image???
SVP, aidez-moi!! Je suis vraiment perdue






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour NickelAlpha325,
Merci pour ta question :)
Le manomètre B est un manomètre fermé, donc le calcul est simplement effectué par la différence entre les hauteurs de mercure. Cependant, le manomètre A ne peut être considéré comme fermé (dans un manomètre fermé, le tube de mercure contient aussi du gaz, donc aucune particule ne pousse «contre» le mercure du manomètre). Dans le cas de A, le gaz B pousse «contre» le mercure dans ce manomètre, tout comme le gaz A. Tu dois donc traiter la question comme si A était un manomètre ouvert...mais pas avec la pression atmosphérique, puisque ce ne sont pas les particules de gaz de l'air qui pousse, mais les particules de gaz B.
La formule sera donc P_A=P_B+h.
N'hésite pas si tu as d'autres questions :)
Sandrine
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!