Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment on fait les équations de formation
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ’aimerais comprendre la lois de Hess je ne la comprend pas vraiment.
-
Vérifiée par Alloprof
Secondaire 5 • 2arebonjour
voila ma démarche pour cet exercise
-
Vérifiée par Alloprof
Primaire 5 • 2aJe n’ai pas compris cette exercices:Merci d’avance!!!!!!!!!!!n :)
-
Vérifiée par Alloprof
Secondaire 5 • 2abonjour
je veux savoir si ma démarche est correcte et que ma réponse aussi pour cet exercise la
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
j'espère que vous allez bien. J'ai de la difficulté à comprendre comment calculer la variation de l'enthalpie par la stœchiométrie. Je ne comprends pas bien mes exercices et j'ai une évaluation vendredi matin portant sur cette matière. Pourriez vous m'aider avec cela ?
Merci en avance,
TortueDynamique1064
P.S.: nous travaillons avec le volume de chimie Quantum, de secondaire 5.
-
Vérifiée par Alloprof
Secondaire 5 • 2abonjour j’espère vous allez bien
jaurais bien besoin d’un coup de main sur cet exercise(6). si vous pouvez svp m’écrire la démarche
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour alloprof,
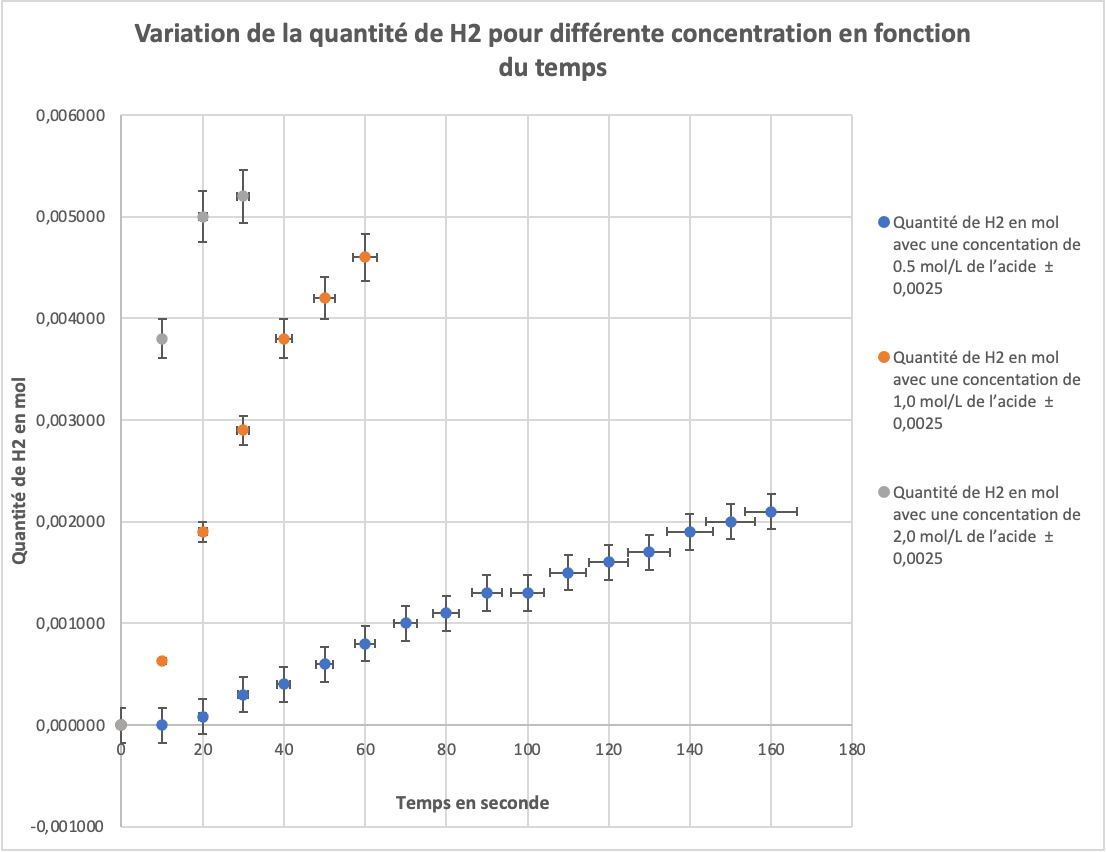
Quest ce qui explique la variation de la vitesse instantanée de formation du dihydrogène?
-
Vérifiée par Alloprof
Secondaire 5 • 2aEst-ce que c’est possible d’avoir un pourcentage d’écart négatif entre les valeurs théoriques et expérimentales?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, est-ce que c'est normal que ma pente change selon les points que j'utilise dans mon graphique?
-
Vérifiée par Alloprof
Secondaire 5 • 2aEst-ce qu'un atome seul est obligatoirement un ion ? Par exemple : H ou O ou C qui ne sont pas liés à d'autres atomes ? Parce que chaque atome individuel a une charge, sauf ceux dans la famille des gaz rares je crois. J'ai beaucoup de difficultés à comprendre tout le concept des charges, surtout en ce qui concerne les ions polyatomiques.
-
Vérifiée par Alloprof
Postsecondaire • 2aBonjour, je ne comprends pas comment faire:
Calculer la molalité d'une solution obtenue en mélangeant 500,0 mL d'une solution aqueuse de saccharose (C12H22O11) de pourcentage massique égale à 60% et de masse volumique 1,3 g/mL avec 500,0 mL d'eau de masse volumique égale à 1,0 g/mL.
Réponse donnée par le prof: 1.5 mol/kg
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je dois faire un rapport de laboratoire et je doit calculer la production de 10 L de dihydrogène avec de HCl à 0,5 mol/L , 1 mol/L et 2 mol/L mais je sais pas comment le faire et je sais pas si je dois utiliser les mol produits par seconde ou les ml par seconde
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir! je voulais savoir, pourquoi la dissolution de NaOH est-elle exothermique??
-
Vérifiée par Alloprof
Secondaire 5 • 2aC'est une question de chimie jle trouve tlmnt difficile jai besoin d'aide.
merci!
-
Vérifiée par Alloprof
Secondaire 4 • 2aSalut! J'ai besoin de l'aide avec celui-là aussi svp
-
Vérifiée par Alloprof
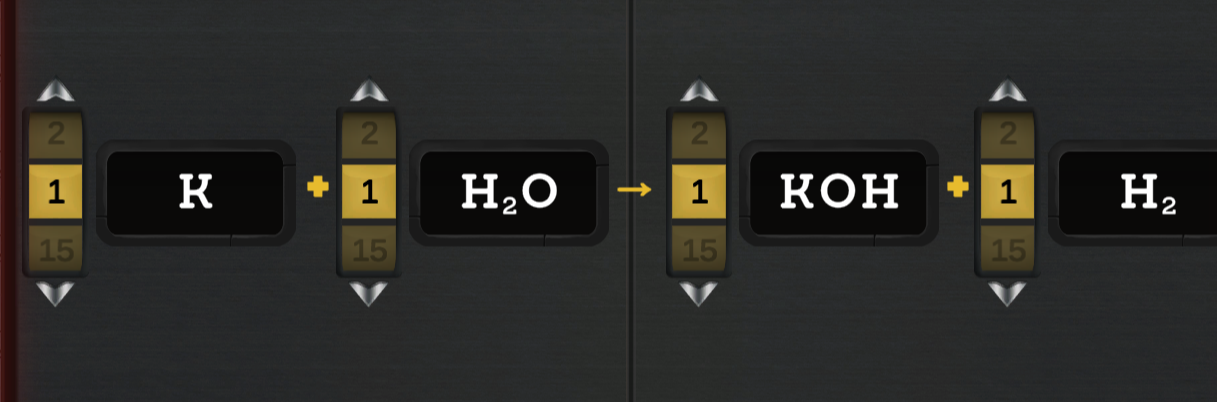
Secondaire 4 • 2aBonjour, comment balance-t-on l'équation
N2O5 -> NO2 + O2
Les chiffres ne sont pas des coefficients.
-
Vérifiée par Alloprof
Secondaire 4 • 2aComment est-ce qu'on trouve la charge d'un ion avec l'aide du tableau périodique? Merci
-
Vérifiée par Alloprof
Postsecondaire • 2aComment l'on fait pour déterminer un delta Tcongélation à partir de deux valeurs de Tcongélation.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je dois faire un rapport de laboratoire et je dois trouver comment faire du h2 le plus rapidement possible avec les 3 concentration différentes mais je ne sais pas comment le calculer parce que j'ai juste le volume par seconde et le nombre de mol produit par seconde? Je dois aussi trouver le pourcentage d'erreur mais il n'y a pas de données théoriques.
Pouvez-vous m'aider s'il vous plaît?
Merci d'avance :)
-
Vérifiée par Alloprof
Secondaire 5 • 2aQuelle est la différence entre un ions polyatomique et une molécule?
-
Vérifiée par Alloprof
Secondaire 5 • 2aHow did J.J. Thomson determine the mass of an electron?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je dois faire un rapport de laboratoire et je dois tracer une sécante pour la vitesse moyenne et une tangente pour un temps choisi sur mon graphique, mais je ne comprends pas comment le tracer dans le graphique. Pouvez-vous m'aider s'il vous plaît?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je me demandais pourquoi lorsqu'une réaction est soumise à une pression irrégulière la formule Q=mcdeltaT n'est pas valide?
merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
Pouez-vous M'aider à vérifier un peu si j'ai bien fait cette question ou non SVP?
Merci en avance
C3H8(g)+5O2(g)→3 CO2 (g)+4 H2O(g)
- 3C(s) + 4H2(g) → .C3H8(g) ΔH°f = -103,8 kJ/mol
C(s)+O2(g)→CO2 (g) ΔH°f =−393.5 kJ/mol
H2(g) + ½O2(g) → H2O(g) ΔH°f = -241,8 kJ/mol
- .C3H8(g) → 3C(s) + 4H2(g) ΔH°= 103,8 kJ/mol (1)
3* (C(s)+O2(g)→CO2 (g))
3C(s)+3O2(g)→3CO2 (g) 3 * ΔH°=−393.5 kJ/mol * 3 = -1186, 5 kJ/mol (2)
4 * (H2(g) + ½O2(g) → H2O(l) )
4 H2(g) + 2O2(g) →4 H2O(g) 4 * ΔH°= -241,8 kJ/mol * 4 = -967,2 kJ/mol(3)
- ΔH° = ΔH°1 + ΔH°2 + ΔH°3
= 103,8 kJ/mol + (-1186, 5 kJ/mol) + ( - 967,2 kJ/mol)
= -2049,9 kJ/mol
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir,
Pouvez-vous aider à vérifier si j'ai bein fait cette question SVP?
Merci en avance : )
CO(g)+ 3H2(g) → CH4(g) + H2O(l)
- C(s) + ½O2(g) → CO(g) ΔH°f = -110,5 kJ/mol
C(s) + 2H2(g) → CH4(g) ΔH°f = -74,6 kJ/mol
H2(g) + ½O2(g) → H2O(l) ΔH°f = -285,8 kJ/mol
- CO(g) → C(s) + ½O2(g) ΔH°= 110,5 kJ/mol (1)
C(s) + 2H2(g) → CH4(g) ΔH°= -74,6 kJ/mol (2)
H2(g) + ½O2(g) → H2O(l) ΔH°= -285,8 kJ/mol (3)
CO(g) + 3H2(g) →CH4(g) + H2O(l)
3) ΔH° = ΔH°1 + ΔH°2 + ΔH°3
= 110,5 kJ/mol + (-74,6 kJ/mol) + (-285,8 kJ/mol)
= -249,9 kJ/mol
-
Vérifiée par Alloprof
Secondaire 5 • 2aallo, je me demandais si plus la température d’ignition d’un substance quelconque est basse, plus la vitesse de la réaction est vite. Ou le contraire?
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment peut-on calculer la chaleur molaire de formation de l'acide sulfurique dans les nuages?
-
Vérifiée par Alloprof
Secondaire 5 • 2a2 contenants identiques, (un avec du dihydrogene et l'autre avec du dioxygène) contiennent chacun 5,0 mol de gaz aux mêmes conditions de température et de pression :
Les deux contenants contiennent le même nombre de particules de gaz.
Les deux contenants renferment la même masse de gaz
La vitesse moyenne de l’ensemble des particules de chacun des gaz est la même.
Sont-ils vrai ou faux ? Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, est-ce que Q=mcdeltaT s'applique pour les réactions avec les gaz? Si non pourquoi?
merci