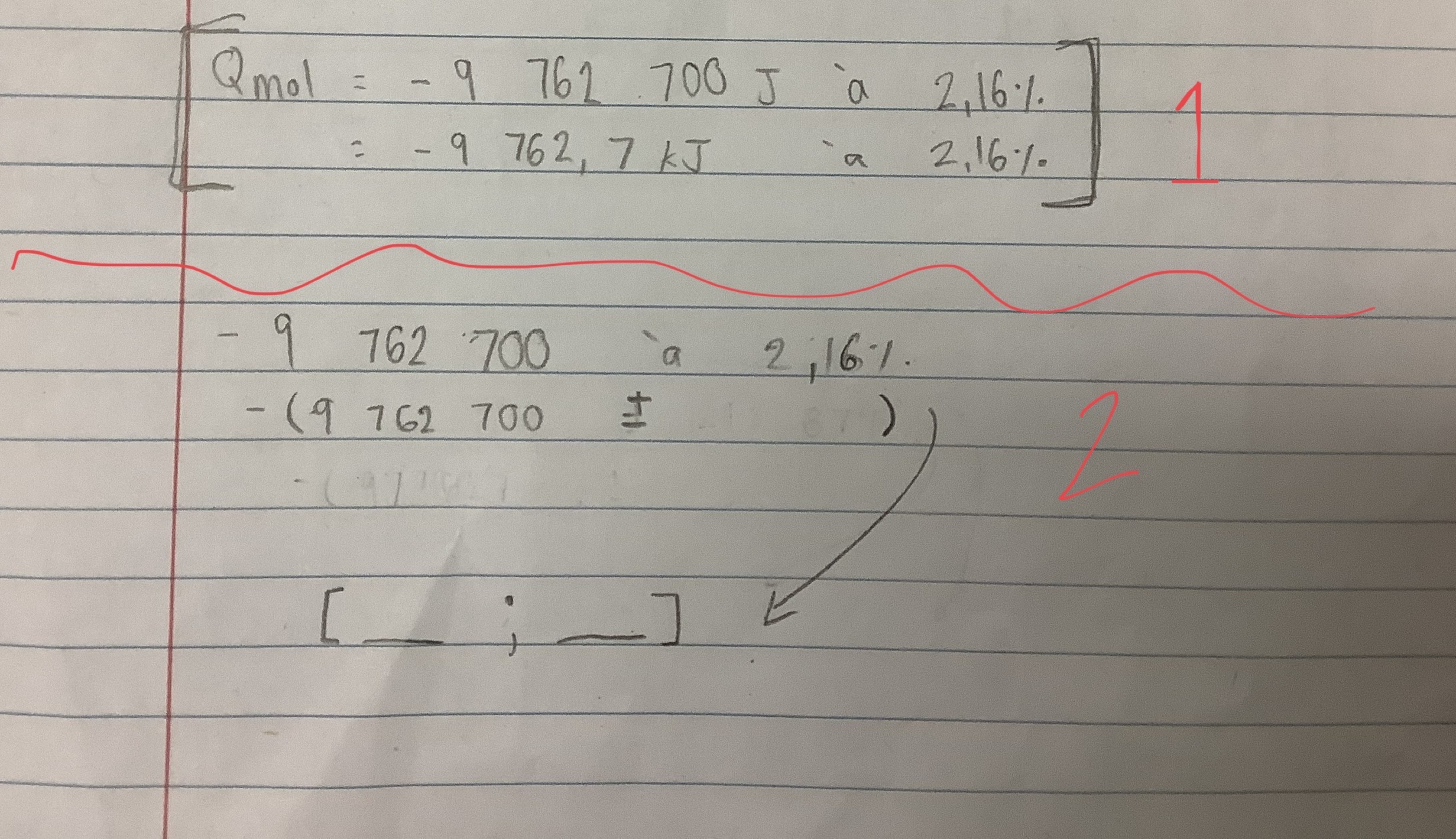Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, je ne comprend pas comment trouvé la masse dans ce numéro:
Dans un calorimètre contenant 1,25 L d'eau, tu fais brûler une quantité de paraffine telle que la température de l'eau monte de 38,3 °C. Sachant que la paraffine a une chaleur massique de combustion de 43,5 kJ/g, calcule la masse de paraffine qui a été brûlée dans ce calorimètre.
-
Vérifiée par Alloprof
Postsecondaire • 1aBonsoir à tous !
J'espère que vous allez bien !
Je vous écris concernant l'exercice suivant, pourriez-vous m'aider à le résoudre svp ? :
Fe₂O₃ (s) + Al (s) -> Fe (l) + Al₂O₃ (s)
On veut produire 15g de Fe, combien faudra t-il utiliser de réactifs ?
Je vous remercie par avance pour votre réponse !
Très belle soirée 😉🤞
-
Vérifiée par Alloprof
Postsecondaire • 1aBonjour, est ce que quelqu'un pourrait m'apporter son aide pour l'exercice suivant en me détaillant les étapes de résolution svp ? : La combustion de 11,5g d’un alcool (CxHyOz) a donné 22,0g de CO2 et 13,5g d’eau. Sachant que sa masse molaire est égale à 86,18g/mol, trouvez sa formule moléculaire.
Je vous remercie par avance pour votre réponse !
TRÈS BELLE SOIRÉE ! 😊
-
Vérifiée par Alloprof
Secondaire 5 • 1aQuelle est l'équation thermochimique de la dissolution de du NH4Cl dans de l'eau? Comment on l'écrit si l'énergie par mol est de 12kJ par mol?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour! J'ai un laboratoire en chimie demain et j'aimerais savoir dans le matériel, on nous offre un bol de glace. J'aimerais savoir s'il est nécessaire d'utiliser de la glace pour refroidir l'acide et la base avant les manipulations ou si on obtiendrait le même résultat sans la glace. Merci beaucoup!
-
Vérifiée par Alloprof
Secondaire 5 • 1aC'est quoi la chaleur molaire de dissolution du CaCl2 théorique?
-
Vérifiée par Alloprof
Secondaire 1 • 1aBonjour,
Pourriez m'expliquer quel sont les 6 postulats de la théorie particulaire de la matière ?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour à nouveau. J'ai essayé de répondre à cette question de différentes manières, mais je n'ai jamais obtenu de réponse. Quelqu'un pourrait-il m'aider à décomposer la question ? Je vous remercie.
Déterminez la chaleur molaire de combustion de CH4, à l’aide des données calorimétriques suivantes:
•CH4 + 2 O2 ==> CO2 + 2 H2O. •Masse de CH4 : 12 g
•Masse de O2 : 18 g
•Volume d’eau: 1 L.
•Température initiale de l’eau: 20 °C. •Température finale de l’eau: 32 °C.
-
Vérifiée par Alloprof
Secondaire 2 • 1aUne transformation à laquelle les propriétés chimiques restent les mêmes, s'agit-il d'un changement chimique, un changement physique ou aucune de ses réponses.
Merci
-
Vérifiée par Alloprof
Secondaire 2 • 1aLorsque nous faisons cuire un œuf, s'agit-il d'un changement chimique, changement physique ou aucune de ces réponses ?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aQuel est la bonne résolution de ce problème de bilan énergétique en chimie sec 5. La bonne réponse doit être delta H= 1.29 x10^3 kj/mol
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, je ne comprends pas vraiment le bilan énergétique. Au secours!
-
Vérifiée par Alloprof
Secondaire 4 • 1aQuel est le cycle d'azote. Les diverses étapes. Comment les étapes ont été crée. Il sert à quoi? Pourquoi sont-ils là? Quelle est leur fonction/utilité?
-
Vérifiée par Alloprof
Secondaire 5 • 1asalut comment calculer la masse molaire d’un élément?
-
Vérifiée par Alloprof
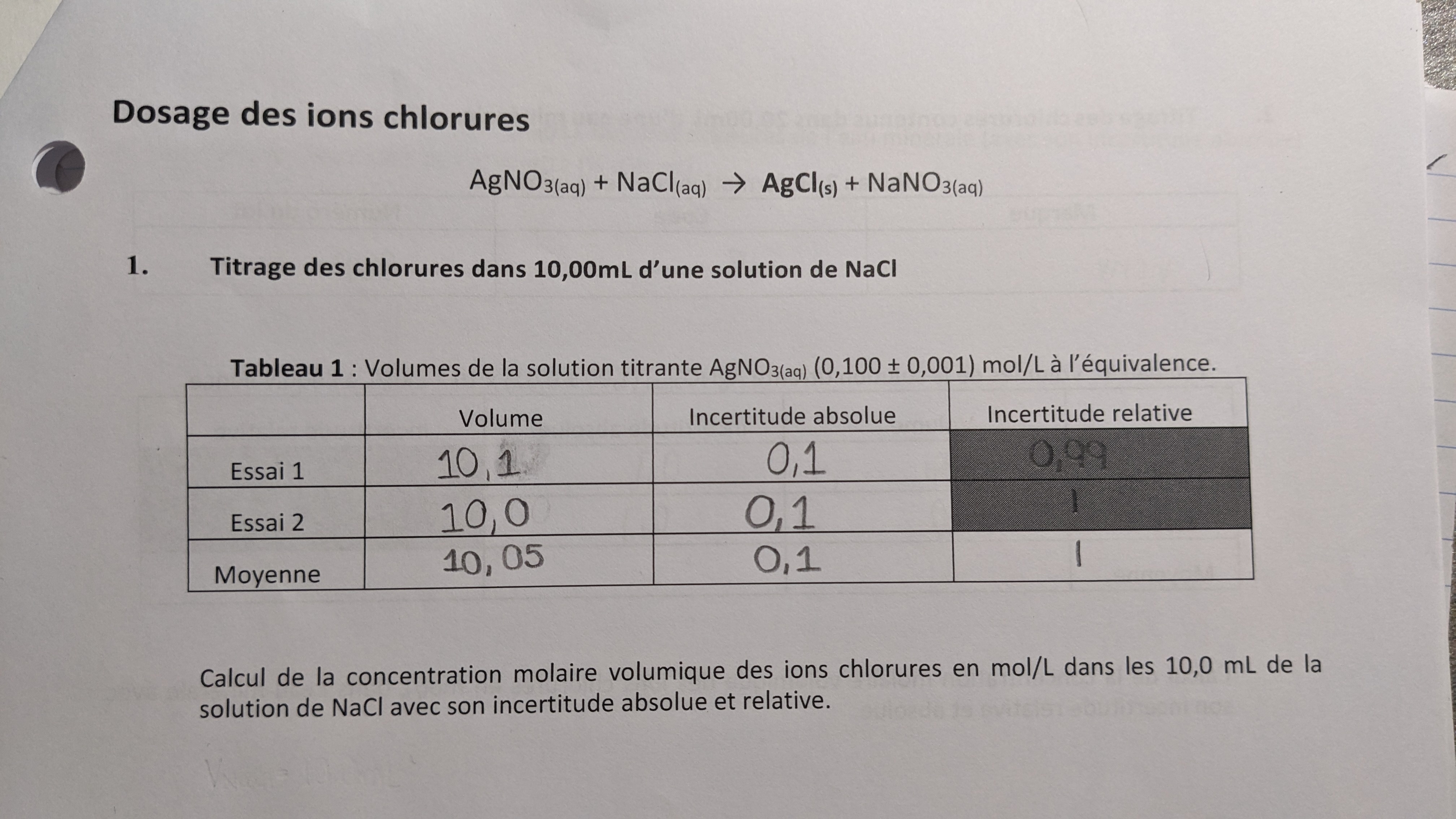
Secondaire 5 • 1aBonjour, j'ai 2 questions. Tout d'abord, la première chose entre parenthèses est-elle correcte ? La deuxième question concerne les calculs d'incertitudes. Comment passer du pourcentage aux parenthèses ?
-
Vérifiée par Alloprof
Postsecondaire • 1aBonjour,
quelqu'un peut m'expliquer étape par étape avec une démarche claire ce que je suis sensé faire.merci d'avance
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Je travaille sur mes exercises de chimie mais malheureusement je n’ai pas le corrigé et l’examen est demain. J’apprécierais que quelqu’un regarde mon exercise est me dise si je me suis trompée quelque part.
Merci d’avance à la personne qui m’aidera.
-
Vérifiée par Alloprof
Secondaire 5 • 1aCombien de chiffres significatifs dans 0,0ml, car je fais PV=nRt et j'ai 0,0000 L et alors je ne sais par combien de chiffres significatifs mettre dans ma réponse.
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour c’est encore pour la question de hier comment le fait de savoir en faite comment qu’elle pourrait être la formule la plus probable. J’ai mal compris merci beaucoup
-comment le fait de savoir qu’on a 1,33 fois plus de (‘?) vas moi aider selon les ml?
-
Vérifiée par Alloprof
Primaire 5 • 1aJe nais vrm rien compris à ce numéro ça fait des heures que je suis dessu et rien de change svp comment on fait
-
Vérifiée par Alloprof
Secondaire 5 • 1abonjour, j’ai galéré plus de deux heures sur ses deux problèmes, est ce que vous pourriez me montrer de a à z comment les faire, merci énormément.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, je ne comprends pas vraiment la différence entre un système isolé et un système fermé en calorimétrie.
Merci!
-
Vérifiée par Alloprof
Postsecondaire • 1aPourquoi il ne faut pas conditionner la fiole jaugée lors d'une préparation de solution ?
-
Vérifiée par Alloprof
Secondaire 5 • 1asalut j'ai besoin d'aide avec un exercice de chimie
Vous plongez un bloc de métal chaud dans 255 grammes d’eau à 22,5°C. Après un certain temps, la température de l’eau monte à 25,5°C. Sachant que la capacité thermique de l’eau est de 4,184 J/g°C, quelle quantité d’énergie l’eau a-t-elle acceptée du métal?
-
Vérifiée par Alloprof
Secondaire 5 • 1aallo j'ai besoin d'aide avec un exercice en chimie
Un cylindre d’O2 utilise pour respirer par le patient atteint d’emphysème a un volume de 3,00 L a une pression de 10 atm. Si la température de la bouteille est 28 oC, quel est la masse d’oxygène dans la bouteille ?
-
Vérifiée par Alloprof
Primaire 6 • 1aquelle deux éléments ensemble explose?
-
Vérifiée par Alloprof
Secondaire 5 • 1aJ'avais ça a faire en exercice suppementaires (facultatif), mais je nai pa été capable de le faire :!
Vous devez préparer 100,0 g de solution H2SO4 de fraction molaire 0,00500 à partir d’une solution De H2SO4 concentrée à 62,0 %m/m dont la masse volumique est de 1,52 g/mL. Calculer le volume de la solution de H2SO4 concentrée à mesurer ainsi que le volume d’eau à ajouter, en supposant que la masse volumique de l’eau est de 1,00 g/mL. Calculs complets.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, comment résoudre cette question?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour. C'est quoi tout à fait une orbitale, et pourquoi lors de la configuration électronique, 4s viens avant 3d?
-
Vérifiée par Alloprof
Secondaire 5 • 1asi on a 140 ml plus ou moin 3 ml et on veut transformer la donner en L comment on change l’incertitude. aussi si on a 23,0*C plus ou moin 0,1*C d’incertitude et que je change ma température en kelvin comment je change l’incertitude??