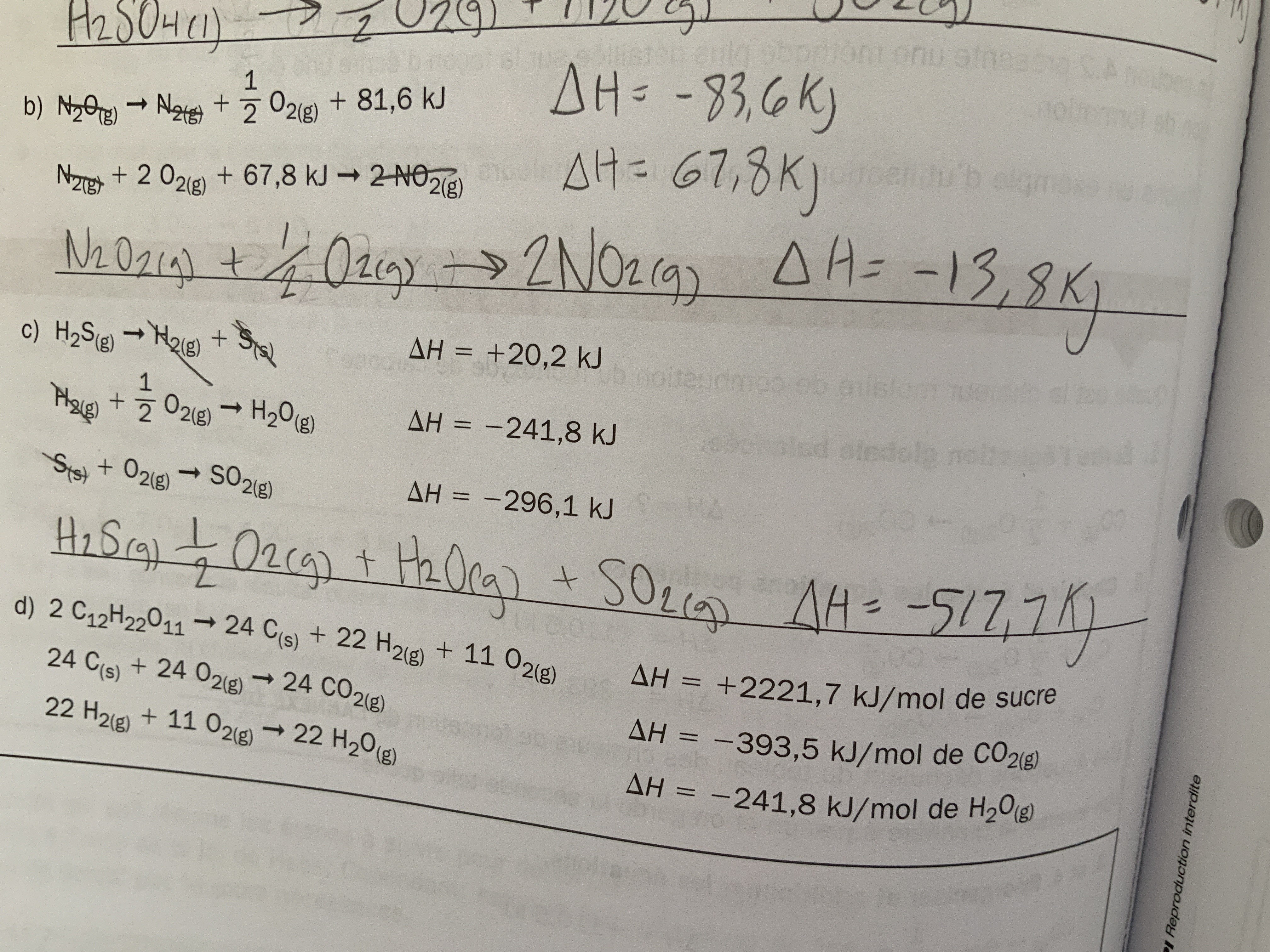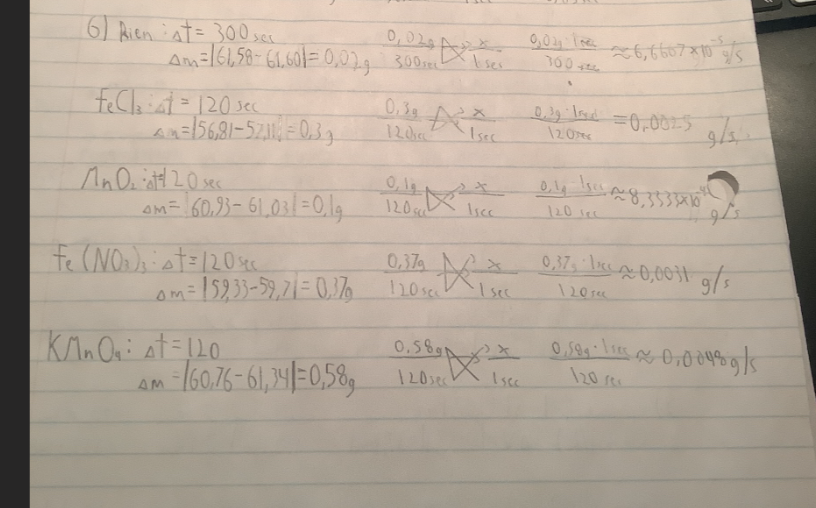Liste de discussions
-
Vérifiée par Alloprof
Secondaire 1 • 1aComment on calcule le volume
-
Vérifiée par Alloprof
Secondaire 5 • 1aquel est le l'élément chimique qui porte le nom de Albert eistein
-
Vérifiée par Alloprof
Secondaire 5 • 1aSerait il possible d’aider avec la résolution de ce problème? ( oubliez les calculs en bas)
-
Vérifiée par Alloprof
Secondaire 2 • 1aQuelle est la composition chimique de la surface de Mars. Car j'ai trouver qu'il était composer d'un désert de poussière et de cailloux, de roches très riches en fer mais ce n'est pas chimique. ??
-
Vérifiée par Alloprof
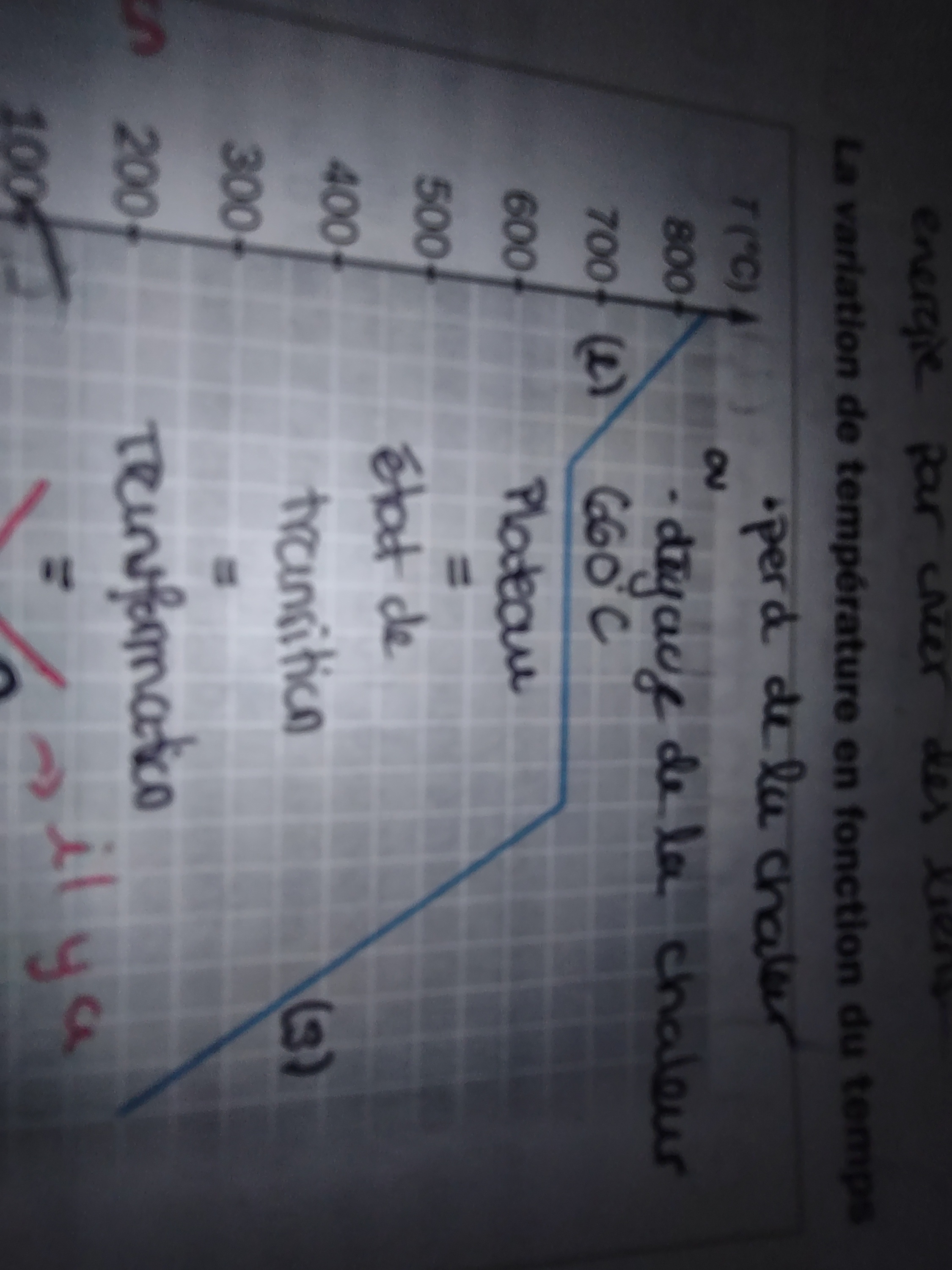
Secondaire 5 • 1aSalut !<br> Je ne comprend pas le plateau de ce diagramme<br> C' est — Alloprofvoila les donnees manquantes
Ici l'axe des x indique le temps et la 4e - 12e minutes c est le le temps du plateau .
merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aC'est quoi la différence entre de l'eau liquide et de la vapeur d'eau , précisement en quoi l'état liquide différe de l'état vapeur? Au niveau des liaisons,etc. ?
merci
-
Vérifiée par Alloprof
Secondaire 5 • 1abonjour , j ene comprend pas le est consomme par suffisament de fluor ? merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour ! Est-que la chaleur molaire de dissolution est une propriété caractéristique? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aCher Ramzi Z,
la première question à laquelle vous m'aviez répondu (même la deuxième) n'étais malheureusement pas suffisante.
S'il vous plait, j'aimerais une réponse (une explication) plus développée et non seulement l'envoi d'un lien vers une page d'Allo-Prof (même si cela parle du sujet)
Si vous ne me répondez pas adéquatement, mieux vaux voir ailleurs que Chez Allo-Prof..
Avec Sincéritée,
Hirondelle truc bucheee
-
Vérifiée par Alloprof
Secondaire 5 • 1aPour une plongée à l’air, comment calculerez-vous la pression partielle du diazote à une profondeur donnée ? (À l'aide des notions vues en secondaire 5)
Encore une fois, celui qui me répondrera, ne me donnez pas de liens d'Allo-Prof et\ou m'expliquer brievement.
J'écris le message pour justement comprendre le sujet et\ou répondre éventuellemnt à la question.
À la personne qui me répondrera correctement:
Merci ÉNORMÉMENTTTT!!!!
-
Vérifiée par Alloprof
Secondaire 5 • 1aÀ l'aide des lois des gaz (parfaits, général et simples), Comment pourrions-nous répondre à cette question: Comment pourrez-vous calculer la pression à une profondeur donnée sous l’eau ? (C'est une question de laboratoire)
S'il vous plait, la personne qui répondera à mon message, expliquez moi bien, ne m'envoyez pas un lien d'Allo-prof et juste m'expliquer en bref.
Je pose cette question pas pour recevoir un lien ou autre, mais pour comprendre la matière (ou juste pouvoir répondre à la question)
Merci énormément de votre aide (si c bien fait)
❤️❤️❤️❤️❤️❤️❤️❤️❤️
-
Vérifiée par Alloprof
Secondaire 5 • 1aÀ l'aide des lois des gaz (parfaits, général et simples), Comment pourrions-nous répondre à cette question: Comment pourrez-vous calculer la pression à une profondeur donnée sous l’eau ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aComment pourrez-vous calculer la pression à une profondeur donnée sous l’eau ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe ne comprend absolument rien. C’est de la loi de Hess. Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aSalut !
Je ne comprend pas le plateau de ce diagrammeC' est 18.0g de Al qui se solidifie.
Donc je aimerai avoir plus de détails au niveau du plateau
Pk. 1. la variation de température ne change pas, 2.comment les liaisons du solide se forme si l énergie est dégagée ( donc il y en a pas pour former des liaisons), 3.est ce que cette transition dégage de la chaleur ou en absorbé? ( Même si en général c' est Exo) Parce que on me demande pour la question de dire combien y avait d énergie entre la 4e et 12 et minute . J'aurai mis 0 car Q=mc∆T et ∆T =0 mais ils disent qu elle est de 7.21kj ( comment💀 ?!?)
Une autre pas vraiment un peu en lien avec ça
4. La chaleur molaire de fusion de l aluminum correspond a la chaleur molaire de solidification de celui ci juste le signe négatif , est ce que cela s applique a tout les autres substances , genre la réaction contraire a la même chaleur molaire juste il faut changer le signe ?
Merci encore.pour vos services!👍
-
Vérifiée par Alloprof
Secondaire 5 • 1aSaluT!
icije ne comprends pas vraiment quoi represente ces équations ? je sais cest en rapport avec la chlaleur molaire , mais je sais pas pourquoi c est different?
Ce qui me derange c est si on veut connaitre la quantite d energie degagee par chacun des reactifs on obtient des reponses differentes..
par exemple dans la premeire eqn je dirai qu'une mole de O2 produit 483.6kj
et deux moles de H2 produisent (483.6 x 2 )kj
ensuite pour la deuxieme eqn
une mole de O2 produit 241.8kj
et deux moles de H2 produisent (241.8 x 2 )kj
les reponses sont differentes ? je pense que mon erreur c est que pour faire ce compte il faut se basait sur l'element principal de la reaction dans ce cas la synthese de la molecule H2O ( etant donne que une molecule O2 possede 498kj d energie et non 486.6 kj ), alors le bon compte serait de dire
2 moles de H2 produisent (241.8 x 2 )kj
et une mole de O2 produit 241.8kj
je suis pas sûr , au niveau de cette affaire , est ce que vous pouvez me clarifier tout ca un peu plus svp ?
aussi (😅) le terme chaleur de reaction est il different de chaleur molaire , si oui , dans ce cas la chaleur de reaction serait celle du H2O meme si elle est sa chaleur molaire vu que c est le but de cette reaction produire du H2O, mais si j avais mis -486.6kj/mol ce serait faux parce que c est juste la chaleur molaire du O2 ?
merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour ! J'aurais besoin d'aide pour la rédaction d'un rapport de labo. Je me demandais précisément ce qu'était le complexe activé ? Est-ce qu'il varie selon chaque substance ? Si oui, qu'est-ce qui le fait varier ? Et si deux substances sont à la même température, le complexe activé sera-t-il le même ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aSalut!
Est ce que vous pouvez me montrer comment trouver le réactif limitant et en excès en stoechio? Je n' AI pas trouvé de fiches.
Merci encore!
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe comprend pas trop votre réponseJe pense avoir fait une erreur ici ,comment ça se fait que les deux équations veulent dire la même chose mais sont différentes?
Même si j AI dit que chacun est écrit en fonction d une substance de la réaction, je sais pas si ce que je dis est bon?
La peut être erreur iciEnsuite j AI la même question pour cette équation : est ce que c' est bon de écrire comme ça , genre mes kj/mol ils sont bien égaux aux proportions dans la réaction?Donc ici pour savoir en fonction de quoi j AI mis ma chaleur molaire c' est souligné en vagues.
Merci !🐢
-
Vérifiée par Alloprof
Postsecondaire • 1aEst-ce que la réaction exo est plus rapide que la réaction endo?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aSalut!
Ici j AI était savoir si je peux écrire cette équation thermique de ces deux manières différentes, je parle pas du fait de mettre la chaleur dans le équation où a l' extérieur de celle ci avec un ∆H , mais au niveau de ... Par rapport a quelle substance on va écrire notre chaleur molaire.Donc pour la première manière de écrire je la ferai en fonction du H2 donc
H2+Cl2-->2HCl + 92.3kj
H2+Cl2-->2HCl ∆H = - 92.3kj/mol
Ou 2 manière en fonction du 2 Hack
H2+Cl2-->2HCl + 186.4kj
H2+Cl2-->2HCl ∆H= - 186.4kj/mol ( ou 92.3kj/mol. **2ieme question)
Merci !
-
Vérifiée par Alloprof
Postsecondaire • 1aLa solubilité d’un composé est de 32.2g/100mL à 25 ∘C et 37.6g/100mL à 108 ∘C. Si une solution saturée du composé à 108∘C est autorisée à refroidir lentement jusqu’à 25∘C, quelle est la quantité maximale de cristaux solides qui peut être obtenue ?
Rendement max :
-
Vérifiée par Alloprof
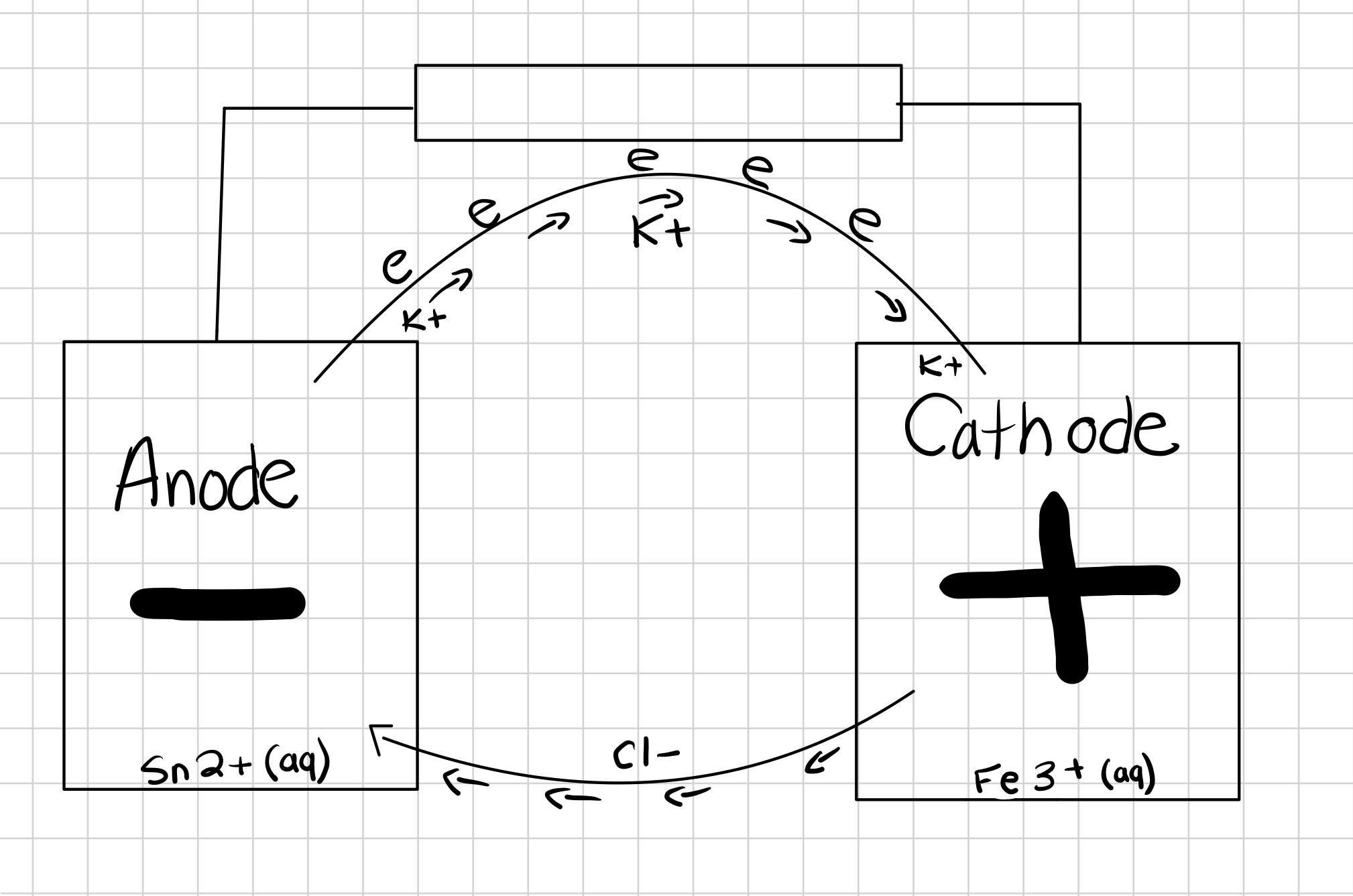
Secondaire 5 • 1aest-ce que mon schéma est correct?
voici la question:
Faire un schéma de la pile sur lequel le sens de circulation des électrons est précisé ainsi que le sens de migration des ions K+/Cl- dans la jonction électrolytique
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour, je ne comprends pas se fait la distribution des électrons dans les orbitales et comment on fait pour écrit la formule de lewis
-
Vérifiée par Alloprof
Secondaire 1 • 1aC'est quoi la chimie
-
Vérifiée par Alloprof
Primaire 4 • 1aQu’est-ce qu’un hydrocarbure ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Je suis entrain de faire des exercices sur la loi de Hess. Je dois déterminer l’équation thermique avec des mécanisme de réaction. Deux numéro de suite je suis arrivé à la bonne réponse sauf pour le O2. J’ai écrit 1/2 mais je suis censé arriver à 3/2. Je ne comprend pas comment je suis supposé arriver à cette réponse. Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, on vient de faire un labo avec différents catalyseurs et je comprends comment il fonctionne, mais je ne comprends pas pourquoi les différentes substances affectent mes résultats différemment.aidez-moi SVP!
-
Vérifiée par Alloprof
Secondaire 5 • 1abonsoir, j’aimerai savoir la dissolution d’une mole d’acide sulfurique donne quoi équation chimique ?
-
Vérifiée par Alloprof
Secondaire 5 • 1aEst ce que quelqu’un peut m’expliquer comment calculer le bilan énergétique car mon professeur me l’a expliqué mais je n’ai pas compris