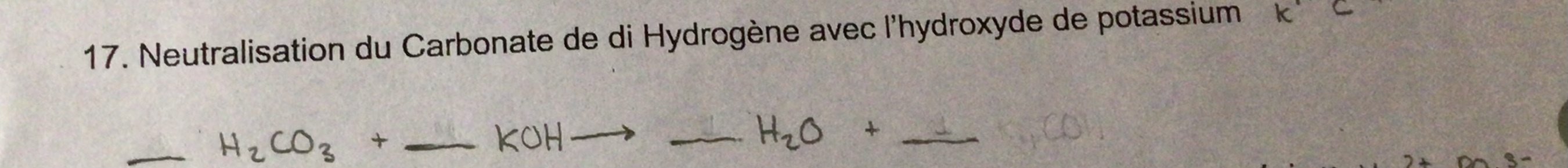Liste de discussions
-
Vérifiée par Alloprof
Primaire 4 • 1apouvez vous ajouter encore d'autre noms posible? comme des nourritures ou d'autre animaux moi jamerais etre PizzaAlpha101!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Qu'est ce que je peux mettre comme cause d'erreur pour le spectrophotométrie?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 1avoici ma question précedante:
salut, comment pourrais je calculer la vistesse instantané d une reaction en mol/s si j’ai deja la valeur de la vitesse instantanée en mL/s? c’est quoi la firmule qui m’aidera a convertur ces valeurs? merci pour votre reponse.
donc vous m’avez dit de calculer le nombre de mol avec la formule de pv=nRT et j ai eue un nombre de mol= a (1,02 x 10 exposant -4) mol
ainsi que j au deja ma vitesse instantanée de la réaction en unite de mL/s = (5,4 ) mL/s
donc ma question c’était a partir de ses donnes ( le nombre de moles de ma réaction ainsi que sa vitesse instantanée en mL/s) comment je peux calculer la vitesse instantanée en mol/s svp?
votre réponse m’aidera énormément!! merci bcp!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, quelle est la différence entre la dissociation et la dissolution?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Dans l'exercice suivant, nous avons doublé la quantité d'énergie afin de mieux balancer l'équation de la formation du CS2.
Mais dans la question, ils nous demandent de mettre le résultat en KJ/mol. Mais puisque nous avons doublé la quantité d'énergie, je ne comprends pas comment cela est toujours considéré comme KJ/mol (-296,8 x 2) KJ/mol.
Donc même si nous doublons ou triplant ou peu importe la puissance, la réponse demeura sous l'unité de KJ/mol?Merci!
-
Vérifiée par Alloprof
Postsecondaire • 1aBonjour, j'ai ce problème dans mon devoir et je n'arrive pas à le résoudre. Quel sera le pH d'une solution aqueuse de CH3CH2COOH 0,00035 mol/L sachant que le pKb de l'ion CH3CH2C00- est égal à 9,00.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, si j'ajoute un réactif dans une équation chimique, qu'arrivera t'il à la concentrations des réactifs ainsi que des produits?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, je ne comprends pas pourquoi un lave-vaisselle en marche s’agit d’un système ouvert.
Merci!
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour,
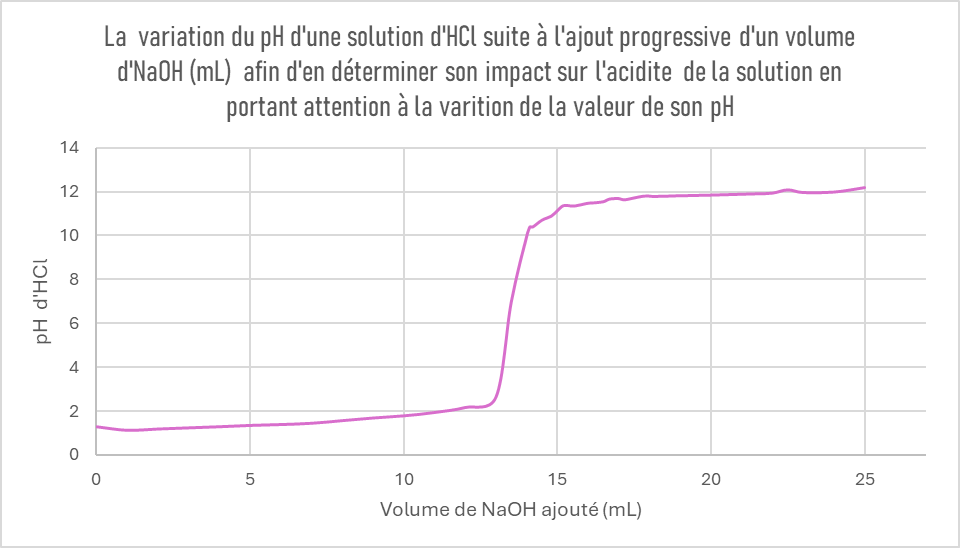
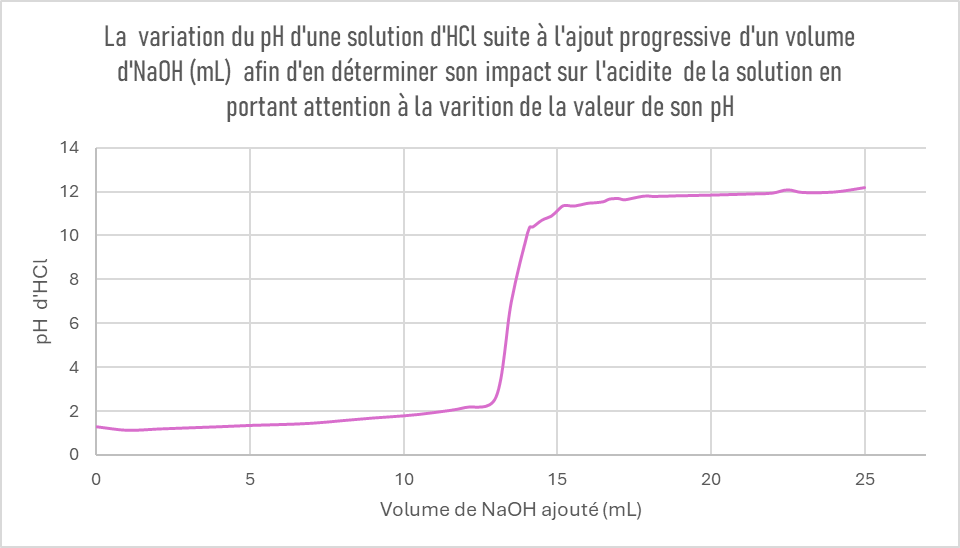
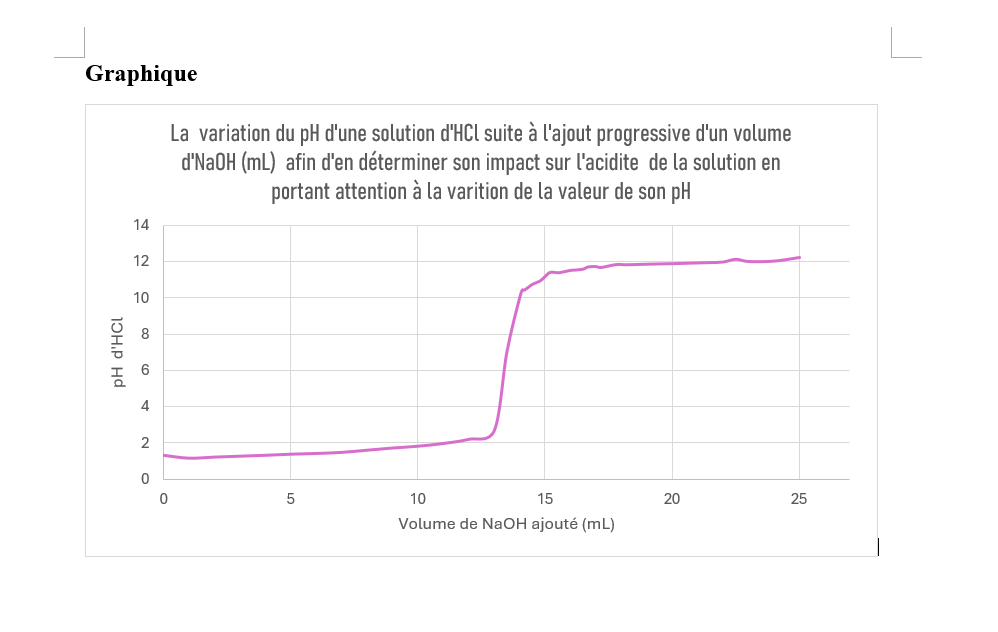
Je dois faire un rapport de laboratoire qui est centré sur l'influance d'une base sur le pH d'une solution acide. Le but de ce laboratoire est d'observer l'effet de la solution basique sur le pH de la solution acide. La courbe du graphique obtenu grâce à mes résultats est très semblable à une fonction exponentielle et une fonction logarithmique fusionnées ensemble. J'aimerais savoir si vous pouver me donner une définition claire de ces deux fonction puisque nous n'avons jamais rien appris sur celle-ci.
Merci d'avance!
-
Vérifiée par Alloprof
Secondaire 4 • 1aD'accord, merci pour ces précisions!
Cepedant, j'aimerais une petite confirmation, est-ce que la section avant le point de virage dans ma courbe est une fonction exponentielle ? Si oui, est-ce que cette fonction est aussi caractérisé par une pente lente? Aussi, qu'est-ce qui est à l'orginie du changement de fonction dans la courbe?
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour,
j'ai un rapport de laboratoire sur l'effet d'une base sur le pH d'un acide à rendre que je ne comprend pas vraiment. On doit expliquer ce qu'est une fonction logarithmique ainsi que la maniére dont elle varie afin d'expliquer la manière dont le pH varie. Je n'arrive pas a faire cela car nous n'avont jamais appris la notion de fonction logarithmique.
-
Vérifiée par Alloprof
Secondaire 4 • 1aMerci beaucoup pour votre indice! Cependant, comment puis-je formuler la «croissance rapide» dans mon analyse? J'ai bien peur que cela ne soit pas suffisant. Est-ce que les fonctions logarithmiques sont caractérisé par une varition rapide?
Aussi, pour ce qui est du plateau de la courbe, voulez-vous parler de la droite verticale dans la courbe? Car je dois avouer, que j'ai beaucoup chercher là-dessus, mais je n'ai malheureusement rien trouver de concré ni comprehensible.
Aussi, d'après notre prof de math, il serait possible qu'il y a deux fonctions dans la courbe, mais je ne sais pas si c'est correct à 100%.
Merci!
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour, je suis désolée, mais j'ai encore une autre question.
J'aimerais savoir comment peut-on faire un bon lien entre la variation d'une fonction logarithmique et la variation de pH? Quel paramètre serait le plus utile? (Prenez en considération que nous ne voyons pas les fonction logarithmique en SN4 cette année, alors s'il vous plait, soyez le plus clair possible, car je ne connais rien à propos de cette fonction)
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour, j'ai vraiment besoin d'aider sur mon rapport de laboratoire. Je suis bloqué à un point de mon analyse et la remise de ce travail est mardi.
S'il vous-plaît, j'aurais besoin d'une explication claire sur comment je peux analyser cette courbe en utilisant des notions de fonction logarithmique. (Le labo consitait à determiner l'effet qu'à l'ajout d'une base (NaOH) dans une solution acide (HCl) )
-
Vérifiée par Alloprof
Secondaire 4 • 1aSalut,
je fais de la chimie plus précisément des transformation chimie et je ne comprend pas quelle atome prendre lorsqu'il est temps de former un sel dans la neutralisation acidobasique.pouvez-vous m'aider?
merci
-
Vérifiée par Alloprof
Secondaire 5 • 1asi j’ai à calculer l’ordre d’un réactif à partir de trois expériences’ est-ce que je suis obligée de toujours prendre la première expérience (expérience 1) avec une autre ou je peux choisir l’expérience 2 et 3 ?
Et est-ce que la concentration doit toujours doubler ou je peux prendre 1 où ça triple
-
Vérifiée par Alloprof
Secondaire 5 • 1abonjour, lors d'un labo, je dois comparer les facteurs qui influencent la vitesse de réactions. Mes criteres sont la concentration et la grosseur de molécules. je devais faire des tests entre une petite molécule à 3 moles et à une mole et une grosse à 3 moles. evidemment, celle à 3 moles qui est plus petite est la plus rapide, sauf que je ne sais pas quel facteur serait le plus influant entre les deux. comment je pourrais le savoir?
Merci
-
Vérifiée par Alloprof
Secondaire 4 • 1aMerci beaucoup! Toutefois, comment dans mon analyse je justifier l'allure de la courbe avec la notion de fonction logarithmique ?Pourquoi est-ce que le graphique commence doucement, puis tout à coup il monte à pH=7, puis recommance à monter doucement? Merci!
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonsoir! Le but du rapport est de déterminer qu'elle est l'influence de l'ajout d'une solution basique dans une solution acide.
Pour ce qui est de ma deuxième question, j'aimerais savoir, comment je peux faire une analyse dans rapport de laboratoire sachant qu'il s'agit d'une courbe de pH entre un acide fort et une base forte. Ma professeure de science à glisser un indice comme quoi il faut l'analyser avec la notion d'une fonction logarithme, mais puisque c'est une notion de secondaire 5 et que nous sommes en secondaire 4 STE, il faut faire beaucoup de recherche à ce sujet. Pourreiz-vous m'aider? Merci!
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour, je vais expliquer ce que j'ai fait et vous pourriez peut-être m'indiquer si quelque chose est mauvais!
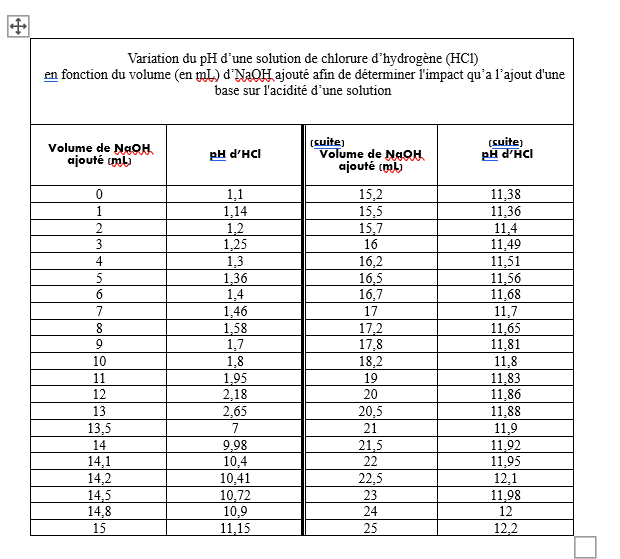
1) j'ai calculer la concentration mol/L de mon HCl avec son pH en utilisant la valeur trouvée en laboratoire avant d'avoir ajouté du NaOH
10^-pH = [H+]
[H+] =10^-1.1 ≈ 0.079mol/L
ensuite j'ai trouvé son nombre de moles avec la formule C= n/V (nous avions 10mL que j'ai ensuite convertis en Litres pour trouver le n)
Par la suite, j'ai utilisé C1V1=C2V2 pour trouver la concentration molaire de NaOH quand le pH de HCl. Nous savons que à 13,2 mL de NaOH, le pH =7.
Après avoir trouvé mon C2, je trouve le n avec C=n/V pour pouvoir dire dans mon analyse qu'il y a autant de moles d'ions H+ que OH- à pH 7
Pour trouver mon nombre de moles de OH- avant un pH de 7 du HCl, j'ai pr un volume de NaOH ajouté quand le pH de HCl est inférieur à 7 et j'ai utilisé C=n/V (le C est la concentration trouver avec le C2V2=C1V1) et j'isole ensuite le n
Pour le nombre de moles après un pH de 7, c'est la même chose avec un volume de NaOH quand le pH d'HCl est plus que 7.
Voila!
J'ai aussi une autre question! Comment je peux analyse mon graphique pH (la courbe de pH entre l'acide fort HCl et la base forte NaOH) en utilisant la notion de fonction logarithm? Merci beaucoup !
-
Vérifiée par Alloprof
Secondaire 5 • 1aQu'est-ce-que l'ordre des réactions?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour si je soustrais des données avec des incertitudes différentes, par exemple 10.01 +- 1.0 - 2.05 +- .001 - 4.2 +- 0.2 = 3.76 +- .799
Donnée absolue = 3.8 +- 1 parce que je prends la donnée d'incertitude absolue la moins précise?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
C'est quoi la différence entre la vitesse de réaction et la vitesse moyenne?
Merci
-
Vérifiée par Alloprof
Secondaire 4 • 1aMerci beaucoup pour cette explication détaillée! Cependant, comment comment je peux trouver la concentration pOH si je n'ai pas pris la mesure du pH du NaOH lors de l'expérience?
Toutefois, nous savons que le volume total de NaOH titré est de 25mL à la fin de l'expérience et que le pH du HCl à la fin de l'expérience était de 12.
Auriez-vous une idée sur comment me guider là-dessus? Merci!
-
Vérifiée par Alloprof
Secondaire 4 • 1aMais en calculant C1V1=C2V2 à pH 7, on trouve la concentration de NaOH?
Selon ma professeure de science, nous devons trouver le nombre de moles avant l'équivalence, à l'équivalence et après l'équivalence afin de prouver qu'effectivement, le nombre de mol = nombre de mol a ph7 que avant le nbr de mol de HCl et plus grand que nbr de mol de NaOH et etc.
Cependant, je ne sais pas comment procéder pour trouver ce nombre de mol de NaOH avant l'équivalence ni après.
-
Vérifiée par Alloprof
Secondaire 4 • 1aMerci beaucoup pour l'explication! Cependant, maintenant que je peux calculer la concentration à pH 7, comment je peux trouver la concentration de NaOH avant que le pH d'HCl soit 7? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
j’aimerais comprendre pour quelle raison Esce que la deuxième variation d’enthalpie (deltaH2) est multiplié par deux. (Surlignée en jaune)
merci beaucoup!
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour, toujours en lien avec ma question précédente, serait-il possible d'avoir la formule exacte à utiliser pour trouver le nombre de moles de NaOH avant et après le pH de 7? De plus, juste pour en être certaine, qu'elles sont les variables indep, dep et constante de ce labo? Merci!
-
Vérifiée par Alloprof
Primaire 5 • 1asalut j'aimerais savoir comment peux t'on faire un volcan multicolore
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir, je me demandais comment il est possible de transformer des millilitres d'une solution en moles. Par exemple, j'ai 0,653 ml de NaHSO3 et je dois le transformer en mole.
(Je sais que la formule n= C/V existe, mais je ne sais pas comment trouver la concentration?)