Liste de discussions
-
Vérifiée par Alloprof
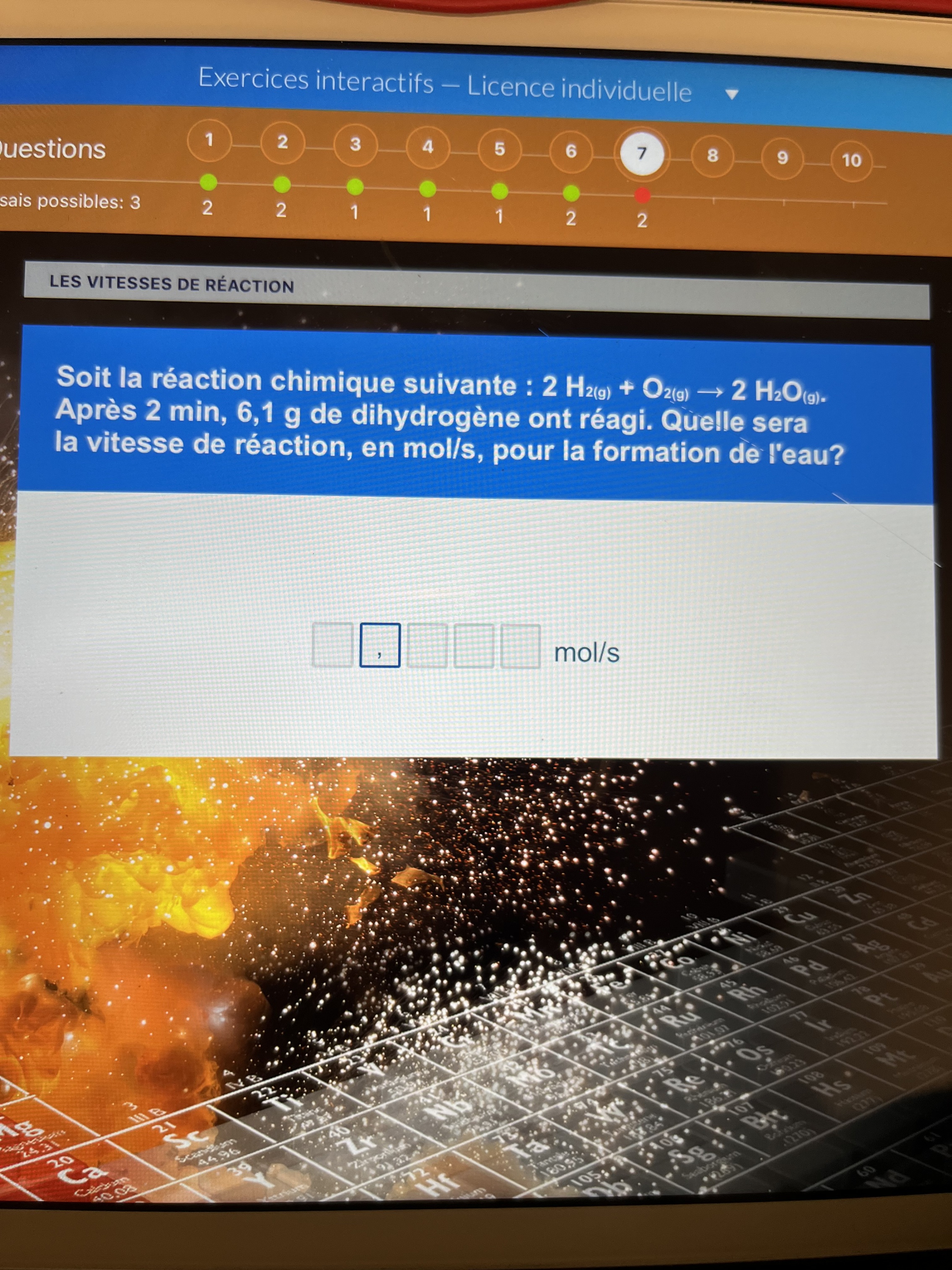
Secondaire 5 • 1aJe n’arrive pas a trouver la réponse correcte, la réponse dit que c’est 0,025 mol/s mais je veux savoir la démarche pour en arriver la svp
-
Vérifiée par Alloprof
Primaire 5 • 1aque veut dire H20 en chimie
-
Vérifiée par Alloprof
Secondaire 4 • 1abonsoir,
comment résoudre une équation de stœchiométrie mais avec la formule C1V1 = C2V2
-
Vérifiée par Alloprof
Secondaire 4 • 1abonsoir,
je ne comprend absolument pas pourquoi dans les réactions endothermiques, il y a plus d'énergie dans les produits si l'énergie est du côté des réactifs et vice-versa pour les réactions exothermiques.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir
je ne suis pas sure si ce système si c'est ouvert ou fermé
1- La réaction de précipitation du chlorure d'argent (AgCl) à partir du chlorure de sodium
(NaCl) et du nitrate d'argent (AgNO,) dans une éprouvette ouverte.
Lequel des systèmes suivants est à l'équilibre?
La coque d'un bateau qui rouille sur un rivage.
- Une bougie qui brûle et dont la lueur est constante.
- La réaction d'un ruban métallique avec un acide dans un ballon fermé, qui fait augmenter la température dans le ballon.
- Un ballon fermé contenant un mélange gazeux de dihydrogène de diiode et d'iodure d'hydrogène (HI) où la pression, la température et la couleur du mélange sont constantes.
-
Vérifiée par Alloprof
Secondaire 5 • 1aQuelqu’un peut m’aider pour ceci svp?
-
Vérifiée par Alloprof
Secondaire 5 • 1aJe ne comprends pas ce qu’il faut faire, quelqu’un pourrait m’aider svp?
-
Vérifiée par Alloprof
Secondaire 5 • 1aUne réaction à 25 °C se fait en 60 s. On la reprend à 10 °C. En combien de temps se fera-t-elle? La réponse est 171 secondes. Comment arriver à cette réponse?
-
Vérifiée par Alloprof
Secondaire 5 • 1aUne réaction à 25 °C se fait en 60 s. On la reprend à 10 °C. En combien de temps se fera-t-elle?
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, j'ai récemment fait un laboratoire sur la loi de Hess et je ne comprends pas ce que je fait de mauvais.
Le but du laboratoire était de trouver la valeur de la chaleur de formation du monoxyde de magnesium d'une réaction.
On a essayé deux reactions :
Mg + 2 HCl -> MgCl2 + H2O (Cela nous a donné une variation de 37 degrés celsius)
MgO + 2 HCl -> MgCl2 + H2O (Variation de 7 degrés Celsius cette fois-ci)
La quantite de MgO et de Mg était de 0.50g (solide) pour chacun et celle du HCl était de 50ml
Lorsque j'ai essayé de trouver la valeur de la chaleur dégagé des deux réactions par calorimétrie, cela ma donné une valeur de 3763 J pour la réaction du Mg et 1180J pour le MgO.
Je sais aussi que dans cette réaction, il y a une reaction qui crée de l'eau dont sa chaleur de formation est de 284kJ/ Mol.
D'apres la loi de Hess, si on additionne l'enthalpie de chacune de ces réactions , cela va nous donner la chaleur de formation du MgO et c'est ce que j'ai fait. Malheureusement, cela ma donné une valeur qui est loin d’être similaire à la chaleur de formation théorique du MgO qui se retrouvait dans mon cahier d'activité. Je ne comprends pas pourquoi mon resultats diffère de la théorie.
Alors, si possible, j'aimerais avoir de l'aide pour savoir ce que j'ai fait de mal.
Merci énormément d’avance.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, pour chimie sec 5 chapitre 6.4 sur la loi de la vitesse de réaction, je ne comprends pas comment la constante (k) fonctionne, d'ou vient les unités pour et comment après quand tu fais un calcul comment tu faits, par exemple si ma concentration est à la 2, estceque les unités sont a la deux aussi, puis comment ça seneleve et tout??
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
K de l'eau à 25 C est 1,0 x 10^-14.
Si on augmente la temperature, est ce que
- on n'a plus d'équilibre
- L'eau s'ionise plus
- PH ><7
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour, comment trouver le nombre de mol pour être capable de trouver le concentration en faisant c=n/v lorsque nous avons seulement la vitesse de réaction en litre par seconde ? Merci !
-
Vérifiée par Alloprof
Primaire 4 • 1aallo!
j'aimerais que on m'aide pour le jeu : Réaction solitaire.
j'aimerais comprendre mieux les balancement des équations chimiques.
merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aComment calculer avec une calculatrice casio:
(6,02 x 10 exposant24 x 22,4) divisé par (6,02 x 10 exposant 23)
-
Vérifiée par Alloprof
Secondaire 5 • 1aQuels sont les facteurs qui influencent la vitesse de combustion de la paraffine solide?
-
Vérifiée par Alloprof
Secondaire 5 • 1aComment je suis censé m’y prendre..
-
Vérifiée par Alloprof
Secondaire 5 • 1aComment faire ces 2 numéros svp :
Voici une série de transformations :
- Hg) +2,29 kJ → Hgo
- La dissolution de l'hydroxyde de potassium (KOH) qui fait augmenter la température de l'eau.
- Des vêtements qui sèchent sur une corde à linge.
- La réaction C(s) + O2(g) → CO2(g) où l'enthalpie contenue dans le COz est inférieure à l'enthalpie totale contenue dans C et dans O2.
- 2 NO2(g) → N2g) + 2 0г(g) ДН = 33,2 kJ/mol
Parmi ces transformations, lesquelles dégagent de l'énergie?
- a et c
- b, c, d et e
3. a, d et e
b, d et e
Exercice 2
Un artisan en moulage fabrique un moule à tarte antiadhésif en acier inoxydable dont la masse est de 420 g. Pour ce faire, l'acier est chauffé à une très haute température, puis refroidi rapidement dans 5,00 L d'eau à une température de 16,2 °C. La température finale de l'eau est de 21,9 °C. Sachant que l'acier inoxydable possède une capacité thermique massique de 0,450 J/g • °C, initialement.
calculez à quelle température il a été chauffé
-
Vérifiée par Alloprof
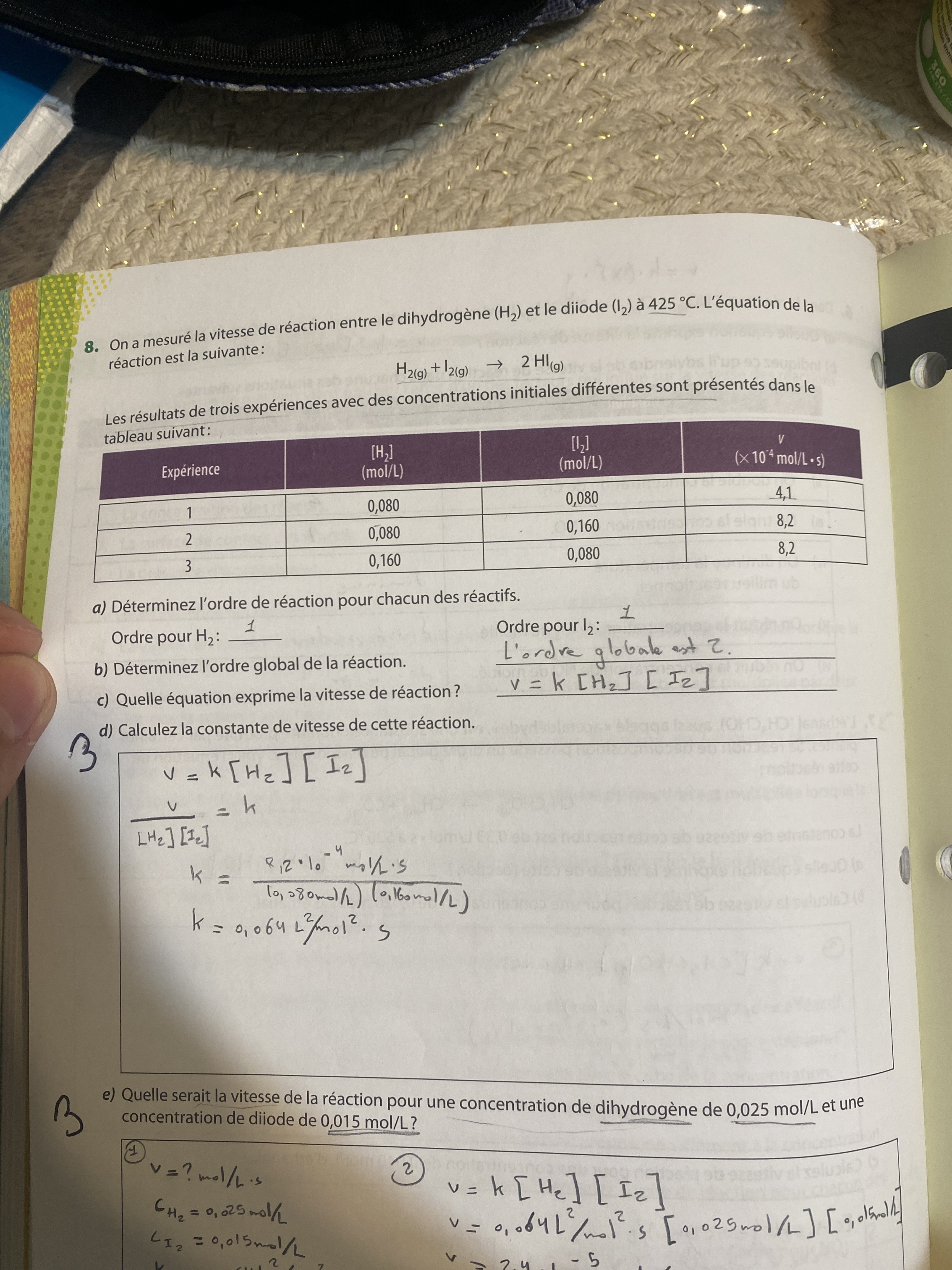
Secondaire 5 • 1aA la question D, pourquoi choisir t on cette vitesse pour trouver la constante de vitesse?
-
Vérifiée par Alloprof
Secondaire 5 • 1aSerait il possible d’expliquer le probleme c? La multiplication par 4 dans le processus de calcul m’a causé de la confusion, mais de ce qui parait il est relié a la question b.
-
Vérifiée par Alloprof
Secondaire 5 • 1aPourriez vous s’il vous plaît m’expliquer cas par cas cette question sur l’ordre des réactions et leur effets dependement de la vitesse et la concentration dans cette question? Je l’avais déjà fait mais maintenant n’arrive plus à comprendre le logique
-
Vérifiée par Alloprof
Secondaire 5 • 1aJ’aimerais avoir de l’aide sur la vitesse de réaction ainsi que les facteurs qui l’influencent et la théorie des collisions
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
J'aurais une question sur la mise en situation suivante:
Nous avons initialement 1,50 mol de NO2 dans un contenant ayant une capacité de 4,00 L. Le NO2 se décompose en NO et O2 selon l'équation suivante:
2NO (g) + O2 (g) = 2 NO2 (g)
Le K est égal à 6,4 x 10⁹
La question est de trouver la concentration du NO (g) à l`état d`équilibre chimique de la réaction.
Après avoir rempli le tableau ci-dessous, j`ai essayé d`isoler x. Malheureusement, je n'ai pas obtenu de carré parfait, me laissant alors sans aucune valeur pour x (la formule quadratique n'était pas applicable) .
Y aurait-il une faille dans mon tableau?Vos explications seraient très appréciées.
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonjour,
Pourriez-vous me dire comment on doit trouver la concentration du métal en fonction du temps s'il vous plaît? Je ne sais pas comment il faut trouver ces données là.Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aComment est-ce que je mesure un volume dans une seringue et quelle est son incertitude?
-
Vérifiée par Alloprof
Secondaire 5 • 1apouvez vous m’expliquer comment faire ce type de problème et trouver la réponse
-
Vérifiée par Alloprof
Secondaire 5 • 1aest-ce que les 5 facteurs qui influencent la vitesse de réaction chimique peut avoir un impact sur l’énergie d’activation. Donc le fait d’augmenter la température va en quelques sortes réduire l’énergie d’activation?
-
Vérifiée par Alloprof
Secondaire 5 • 1aJ'ai besoin de valider ma compréhension sur pourquoi le CO2 et le H2 augemente;
Mon hypothèse c'est qu'une réaction gazeuse se déplace de là ou il y a le plus de molécules (réactifs) à l'endroit avec le moins de molécules (produits) pour permettre le système à atteindre l'équilibre.
Corriger moi si j'ai tort, merci!
-
Vérifiée par Alloprof
Secondaire 5 • 1aBonsoir!
J’ai de la difficulté à différencier les réactions directes et inverse. Je suis présentement dans le chapitre 6 et je vois le principe de Le Chatelier. Plus précisément, la concentration des substances.
Puis-je avoir de l’aide svp? Merci
-
Vérifiée par Alloprof
Secondaire 4 • 1aBonjour,
En secondaire 4, y a-t-il une distinction entre la variation d'enthalpie molaire et le bilan énergétique (d'une réaction chimique)?
Peut-on utiliser les deux formules ci-dessous inversement?
- Bilan énergétique = énergie absorbée + énergie dégagée
- ΔH = ΔHréactifs + ΔHproduits