Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! Pouvons-nous prévoir expérimentalement si une réaction est endothermique ou exothermique ?
Car, par exemple, c'est deux réactions sont des dissolution, et pourtant l'une est endothermique (eau et KNO3) et l'autre et exothermique (eau et LiCl)Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mJ'ai une question. Pour une neutralisation acidobasique, est-ce qu'il faut le même volume d'acide que de base ? Dans un exercice où il y avait 75 mL d'acide et 100 mL de base, ça dit que la base est en excès (réactif limitant). Faut-il les mêmes volumes ?
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/115415/questionMais, dans ce cas-là, par exemple, une réaction endothermique absorbe l'énergie, sa température augmente, non?
En soit, qu'est-ce qui est considéré comme l'environnement d'une réaction? Si on mélange de l'eau et du KNO3 par exemple, une endothermique, est-ce que l'eau est considéré comme l'environnement, du pourquoi la température baisse?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour, en lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/115412/questionJe ne suis très sûre de comprendre comment déterminer le signe de delta H à l'aide de la variation de température
Merci!
-
Vérifiée par Alloprof
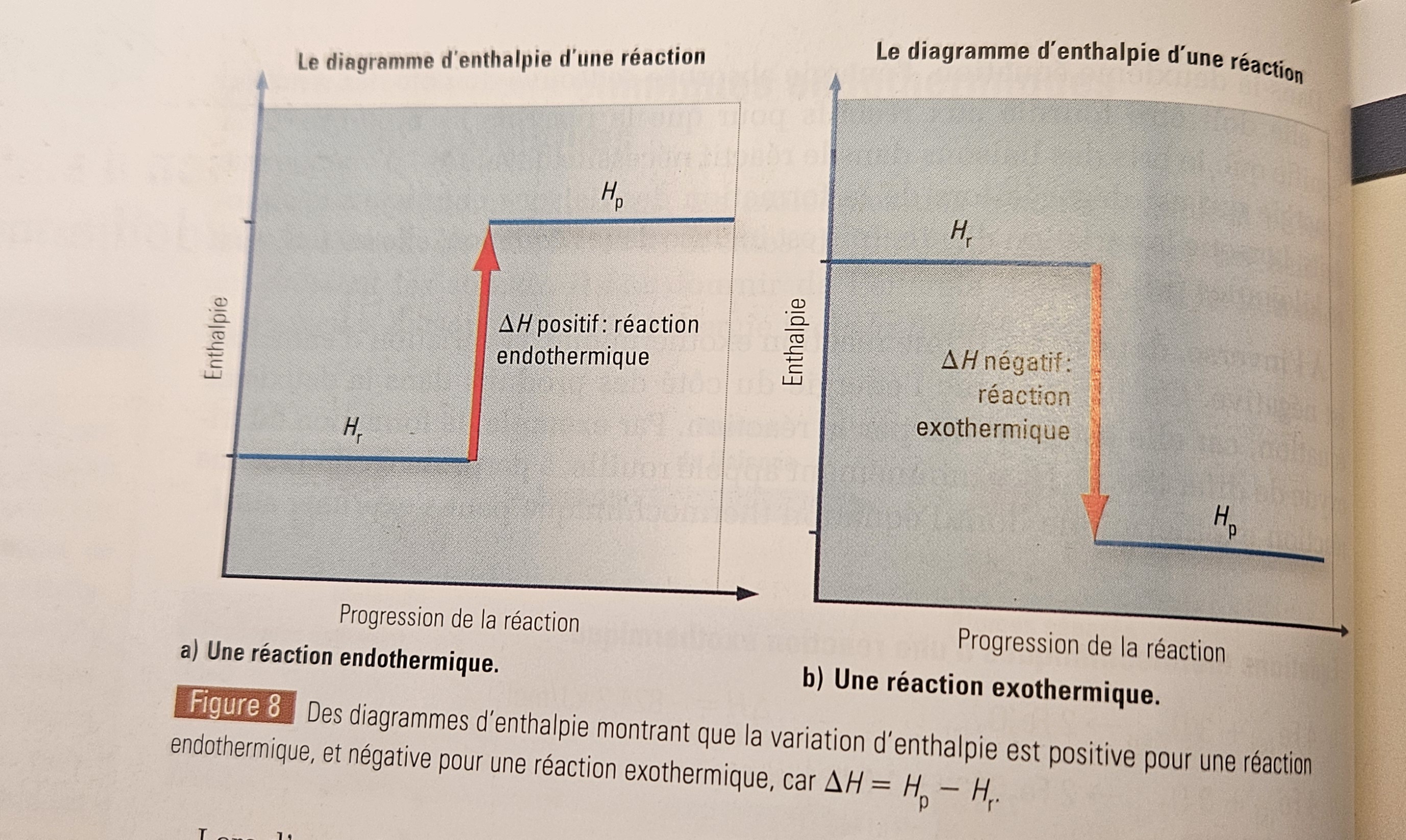
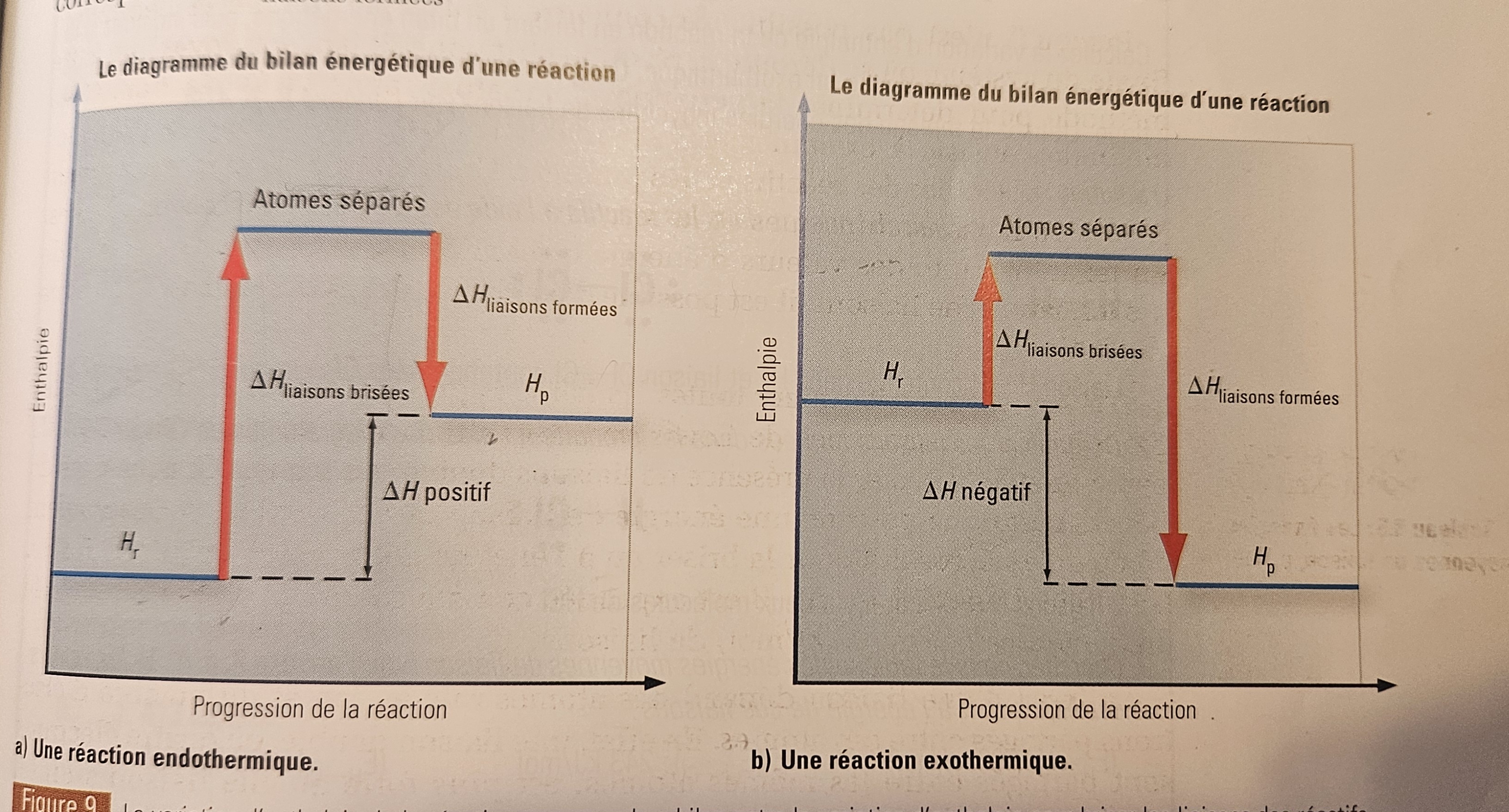
Secondaire 5 • 11mBonjour! Je vais essayer d'expliquer ce que je comprend du pourquoi une réaction endo (en expérience) fait descendre la température du thermomètre et une réaction exo la fait monter, puis, s'il vous plait, corrigé moi si je n'ai pas bien saisi le concept!
Endo: Une réaction endothermique nécessite d'absorber de l'énergie pour se produire (afin de briser les liaisons des réactifs). Ainsi, quand nous mettons un thermomètre dans notre bécher où se déroule une réaction endothermique, la réaction va absorber l'énergie du thermoètre pour favoriser le bris des lisaisons. Ainsi, vu que l'énergie a été dégagé du thermomètre, c'est un comme si, du point de vu du thermomètre, la réaction est exothermique (car le thermomètre dégage de l'énergie). Cette perte d'énergie cause au thermomètre d'afficher une température plus basse ?
Exothermique: Une réaction exothermique dégage de l'énergie, notamment à cause de la formation de nouvelle lisaison chimique de produits. Le thermomètre vient donc, lorsqu'on le met dans le bécher, absorber cette énergie dégager. En absorbant cette énergie, la température indiquée monte?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour, comment pouvons nous écrire l'équation thermchimique dans cette situation si on a juste les delta T et si c'est endothermique/exothermique? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! Je ne comprend pas pourquoi il y deux formule pour la variation l'enthalpie d'une réaction. Qu'est ce qui les diffères?Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour, j'ai la masse du gaz, la température et la pression. Je n'ai pas le volume ni la quantité de mol ni le nom du gaz. La question demande qu'elle est la masse molaire. Je sais que la deuxième étape doit etre n=m/M, mais je ne sais pas quelle doit etre la première étape. Certains m'ont dit de faire les gaz parfait ou la règle générale des gaz, mais je n'ai pas de donné inicial ou finale vue que c'est une question théorique, donc je ne peux pas faire la règle générale des gaz. Aussi, comme je n'ai ni volume (v) ni quantité de mol (n) je ne peux pas appliquer la règle des gaz parfait. Pouvez-vous m'éclairer sur comment faire ou comment trouver le volume pour ensuite trouver la quantité de mol (n)? Merci beaucoup pour votre temps et votre aide! Passer une bonne journée!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour, je cherche une formule qui contient la masse, la pression et la température, mais je n'ai pas le volume et je ne sais pas comment le trouver et le but final est d'identifier le gaz et donc de trouver n. Merci beaucoup pour votre temps et votre aide!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour,
Est-ce nous qui décidons quel est le milieu pour déterminer si une réaction est endothermique ou exothermique? Par exemple, si je décides d'étudier la sueur et que je décide de mesurer la température du corps, puisque la température du corps va diminuer, alors suer est une réaction endothermique. Mais si je décide de mesurer la température de la sueur et que celle-ci va augmenter, alors c'est une réaction exothermique. Donc dépendant de notre choix du milieu, une situation peut-être endothermique ou exothermique?
Merci de clarifier ceci, bonne journée!
-
Vérifiée par Alloprof
Secondaire 5 • 11mSalut, quelle serait une formule avec la masse, la température et la pression qui permettrais d’identifier un gaz?
Merci et bonne fin de journée !
-
Vérifiée par Alloprof
Secondaire 3 • 11mPourquoi lorsqu’on mélanges 5g d’acide citrique et 5g de bicarbonate de soude dans 25ml d’eau une réaction ce produit , tandis que si on mélange 10g de bicarbonate de soude dans 25 ml d’eau et 10g d’acide citrique dans 25ml d’eau rien ne se produit?
Et quelle type de changement chimique se produit-il?
-
Vérifiée par Alloprof
Postsecondaire • 11mBonjour,
J'ai de la difficulté avec l'isolation du X dans mes équations, quel sont les règles de base pour savoir par quoi commencé ?
Aussi : si j'ai une racine sur mon équation de gauche et un exposant 2 dans mon équation de droite, est-ce qu'automatiquement les deux s'annulent ?
Merci d'avance!!
-
Vérifiée par Alloprof
Postsecondaire • 11mQuel volume d'eau bouillante faut-il ajouter pour réchauffer 100ml d'eau à 25°C afin que sa température atteigne 65 °C?
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! Je ne suis pas sûre de comprendre ce que le corrigé a fait:On demande pas de trouver Q pourtant? Mais delta T...personnellement, j'avais trouvé que celle du cuivre aurait une température plus élevé d'environ 2,34... merci!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! Pourquoi ici au a), on parle du Becher et de son contenu, mais au c) d) e) et f) on parle pas des contenu des systèmes? Par exemple, pourquoi on dit pas l'eau et la bouillotte au c)? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir, je ne suis pas sûre de comprendre ceci, pourriez-vous m'aider? Merci:
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/115163/questionMerci beaucoup pour l'explication! Toutefois, je dois avouer que je ne suis pas sûre de comprendre comment même définir si la réponse finale possède le bon nombre de chiffres significatifs avec toutes les calculs dans cette même formule. Merci :)!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/115160/questionMerci beaucoup pour l'explication et j'espère que vous aviez également passé de bonnes vacances :)!
Juste question d'être sûre que j'ai bel et bien compris!:Dans un calcul comme celui-ci, il faudrait donc tenir compte des C.S. pour le m2c2Ti2, ensuite des CS pour le m1c1Ti1, pour le m1c1, pour le m2c2, puis pour le m2c2Ti2 + m1c1Ti1, pour le m1c1 + m2c2 puis le C.S de la division des deux somme?
Car je dois avouer que cela semble très long, surtout lors d'un examen...
Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir? Comment pouvons-nous tenir compte des chiffres significatifs dans une formule comme celle de la température finale? Devons -nous tenir compte des chiffres significatifs pour chaque mini calculs dans la formule ou il faut procéder autrement?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour,
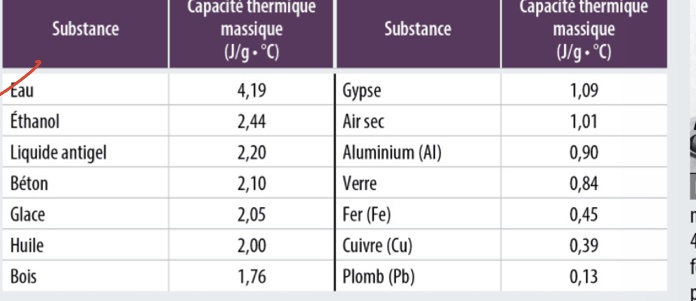
je voulais Just savoir si c’est eu comme réponse la capacité thermique massique est 0,44 est ce que c’est du fer ou c’est du cuivre.J’arrondis à quel substance
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir, je ne comprend pas ici pourquoi l'astronaute est un système ouvert et pourquoi l'environnement n'est pas la station spatiale mais l'espace? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! Pourquoi ici Tf serait 0°C si le 0°C est le point de fusion? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! Si nous additions deux nombres, comme 53.3433 et 61.6857, la somme donne115.029. Mais, ici, comment peut on avoir 4 chiffres après la virgules si on veut respecter la règles des chiffres significatifs avec des addtions? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! Quand nous effectuons plusieurs calculs dans un problème qui ne demande qu'une seule donnée comme réponse (donc, par exemple ici on voulait le c du métal, mais nous devions faire un petit calcul de Tf pour trouver ∆T), doit-on mettre en place les bons chiffres significatifs pour chaque calcul? Donc par exemple, aurais-je du mettre 49°C au lieu de 48.5°C pour le 1) trouver Tf? Et utiliser le 49 dans le calcul suivant? (Puis continuer comme ceci jusqu'à trouver mon c? )
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonsoir! Comment doit-on procéder pour tenir compte des chiffres significatifs dans un problème comme ceci:Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! Je ne suis pas sûre de comprendre la distinction entre entre un transfert par travail et par chaleurDès qu'il y a un mouvement, c'est un travail? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! Pourquoi le congélateur est considéré comme un système isolé? Merci!Également, pour on considère pas le verre et l'eau comme deux système différents? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! Je ne suis pas sûre de comprendre ceci:La question était si la chaleur dégagé par l'eau serait suffisante pour fondre la glace. Toutefois, le point de fusion est 0 degré, ainsi, comment la réponse peut être «oui» ? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 11mBonjour! Je suis confuse de cette réponseC'est pas plutôt l'inverse? La chaleur du bois n'est pas plus grande que celle du verre? Merci!