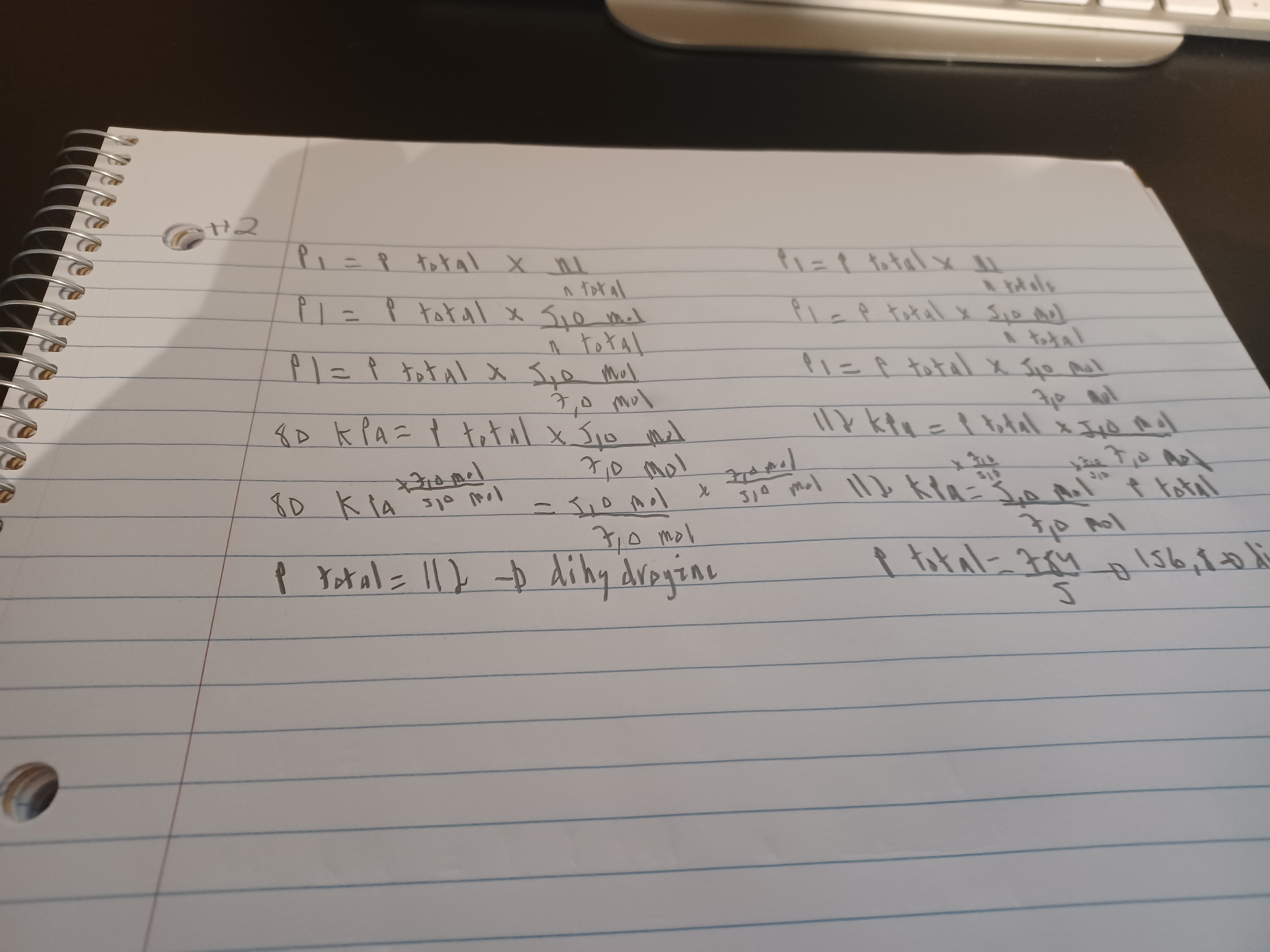Liste de discussions
-
Secondaire 4 • 3a
Bonjour. J'aimerais savoir quels ions peuvent être dissous dans l'eau?
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour, j’aimerais que vous me dîtes s’il vous plaîtsi c’est juste merci
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour, est-ce que vous pouvez me corrigez s’il vous plaît merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aMa question est qu'est que il au bout de l'infinie
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
...
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
...
SVP si vous pourriez m'éclairer en détail sur les démarches suivies!
Merci!
-
Vérifiée par Alloprof
Secondaire 3 • 3a1+1 sa egale a quoi????
-
Vérifiée par Alloprof
Secondaire 5 • 3aJ’ai besoin de la réponse du 4 et 5 merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aQuestion 4 5 et 6 s’il vous plaît. Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 3aLa questions 11 et 12 s’il vous plaît.
-
Vérifiée par Alloprof
Secondaire 5 • 3aSi vous plongez sans avoir fait de manœuvre d’équilibrage, à quelle pression est votre oreille interne ?
...
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, j'aurais besoin d'aide pour cette question merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, pouvez-vous m'aider à faire cet exercices? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, j'espère que vous allez bien... J'aurais une petite question concernant la chimie...
...
15,06 L d’une solution de KOH à une concentration de 0,073 mol/LCruche 2:23,40 L d’une solution de H2SO4 à une concentration deCruche 3:3,01 L d’une solution de CaCO3 à une concentration de 0,36 mol/L
En faite, l'objectif de ce devoir est de neutraliser les déchets tout en entraînant un coût minimal pour le laboratoire. Puis nous avons à notre accès:
- Une solution de NaOH concentrée à 0,15 mol/L,coûtant 2$ /100ml
- Une solution de HCl concentrée à 0,1 mol/L,coûtant 2,25$ /100ml La question est donc de savoir le plan d’action détaillé pour neutraliser les déchets et le coût final d' opérations de neutralisation.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, pouvez-bous m'aidez à trouver une formule pour ce type de problème?
...
Si j'ai la cruche #1 contenant ces solutions:
6,23 L d’une solution de Mg(OH)2 à une concentration de 0,23 mol/L
15,06 L d’une solution de KOH à une concentration de 0,073 mol/L
et la cruche #2 contenant cette solution:
23,40 L d’une solution de H2SO4 à une concentration de 0,199 mol/L
Je dois neutraliser ces déchets et j'ai l'aide d'une solution de NaOH concentrée à 0,15 mol/L et une solution de HCl concentrée à 0,1 mol/L.
Je sais que la première étape est de mélanger la cruche 1 et 2 pour ensuite neutraliser à l'aide des solutions NaOH ou HCl dépendamment du PH positif ou négatif de la solution qui en résulte. A-t-il une formule possible pour trouver la concentration des 2 solutions de la cruche 1 lorsqu'elle sont mélangées?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
...
Pour la question b, selon l'annexe 11, la chaleur molaire de la fusion de l'aluminium est de 10,8kJ et vu que la fusion s'agit de S --> L, c'est donc une réaction endothermique (absorbant de la chaleur) donc façon #1 d'écrire la réaction : Al(s) + 10,8kJ --> Al(l). façon #2 : Al(s) --> Al(l) delta H : +10,8 kJ
Pour la question c et d, j'aurais besoin d'aide, que dois-je faire?
Merci et bonne journée! :)
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour j'ai de la difficulté avec cette question merci infiniment
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour, j’hesite entre l’option 1 et 3 vous me dire la quelle est juste Merci d’avance
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour, vous pouvez me dire quelle est la proposition juste s’il vous plaît merci
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour, quelle est la réponse s’il vous plaît
-
Vérifiée par Alloprof
Secondaire 4 • 3aL’atome d’Azote souhaite obtenir la même configuration que l’atome de Néon (Ne), pour cela il va :
...
gagner 2 électrons
perdre 3 électrons
perdre 3 électrons
-
Vérifiée par Alloprof
Secondaire 4 • 3aL’atome de Béryllium Be souhaite obtenir la même configuration que l’atome de :
...
Bore (B)
Néon (Ne)
Helium (He)
-
Vérifiée par Alloprof
Secondaire 5 • 3aSi j'ai un contenant étanche dans lequel j'enlève tout le gaz, y a-t-il une pression dans mon contenant?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir svp aider moi pour ce problème merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour j'ai fait la solution # 2 est-ce que c'est correct ? Et pour le # 1 je ne comprends toujours pas svp essayer de faire le # 1 avec moi. Comme vous voyez j'ai vraiment essayé. Merci beaucoup
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour j'ai fait la question # 1 et 2 est-ce que j'ai bien faite ? Si non svp pouvez-vous m'aider, il y a un prof qui m'aider, mais je ne comprends toujours pas, si vous pouvez faire juste ces 2 numéros avec moi je vais essayer de faire les autres toute seule. Merci du fond du cœur
-
Vérifiée par Alloprof
Primaire 3 • 3aQu'est ce que la fusion nuclaire?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour j'ai cette question que je ne comprends pas, pouvez-voussvp M'aider à le faire merci énormément
-
Vérifiée par Alloprof
Secondaire 5 • 3aJ’ai beaucoup de difficulté au niveau des tableaux IRF ( limitant, excès et information sur la question) et bien déchiffrer les informations avec les exercices de solutions (solvant,soluté,molalité,concentration de solution ,etc. ) . Je me demande s’il y’a des techniques pour mieux être à l’aise avec ça? Merci !
-
Vérifiée par Alloprof
Secondaire 4 • 3aComment résoudre s'il vous plaît ?