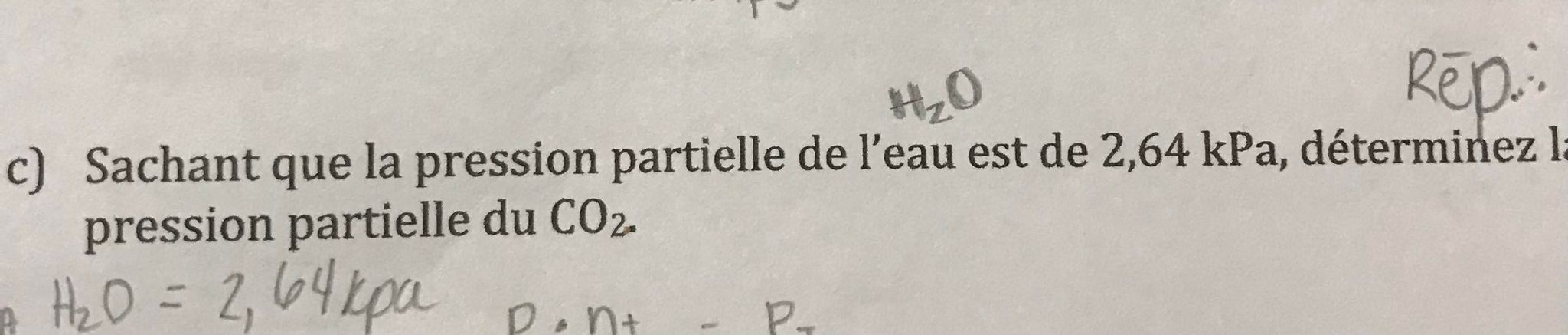Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, quelqu'un peut m'aider avec cette question ?
Merci d'avance,
FramboiseDynamique
-
Vérifiée par Alloprof
Secondaire 5 • 3aLors d’une expérience de calorimétrie, on observe que 50 ml d’un liqueur inconnu absorbé 3626J lorsque la température passe de 20.0°C a 55.0°C.
Calculer la capacité thermique (C) de ce liquide, sachant que sa masse volumique et de 1.120 g/ml.
Je ne sais pas comment procéder avec ce problème. Merci pour votre aide ! Quel sont les étapes requises pour régler ce problème ?
Comment isoler le C et la masse volumique de 1.120 g/ml sert à quoi? Et comment l’incruster dans le calcul si cela est nécessaire?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour !!
J'ai cette question et pour le point c) je ne trouve pas quel information je dois utiliser pour faire le calcul. De plus, pour le point e), je ne comprend pas comment trouver la réponse puisque on ne me donner aucune concentration dans les données du numéros.
Merci d'avance,
FramboiseDynamique :D
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour !!
J'ai cette question et j'ai de la difficulté a cerner ce que je dois faire avec les données qu'ils me donnent, surtout que la concentration du C8H18 est en ppm.
Quelqu'un pourrait m'aider ?
Merci d'avance,
FramboiseDynamique :D
-
Vérifiée par Alloprof
Secondaire 5 • 3aPourquoi les réactions élémentaires d’ordre 4 ne sont pas très rapides alors que normalement plus l’ordre de réaction est élevée plus la réaction est rapide
-
Vérifiée par Alloprof
Secondaire 5 • 3aQuels sont des exemples de combustions complètes et incomplètes dans la vie de tous les jours?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSi j'ai un volume de 0,45L, une pression de 2 atm, une température de 182C, quel sera le volume si la pression augmente a 404kPa et que la température diminue de moitié ?
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour,
Si je dois trouver un nouveau volume, mais que j'ai une température et une pression changé. J'ai la température, le volume et la pression de départ.
Quelle formule rassemble ces 3 données?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour petite question pour vous aujourd'hui : L’augmentation de la température aura-t-elle toujours le même effet sur l’équilibre?
Merci!!
-
Vérifiée par Alloprof
Secondaire 5 • 3aPouvez-vous m’aider à faire la partie c) et le reste
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
une autre question de chimie!
Je mesure une quantité d'O2(g), à pression de 101kPa et une température de 30C. Lors du prélèvement il y a une fuite; le nombre de moles initiale est de 0,0008mole pour un volume de 20 ml. Suite à la fuite, on a un volume de 17ml.
On cherche à savoir; le nombre de moles d'o2 qui se sont échappé? À quelle masse d'oxygène ça correspond ?
J'ai trouvé avec des simple produits croisé; la réponse serait 0,00012 moles perdus, soit une masse de 0,00384g. Est-ce exacte parce que le calcul me semble simple?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Si j'ai un thermomètre à gaz hélium, son volume est de 0,125L, température 0C et 1 atm de pression. On l'immerge dans de l'hydrogène en ébullition, la pression reste d'1 atm et son volume est maintenant 9,2ml.
On veut connaitre la température d'ébullition de l'hydrogène ? Comment faire ?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Mon problème est le suivant:
J'ai un échantillon d'ammoniac (volume inconnu) à 46 degrés celcius, exerce une pression de 510 kPa.
On cherche à savoir la pression si l'on réduit le volume à 1/10 de sa valeur originale?
Comment trouver le volume alors que mon volume est inconnu?
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Quel est la définition de FORME DÉFINIE?
-
Vérifiée par Alloprof
Primaire 3 • 3aUne expérience en trois étapes qui montre comment je peux modifier la masse volumique d'un liquide dans lequel baigne un objet.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Je ne comprend pas cette question vous pouvez m’aider svp.
Merci beaucoup
-
Vérifiée par Alloprof
Secondaire 4 • 3aComment je peux trouver la concentration
-
Vérifiée par Alloprof
Secondaire 4 • 3aJe sais pas comment trouver le volume
-
Vérifiée par Alloprof
Secondaire 4 • 3aJe me sais pas comment calculer
-
Vérifiée par Alloprof
Secondaire 5 • 3aL'équilibre chimique vue dans la vie de tout les jours? quelqu'un des exemples svp:)
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Est ce que la constante (k) est toujours la même dans une réaction si on ne fait que changer la concentration? par exemple, pour Mg+2HCl -> MgCl+h2 que je fais trois fois en changeant à chaque fois la concentration de HCl. Est-ce qu'en utilisant la loi des vitesses le k sera différent pour chaque formule?
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour,
serait-il possible de m'envoyer les structures chimiques de la phénolphtaleine avant et après le changement de couleur ?
Qu'est-ce qui fait en sorte que la couleur change (comment se comportent les structures chimiques) ?
Svp, me fournir des notions poussées car jaime la chimie!!!!!!!!!!!!!!
-
Vérifiée par Alloprof
Primaire 5 • 3aon étudie pas la chime en secondaire hien
-
Vérifiée par Alloprof
Secondaire 4 • 3aC8H18+O2 —>CO2+H2O
comment je peux balancée cette équation
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Mise en contexte: J'utilise un réchaud au propane (C3H8). La combustion produit: CO² et de l'eau. On utilise 50g de propane et le volume molaire de 24,5L (condition ambiante: 25 degré et 101 kPa.)
On veut connaitre:
Le volume de dioxyde de carbone produit?
Que devient le volume du CO2 si la température est maintenant de 100 degrés et pression normale?
Je ne comprend pas le chemin à prendre considérant le peu d'infos.
Voici ce qu'on ma répondu:
La première étape est d'écrire l'équation de combustion, la voici:
5O2+C3H8→3CO2+4H2O
On sait donc que la combustion d'une mole de C3H8 produit 3 moles de CO2. À l'aide de la masse molaire et de la stœchiométrie, tu peux trouver le nombre de moles de CO2 produites par la combustion du propane. Pour trouver le volume, tu n'as qu'à utiliser le volume molaire, s'il correspond au CO2, tu ne sembles pas l'avoir indiqué. Sinon, tu peux utiliser la loi des gaz parfaits, tu connais tout ce que tu as besoin.
Si la température est de 100°, le volume molaire change. En utilisant la loi des gaz parfaits, tu peux trouver le volume produit. Je te laisse essayer!
Ce que je veux savoir c'est quelles solutions parmi les suivants :
Solution #1 :
J'utilise la lois des gaz parfais, donc je fais : 101,3 x V= 3x (8,314 kPa x L / mol x K ) x (273 + 25), ce qui me donne 8,82L de volume pour le CO2.
Ou solution # 2:
1- Je fais un produit croisé pour trouver le nombre de mole pour 50g de propane : 50g x 1 mol / 20,01g (masse molaire de propane) . Ce qui me donne 2,5 mol de propane. On sait que 1 mol de propane donne 3 moles de CO2, donc 2,5mol de propane x 3 = 7,5 mol. Ensuite, on fait la loi des gaz parfait donc: 101,3 x V= 7,5x (8,314 kPa x L /mol x K) x 298, donc Volume de CO2 = 183,43 L?
Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Mise en contexte: J'utilise un réchaud au propane (C3H8). La combustion produit: CO² et de l'eau. On utilise 50g de propane et le volume molaire de 24,5L (condition ambiante: 25 degré et 101 kPa.)
On veut connaitre:
Le volume de dioxyde de carbone produit?
Que devient le volume du CO2 si la température est maintenant de 100 degrés et pression normale?
Je ne comprend pas le chemin à prendre considérant le peu d'infos.
Merci !
-
Vérifiée par Alloprof
Postsecondaire • 3aJe ne comprends pas les questions b) et c), s’il vous plaît pouvez vous m’aider.
-
Vérifiée par Alloprof
Secondaire 4 • 3aJe ne comprends pas comment calculer C1V1=C2V2
-
Vérifiée par Alloprof
Secondaire 5 • 3ajai une questions en chimie.
"seules les reactions endothermiques spontanees necessitent de lenergie pour briser les liaisons des reactifs et former de nouvelles liasons"
ceci est vrai ou faux?? si cest faux, expliquez pour quoi
merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Quelqu'un pourrait m'expliquer ce qu'est le recrutement de cellules inflammatoires? Dans cette phrase la par ex:
Les corticoïdes inhalés agissent au niveau de différents paramètres de l’inflammation, notamment l’inhibition du recrutement de cellules inflammatoires
Merci!