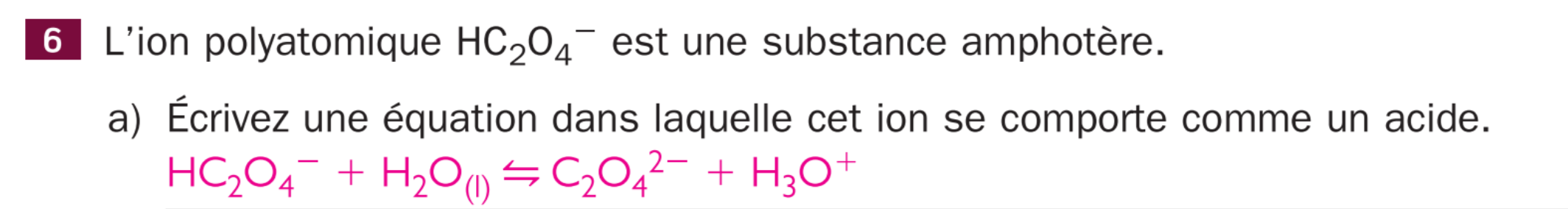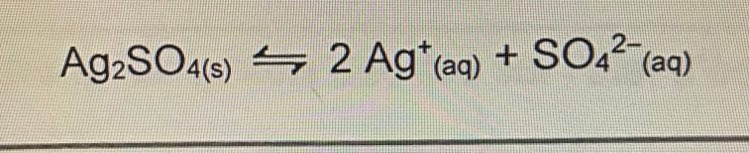Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, j'aimerais savoir comment déduire l'équation chimique d'une réaction. Par exemple, une question nécessite que je trouve l'équation chimique de la combustion du C4H10. Il me demande par la suite de trouver le volume de 02 impliqué. Je sais donc que le C4H10 réagit avec l'02 pour former un ou des gaz inconnu. Comment aurais-je pu trouver la reaction entière sans faire de recherche sur internet ? Mon problème n'est pas de balancer l'équation, seulement de trouver les produits ou les réactifs manquant à partir d'une mise en situation. Pouriez-vous m'expliquer et me dire s'il y aurais un tableau ou une règle à connaitre ?
Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour voici ma question
-
Vérifiée par Alloprof
Secondaire 5 • 3acomment trouver la pression partielle à partir d'un volume de gaz recueilli et d'une équation. On sait que la réaction se produit à 101,3kpa
-
Vérifiée par Alloprof
Secondaire 5 • 3aJe ne sais pas quoi faire
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je n'arrive pas à résoudre ce problème.
Le « lait de magnésie » est une solution saturée de Mg(OH)2(s). Sachant que la constante de produit de solubilité (Kps) est de 5,61 x 10-12, quel est le pH de 15 mL du « lait de magnésie » ?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, comment trouver la chaleur molaire de neutralisation des substances suivantes? NaOH et KOH... Pour un laboratoire et les manipulations ont permis de trouver un delta T de 4,5 degrés (on mélangait 50,0ml de HCl avec une base de 50,0 ml) 1,0 mol/L chacun
merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
je ne comprends pas comment faire ce numéro.
-
Vérifiée par Alloprof
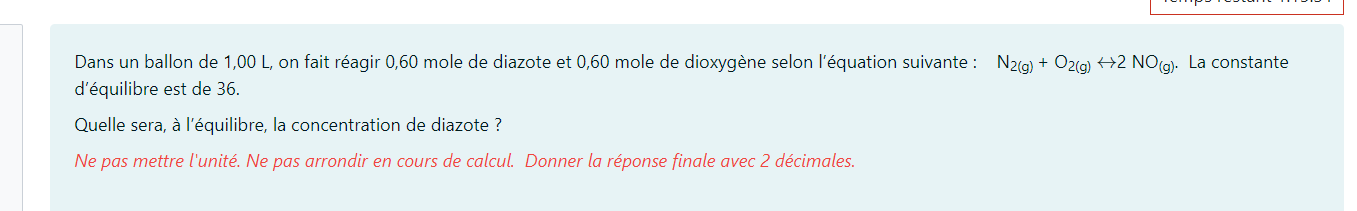
Secondaire 5 • 3aVoici une question dans un test de révision en chimie:Puisque j'ai la constante d'équilibre, je croyais calculer la concentration requise de NO, mais ce n'est pas ce que la question demande. Ils veulent savoir la concentration de diazote à l'équilibre. Moi, je croyais que j'avais déjà le nombre de moles à l'équilibre de diazote (0,60). Donc, j'ai fait selon la formule c=n/v (0,60/1,00) ce qui donne 0,60. Mais, ce n'est pas la bonne réponse.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,est ce que c'est correct si j'ai mis HC204- flèche C2O42-^+ H^+ ? C'est la même chose ?
-
Vérifiée par Alloprof
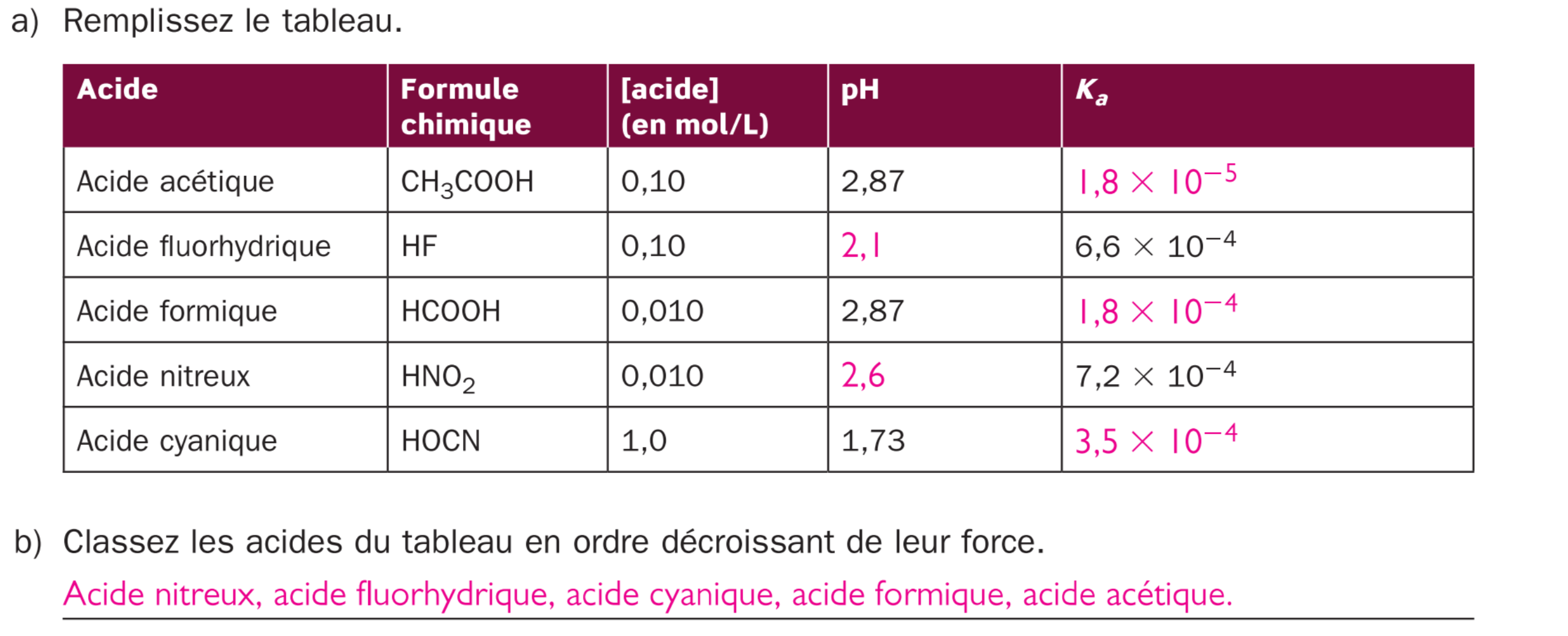
Secondaire 5 • 3aBonjour,
je n'ai pas compris comment on détermine les acides en ordre décroissant de leur force..
On regarde les concentrations ou le pH?
Merci,
-
Vérifiée par Alloprof
Secondaire 5 • 3aSi la masse molaire du gaz X est 16 fois plus petite que celle du gaz. Y, combien de temps faudra-t-il au gaz X, par rapport au gaz Y, pour diffuser, si les deux gaz sont soumis aux mêmes conditions de température et de pression?
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour, je suis bloqué sur cette question et je ne trouve pas les lois pour y répondre.
-pour une pression et un nombre de moles constants, comment réagira le volume si la température kelvin double?
-
Vérifiée par Alloprof
Secondaire 5 • 3aÀ TPN. on introduit 0,050 L d'hélium (He) et 0,075 L de dioxygène (O.) dans un contenant de 150 mL. Quelle est la pression partielle de l'hélium?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour encore!
je me demandais ici pourquoi l’énoncé a) n’était pas inclus dans la réponse car une diminution de température favorise la réaction directe non?
merci en avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir!
je ne comprends pas trop pourquoi la réponse est b à ce numéro. Pouvez-vous me l’expliquer?
merci en avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3aje n'arrive pas a faire celle ci aussi
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour je n'arrive pas à trouver la réponse de cet exercise
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjours à vous. Je me prépare présentement pour un examen de chimie qui comporte les chapitres liés à l'étude quantitative de l'état d'équilibre. Dans un numéro sur le pH, on dit que l'on dissout 0,02 g de Ca(OH)2 dans 12 L d'eau et de déterminer le pH. Ainsi, j'ai calculé le nombre de moles de Ca(OH)2 et cela m'a donné 2,7 X 10-4 mol, et sa concentration, soit 2,2 X 10-5 mol/L. Puisque c'est une base forte, on peut en conclure qu'il se dissout complètement. Mais là vient le problème. Dans le corrigé du cahier, on dit que la concentration en ions OH- est aussi 2,2 X10-5 mol/L. Or, l'équation de dissolution est Ca(OH)2 --) Ca2+ + 2 OH-. Sa concentration ne devrait-elle pas être le double de celle du Ca(OH)2?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour. Pourriez-vous m'expliquer comment trouver la solubilité en g/L du Ag2SO4, avec pour seule information que le Kps est de 1,4 fois 10-5.Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 3aRebonjour Alloprof,
Pour ce numéro je suis un peu perdue, j'ai essayer d'utiliser la formule n=m/M et la formule V/T = V/T. Sauf que ça n'a pas fonctionné.
Merci d'avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
J’ai de la difficulté à identifier le catalyseur dans une équation chimique. Par exemple, pour cet exercice, je ne comprends pas pourquoi c’est le dibrome. Pouvez-vous me donner un truc ou m’expliquer comment déterminer cela?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour Alloprof, j'avoue que je ne sais pas du tout comment m'y prendre avec cet exercices, je ne sais même pas par où commencer. Si quelqu'un peux m'éclairer j'en serais très reconnaissante, merci!
-
Vérifiée par Alloprof
Primaire 5 • 3aPourquoi le savon à vaisselle est-il un liquide et pourquoi la fumée est-il un gaz ?
Merci,
JupiterAdmirable1839
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
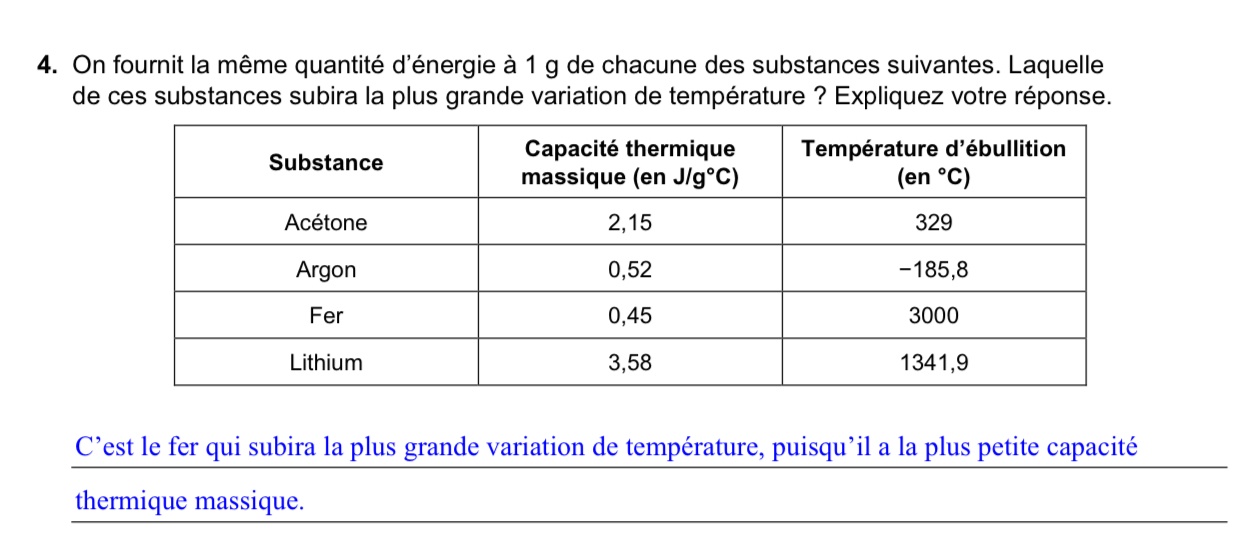
Je crois que cette partie de matière est loin dans ma tête. Je ne comprends pas pourquoi le fer est celui qui subira la plus grande variation de température.
merci en avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir!
je ne comprenais pas ce numéro. Pouvez-vous me l’expliquer s’il vous plaît? J’avais à la base mis le c, mais je ne comprends pas pourquoi ce n’est pas bon.
merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aQuelle est le nombre de liaisons convalentes de H2?
-
Vérifiée par Alloprof
Secondaire 5 • 3aEst-ce que quand K=1 la réaction est complète?
-
Vérifiée par Alloprof
Secondaire 1 • 3aSalut!
j’ai un examen demain en science et je ne sais pas comment faire un protocole pour la dissolution. J’ai regarder partout et vous êtes ma dernière chance. Je ne sais vraiment pas quoi faire alors j’ai penser à vous.
Merci au personnes qui me répondent. C’est très gentil de prendre de votre temps.
LoupArtistique6741
-
Vérifiée par Alloprof
Secondaire 5 • 3aQuelqu'un peut m'expliquer le fonctionnement d'un manomètre en U?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSalut!
J'ai un examen laboratoire demain en chimie! Y'a-t-il des principes de labo qu'il faut que vous me recommander à connaitre?
Je devrai faire une marche à suivre seulement à partir d'une mise en situation, mais j'ai de la difficulté que faire ?
Merci