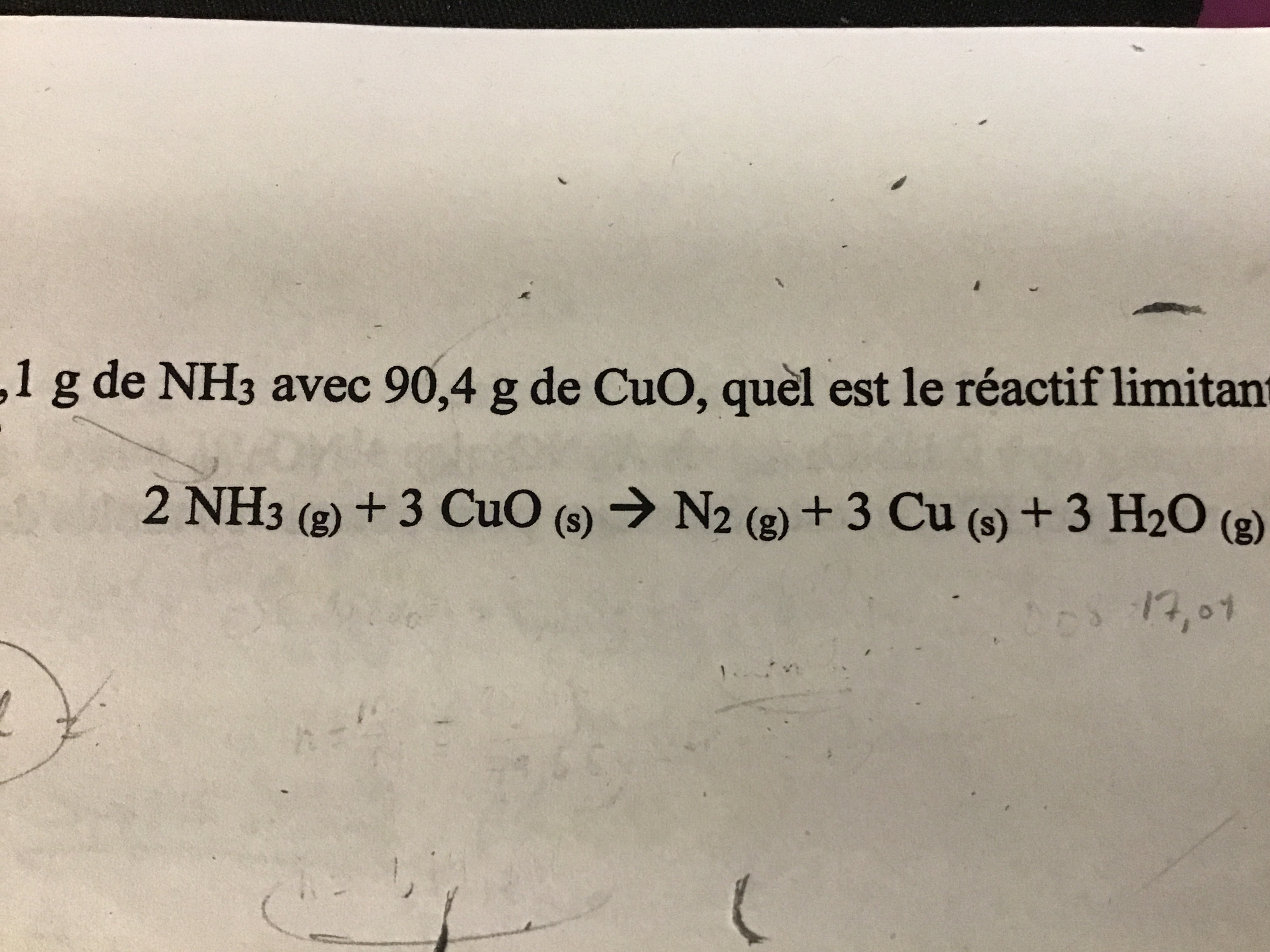Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aJ essaie de balancer des equations
-
Vérifiée par Alloprof
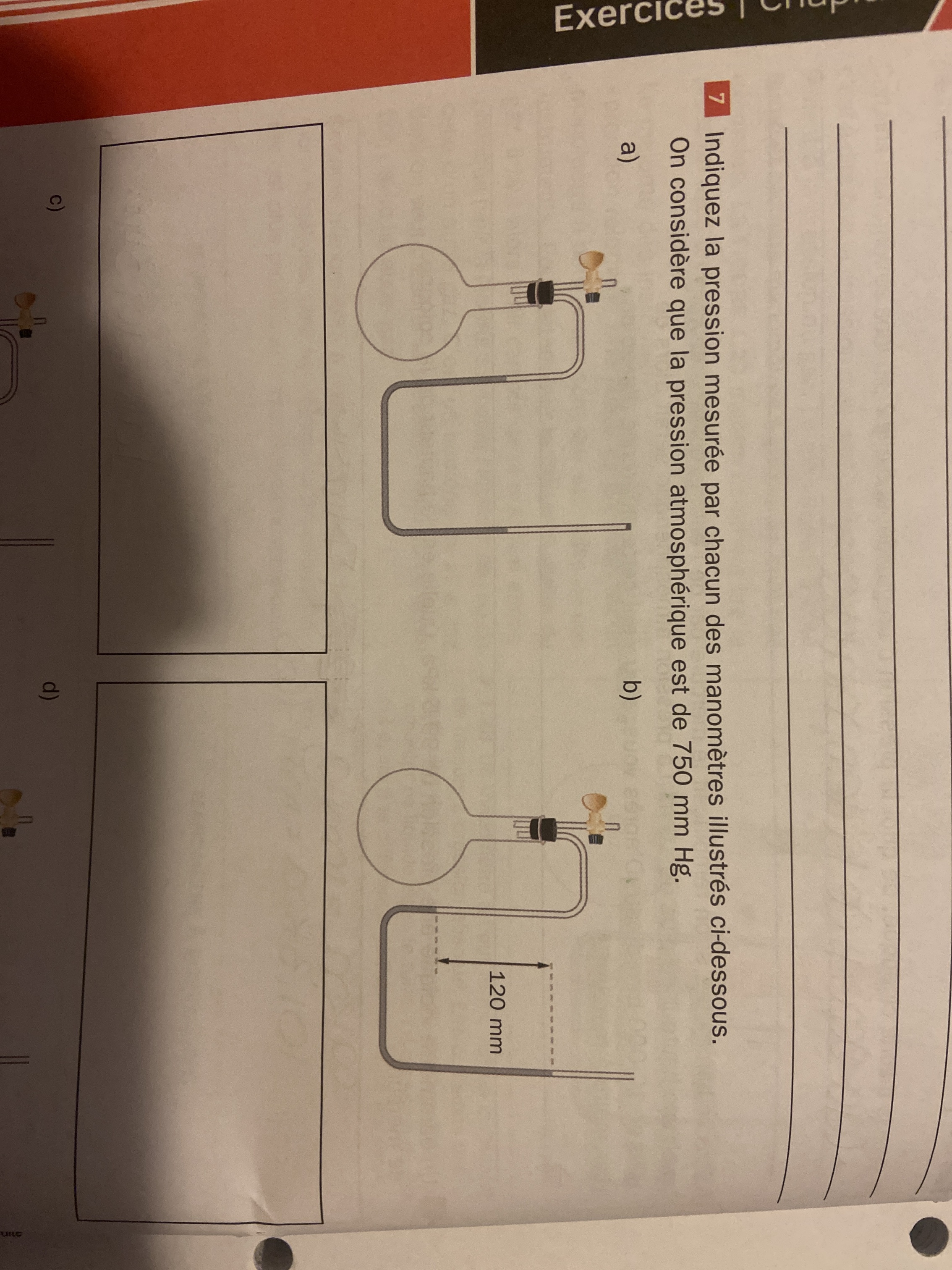
Secondaire 5 • 3aBonjour si quelqu’un pourrait m’expliquer ce numero cela m’aiderait beacoup!
-
Vérifiée par Alloprof
Secondaire 4 • 3aQuelle est la différence entre les formule de la notion de mole: n:Np/NA
et M;m/n??
-
Vérifiée par Alloprof
Secondaire 5 • 3aPourquoi un aérosol n'est une changement de phrase?
C'est quoi la différence entre aerosol et le gaz?
-
Vérifiée par Alloprof
Secondaire 1 • 3aBonjour! je me demandais auriez vous des trucs pour que la mémorisation des noms et des fonctions des cellules animales et végétales soient plus simple?! Merci :D!!
-
Vérifiée par Alloprof
Secondaire 5 • 3aPourquoi l’incertitude absolue de la règle est 0,05 et non 0,5?
-
Vérifiée par Alloprof
Secondaire 5 • 3aComment trouver l’incertitude absolue d’un cylindre gradué de 10mL?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour , j’ai mon examen demain et j’ai beaucoup de difficulté a comprendre , est ce que vous pouvez m’aider? Merci
-
Vérifiée par Alloprof
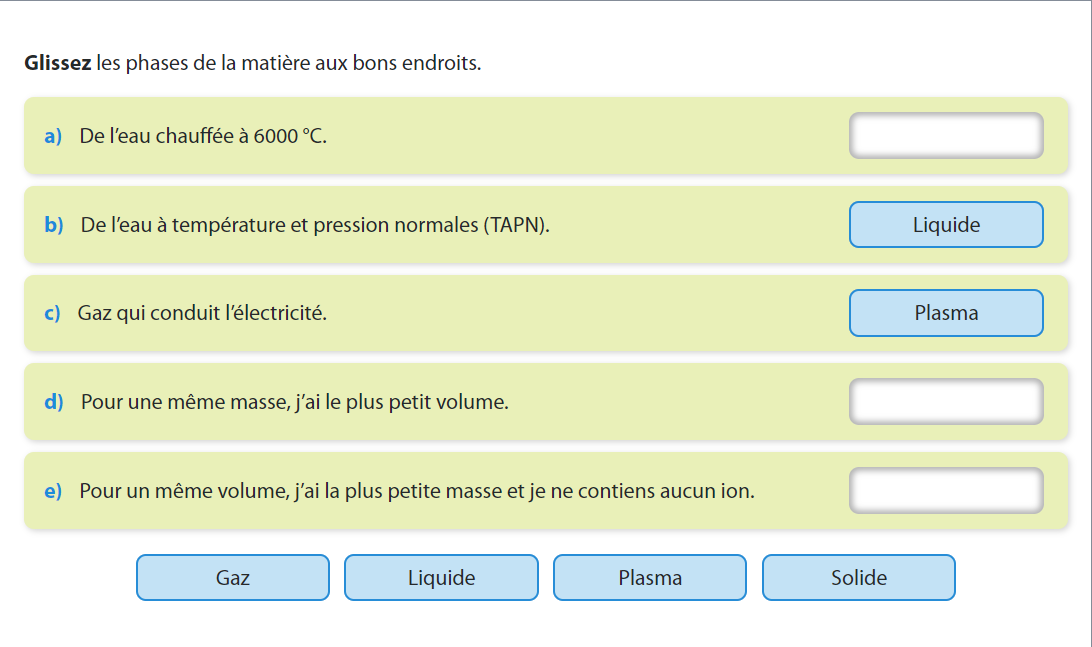
Secondaire 5 • 3aBonjour !
Je suis bloquée à cet exercice...
Et j'aurais besoin d'une réponse rapidement si c'est possible.
Pour le a), je pense que c'est soit un gaz ou du plasma.
Et les 2 derniers m'embêtent, je serais portée à mettre solide pour le d) et gazeux pour le e).
Pouvez-vous m'aider ?Merci de votre aide !
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, comment je dois faire pour trouver le réactif limitant dans des calculs de proportions. Quelle est la démarche des proportions?
-
Vérifiée par Alloprof
Secondaire 5 • 3aC6H12O6 (s) + 6O2 (g) ---/ 6CO2 (g) + 6H2O (s)
on dispose de 5g de glucose et autant de O2 nécessaire pour consommer tout le sucre.
a) calculer la masse d'eau formée.
b) calculer la quantité de matière de CO2 formée.
merci, beaucoup.
-
Vérifiée par Alloprof
Secondaire 5 • 3asalut je sais qu'il fait tard mais je suis vraiment désespérée avec mon devoir
ma question est:
dans 13,478g de propanol (C3H8O), combien y a-t-il de moles d'hydrogène?
-
Vérifiée par Alloprof
Secondaire 4 • 3aCombien d’atomes de H y a-t-il dans 5,30 g de H2O?
J’ai la réponse du corrigé qui est de : 3,54 x 10^(23 atomes de H. Je n’arrive juste pas à la bonne démarche. Merci!
-
Vérifiée par Alloprof
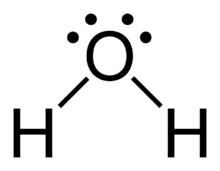
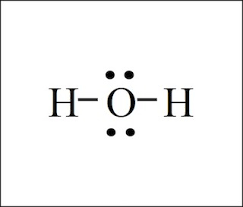
Secondaire 5 • 3aComment est ce qu'on dessine la structure de Lewis pour l'eau H2O ? Est ce que les doublets non-liants sont en haut comme ceci?Où bien de chaque extrémité comme celaDonc je crois la structure est plus linéaire et n'a pas d'angle.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!!
J'avais une question à propos des chiffres significatifs. Je pratique présentement des exercices de chimie comprenant plusieurs étapes de calculs à effectuer. Est-ce que je dois arrondir aux bons chiffres significatifs à chaque calcul? Ou est-ce que je dois tenir en compte des chiffres significatifs seulement au tout dernier calcul?
Merciii
-
Vérifiée par Alloprof
Secondaire 5 • 3apourquoi l'Ozone a une grande réactivité?
quel lien a-t-il avec le nombre de liaison qu'il fait?
-
Vérifiée par Alloprof
Secondaire 5 • 3aCest quoi un echelle atomique?
Et dans mon cahier de chimie
Il est écrit que à l'échelle atomique, les gaz ne subissent pas au force gravitationnelle
Par contre plus on monte haut , il manque d'aire (à cause de gravité ? )
Pouvez vous m'expliquer?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aEst-ce que quelqu’un peut m’expliquer comment trouver le réactif limitant et le réactif en excès en démarche plus détaillée, car j’ai de la difficulté par rapport aux calculs de proportions stœchiométriques pour les trouver, il y a trop de moles, ce qui me mélange.
Voici le problème: « Si on fait réagir 18,1g de NH3 avec 90,4g de CuO, quel est le réactif limitant? Quelle est la masse du composé en excès? »
merci beaucoup
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Pourriez-vous m'expliquer pourquoi si on augmente le gradient de concentration, la vitesse de diffusion augmente ?
Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Quelles sont les différences entre la diffusion et l'osmose ?
Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, j'ai une évaluation bientôt, et j'ai fait cet exercice de révision, mais je voulais m'assurer d'avoir les bonnes réponses. Pourriez-vous me donner les réponses à ces questions pour que je puisse me corriger ? Merci !
-
Vérifiée par Alloprof
Secondaire 4 • 3aQuel sont 3 choses je peux comparer les métaux et les métaux de transition avec?
J'ai déjà comparer avec les charges ioniques mais je ne sais pas d'autre choses je peux les comparer avec.
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour,
quelle est la loi simple des gaz qui entre en jeux lorquon gonfle un ballon de soccer?
-
Vérifiée par Alloprof
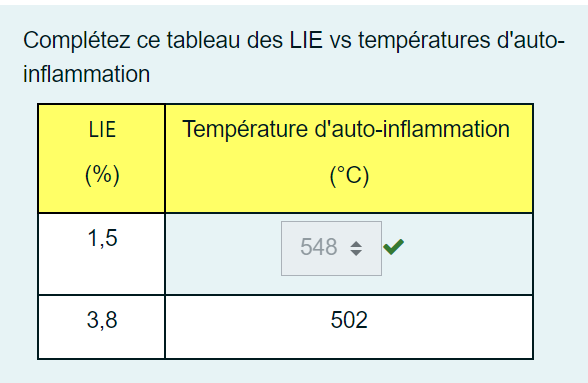
Postsecondaire • 3aBonjour, j'essaie de comprendre pourquoi lorsque la Limite inférieure d'explosivité d'une substance combustible augmente, sa température d'auto-inflammation diminue. La limite n'augmente que si la température ambiante diminue ou encore lorsque la concentration en oxygène de la pièce diminue. Mais cela n'explique pas la variation de la température d'auto-inflammation.
merci
-
Vérifiée par Alloprof
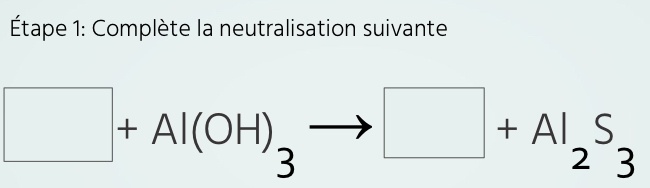
Secondaire 4 • 3aJe ne comprend pas comment faire ce genre de numéro. Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 3aC'est quoi la définition du centre de masse en chimie?
-
Vérifiée par Alloprof
Secondaire 5 • 3aPourquoi donc ? Je comprends que lorsque la masse est élevé, la vitesse est moindre, mais, la formule de l'énergie cinétique est "E=0,5mv^2" donc je n'arrive pas à comprendre comment l'énergie cinétique est toujours constant (peu importe le gaz) en se fiant seulement à la masse et à la vitesse s'il y a une multiplication de 0,5x au tout et qu'il y a un exposant 2 pour la vitesse 😅
-
Vérifiée par Alloprof
Primaire 4 • 3aallo alloproff je voudrais savoire....... comment les tornade se forme?
-
Vérifiée par Alloprof
Primaire 4 • 3aAllô Allôprof. Je me demandait....... Pourquoi quand il'ya du soleil avec un ciel bleu et de la pluie un GRAND arc-en-ciel apparaît ?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
le volume et la quantité de matière ont t’ils un impact du l’énergie cinétique d’un gaz?
Merci!