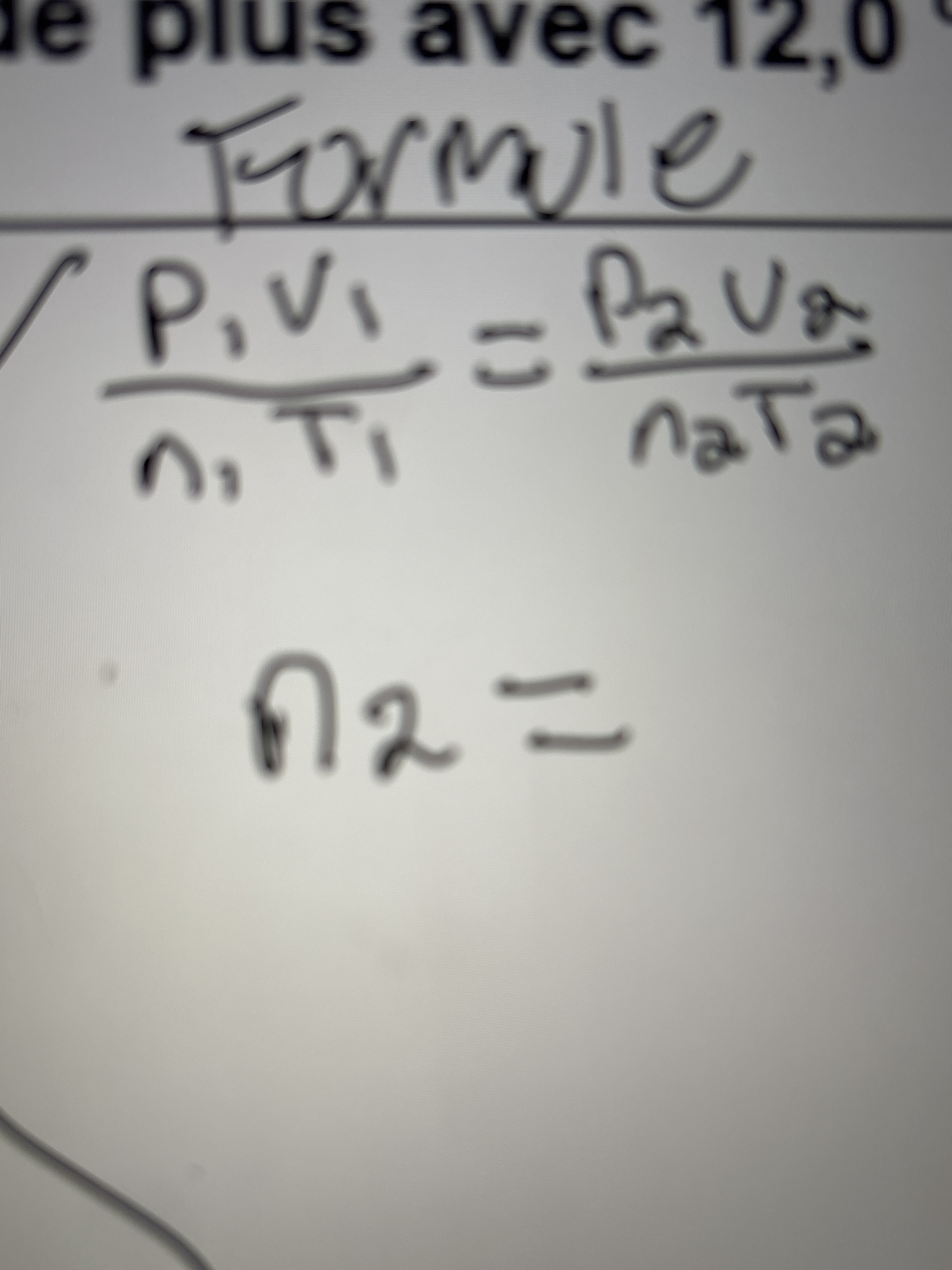Liste de discussions
-
Secondaire 5 • 3m
Bonsoir, sauriez-vous l'incertitude d'une seringue de gaz de 10ml? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, je ne comprends pas pourquoi l'enthalpie augmente malgré le fait que ce soit exothermique. De l'énergie est dégagé dans l'extérieur alors pourquoi l'enthalpie augmente. Merci!
-
Vérifiée par Alloprof
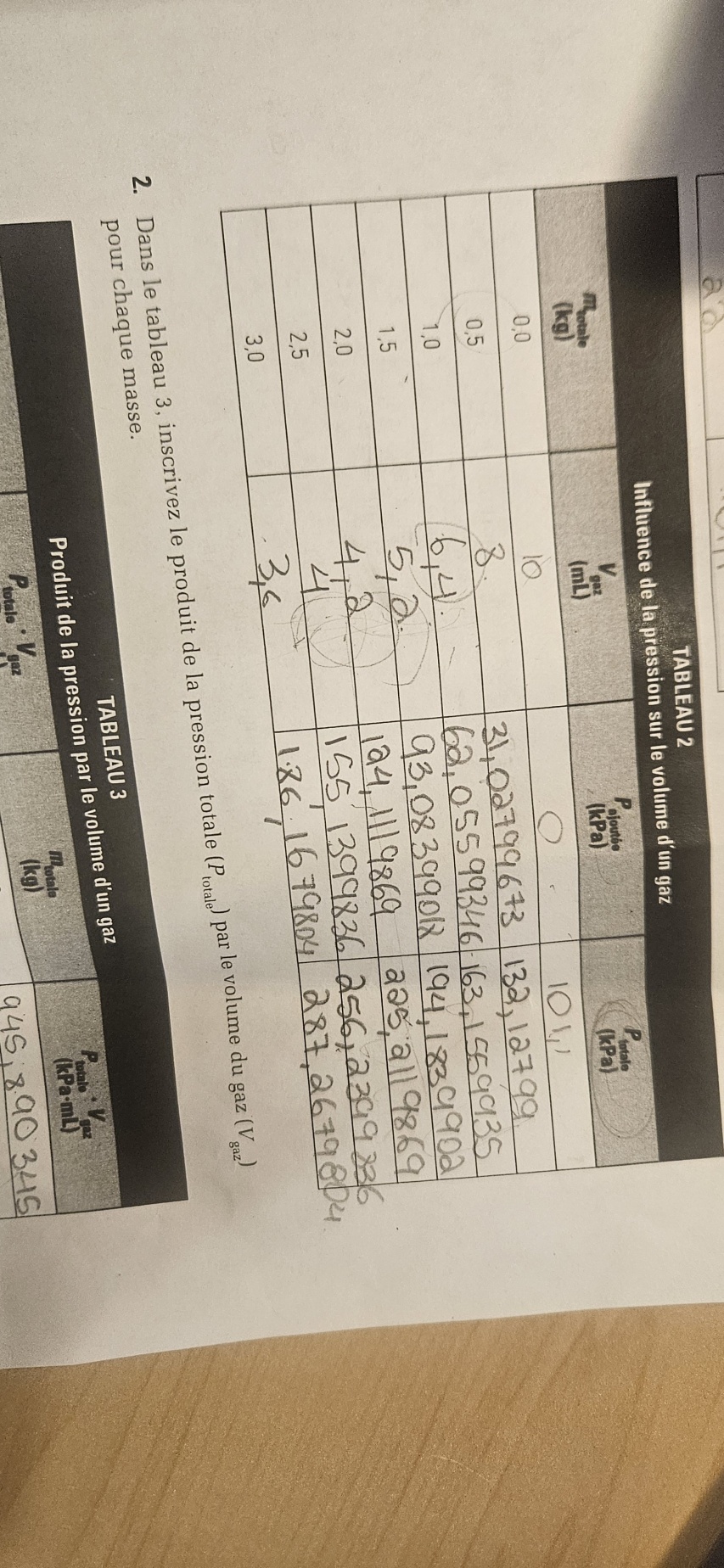
Secondaire 5 • 3mBonsoir! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/113534/questionEn soit, l'expérience consitait à déterminer la relation entre le P et le V d'un gaz. Pour ce faire, nous avions une seringue accrocher sur un support universel auquel nous ajoutions petit à petite des poids à fin de faire abaisser le piston.
...
Ainsi, je ne comprend pas pourquoi ne pas avoir directement utiliser le Pajouté...pourquoi faire +Patm?
Et également, pourquoi utiliser la valeur de la somme dans la formule pour trouver la constante (Ptotal * Vgaz) ?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonsoir! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/113440/questionPourrions-nous trouver la masse des deux gaz (l'inconnu et le N2). Puis ensuite, avec la masse du N2 trouver la son nombre de mol (M=n/m)
...
Et avec cela, selon le principle d'avogadro qui stipule la les volumes égaux de gaz différent comporte le même nombre de mol, nous pourrions utiliser le nombre de mol de N2 et isolé M avec la masse trouver dans la seringue?
Est-ce que cela serait une bonne technique pour identifier le gaz inconnu? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3mRe-bonjour!
...
1)Que veut dire le bilan énergétique et comment est-ce que cela peut influencer la réactivité chimique d'une substance?Pouvez-vous m'aider à le comprendre avec des exemples un peu en détails?
2) Que veut dire une combustion incomplète? En quoi est-ce qu'elle est exactement difféente de la combustion complète? Prenons un exemple qui me mÉlange: la combustion du méthane CH4.En fait, ce qui me mélange, c'est que la combustion par définition implique comme produits le dioxyde de carbone et l'eau. Comment cela se fait-il que le même élément lors une combustion complète produit du CO2 et H2O, alors que lorsque c'est incomplète, le CO monoxyde de carbone s'ajoute dans les produits?D'où sort cette substance pour la combustion d'un même élément?
3) Commentest-ce que les gaz nobles sont utilisés dans la soudure à l'arcet en comment servent-ils à ces types d'applications?
4)Commentest-ce que les gaz nobles créent un milieu inerteet en comment est-ce qu'elles sont utilisés à des fins deconservation par exemple?Merci infiniment :D
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour!
...
1)Pourquoi dans une même famille, malgré le fait que chacun des atomes qui ont le même nombre d'électrons de valence, ont une réactivité différente?Par exemple, si je prends les halogènes, tous les éléments de cette famille ont besoin d'arracher 1 électron pour compléter leurs couches.Alors, pourquoi le Fluor est beaucoup plus réactif que le Chlore? Pourquoi la réactivité dans une famille augmente du bas vers le haut?2) Pour la famille des alcalins, mon profa dit que plus on ajoute des couches électroniques pour les alcalins, plus elle est réactive. Je ne comprends pas.Cela est aussi un peumélangeant,puisque la référance utilisée dans mon cahier montre une flèche qui va du bas vers le haut pour illustrer l'augmentation de la réactivité.3) Est-ce que l'électronégativité est juste une force d'attraction qu'exercent les protons sur les électrons de son propre atome ou bien c'est vraiment l'attraction exercée par l'élément en question sur ses atomes voisins pour former une liasion?Parce que dans ma tête, je vois l'électronégativité plus comme une force d'attraction qui rentre en jeu dans la formation des liaisons entre différents éléments. Aidez-moi svp à distinguer ces deux contextes.Merci beaucoup pour apporter les clarifications.
Ça va vraiment m'aider :D
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour je n’arrive pas à faire la question. Pouvez vous m’aider svp? Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour quelqu’un pourrait m’expliquer comment on peut déterminer si une reaction est reversible ou irréversible avec seulement L’équation? Aussi avec le diagramme énergétique sil vous plait. Je n’arrive pas a faire cet exercice car je ne comprend pas
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour! Pourquoi est-il nécessaire d'ajouter la pression atmosphérique?
...
-
Vérifiée par Alloprof
Postsecondaire • 3mBonjour,
...
Je suis également mitigée, car si il y a une éraflure sur la pièce et qu'une petite partie du zinc part, le fer n'est pas sensé oxyder tant que tout reste dans le même environnement. Pourquoi? Est-ce que le zinc réagit avant que le fer puisse réagir avec l'oxygène dans l'eau? (C'est justement cela qui me fait douter par rapport au fait que la couche de valence du fer est peu être complète grâce à une autre réaction....) merci de m'aider!!
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, je sais que nous ne pouvons pas mesurer l'enthalpie d'une substance expérimentalement, mais nous pouvons mesurer sa variation d'enthalpie lors d'une transformation. Pour trouver cela, nous soustrayons l'enthalpie des produits moins l'enthalpie des réactifs. Cela dit, comment savons nous quelle est l'enthalpie des produit et des réactifs si il est impossible de la mesurer. Je ne comprends pas comment nous mesurons l'enthalpie des produits et des réactifs, avez-vous des exemples. De plus, il est stipulé dans notre cahier que l'énergie mécanique est constitué de l'énergie cinétique et potentielle. L'enthalpie, elle, est la somme de l'énergie cinétique et potentielle. Je ne comprends pas la différence entre les deux. Aussi, est-ce que l'enthalpie contient toute les autres formes d'énergies (ex. électrique, nucléaire, chimique, thermique, rayonnante)? Bref, pouvez-vous m'éclairer sur ces points? Merci et bonne journée!
-
Vérifiée par Alloprof
Secondaire 5 • 3mrebonjour, Merci beaucoup pour vos dernières explications, j'ai compris!!
-
Vérifiée par Alloprof
Secondaire 5 • 3mQuelle est la valeur théorique du nombre de moles du H2 en remplissant toutes les informations utiles dans le tableau
-
Vérifiée par Alloprof
Secondaire 5 • 3mrebonjour, merci pour votre explication!!! Il ya encore une autre petite chose que je n'arrive pas à comprendre en lien avec le même problème, je ne comprend pas pourquoi ses juste le H2 qui libère 536,6 KJ parce que dans le corriger de l'exercice on disait que 1 mole de H2 dégageait 536,6 Kj Merci à l'avance
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, j'espère que vous allez bien, dans votre exercice je ne comprend pas pourquoi ses le H2 qui libère 536,6KJ quand ses le delta H et donc ce n'est pas supposer être l'énergie qui est libéré du H2 et F2 en même temps. De plus, je ne comprend pas pourquoi qu'on met le delta H dans le côté des réactif si ses le H2 et F2 qui libère, je ne comprend pas pourquoi on ne le met pas du côté des réactif. De plus je ne comprend pas pourquoi on met le delta H dans la formule, ses pas supposer être l'enthalpie des réactifs. Merci à l'avance
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, dans ce numéro, je ne comprend pas pourquoi ses le NO2 qui absorbe 66,4 KJ quand ses une réaction endothermique et pour l'exothermique je ne comprend pas pourquoi le 483,6 KJ n'est pas du côté des réactifs car ses le H2 et le O2 qui dégage de L'énergie ??Pouvez-vous m'aider svp?? Merci à l'avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, j'ai encore une petite question, lors d'une réaction endothermique, est-ce que c'est les réactif qui absorbent de l'énergie ou c'est les produits?? Merci à l'avance!!
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, j'espère que vous allez bien, je n'arrive pas a comprendre ce graphique donc ses quoi le delta H et qu'est-ce que celui-ci signifie dans ce graphique. De plus, je ne comprend pas pourquoi la corde bleu est endo et la rouge exo. Pouvez-vous m'aider svp?? Merci à l'avance!!
-
Vérifiée par Alloprof
Postsecondaire • 3mBonjour,
...
J’ai vraiment besoin d’aide svp.
Merci beaucoup.
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, j'espère que vous allez bien, j'ai de la misère a faire la différence entre l'enthalpie et la variation d'enthalpie, pouvez-vous m'aider svp?? Merci à l'avance !!
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonsoir!J'étais à la recherche d'une technique. Toutefois, je ne comprend sincèrement point l'utilité de l'information « l'étiquette de la bonbone N2 est demeurée intacte»
...
-
Vérifiée par Alloprof
Secondaire 5 • 3mJ’ai un problème dans mon cahier d’activités qui est cela : un récipient de 22,0 L contient 22g de propane à 185 kpa. Quelle est la température de ce gaz en degrés Celsius?
...
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour j’aimerais savoir comment fait-on pour isoler une variable en chimie j’ai oublier
...
-
Vérifiée par Alloprof
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, j'ai un peu de problèmes avec les chiffres significatifs. Par exemple, pour ce calcul dans un laboratoire, quel serait la réponse en tenant compte des chiffres significatifs: n=PV/RT
...
= 0,0057851475657
-
Vérifiée par Alloprof
Secondaire 5 • 3mDans la formule pV=nRT si par exemple on cherche la pression donc p=nRT/V comment on fait pour calculer l’incertitude de la pression. Est-ce comment dans l’image? Et aussi R n’a pas d’incertitude donc on fait comment avec cela?
-
Vérifiée par Alloprof
Secondaire 5 • 3mBonjour, je ne comprends pas pourquoi la température finale ne sera pas égale à 55 celcius. Dans le corriger il est écrit que puisque le c du liquide A est supérieur, il aura une plus petite variation de température. Je comprend que sa température augmente moins avec l'énergie thermique qui lui est donné, mais le liquide B augmentera alors plus. En fait, je ne comprend pas le lien entre le c et la variation de température et surtout pourquoi la température finale ne se situe pas entre les deux température initiale comme il est écrit dans le cahier. Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3mcomment résoudre ce problème: 1- L'équation suivante représente la combustion du méthanol. CH3OH (l) + 3/2 O2 (g) ---> CO2 (g) + 2 H2O (g) À l'aide des trois équations suivantes, calculez la chaleur de réaction de la combustion du méthanol. C (s) + 2 H2 (g) + 1/2 O2 (g) ---> CH3OH (l) delta H = + 638,8 kJ C (s) + O2 (g) ---> CO2 (g) delta H = - 393,5 kJ H2 (g) + 1/2 O2 (g) ---> H2O (g) delta H = - 241,8 kJ
...
svp
-
Vérifiée par Alloprof
Secondaire 5 • 4mJe vois! Merci pour l'explication!:https://www.alloprof.qc.ca/zonedentraide/discussion/113187/questionDu coup, pour trouver l'incertitude du volume moyen, c'était bel et bien correcte de ne pas additionner les incertitudes entres les valeurs? Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 4mBonsoir! En lien avec ceci:https://www.alloprof.qc.ca/zonedentraide/discussion/113185/questionMerci beaucoup pour l'explication :)!
...
Merci!