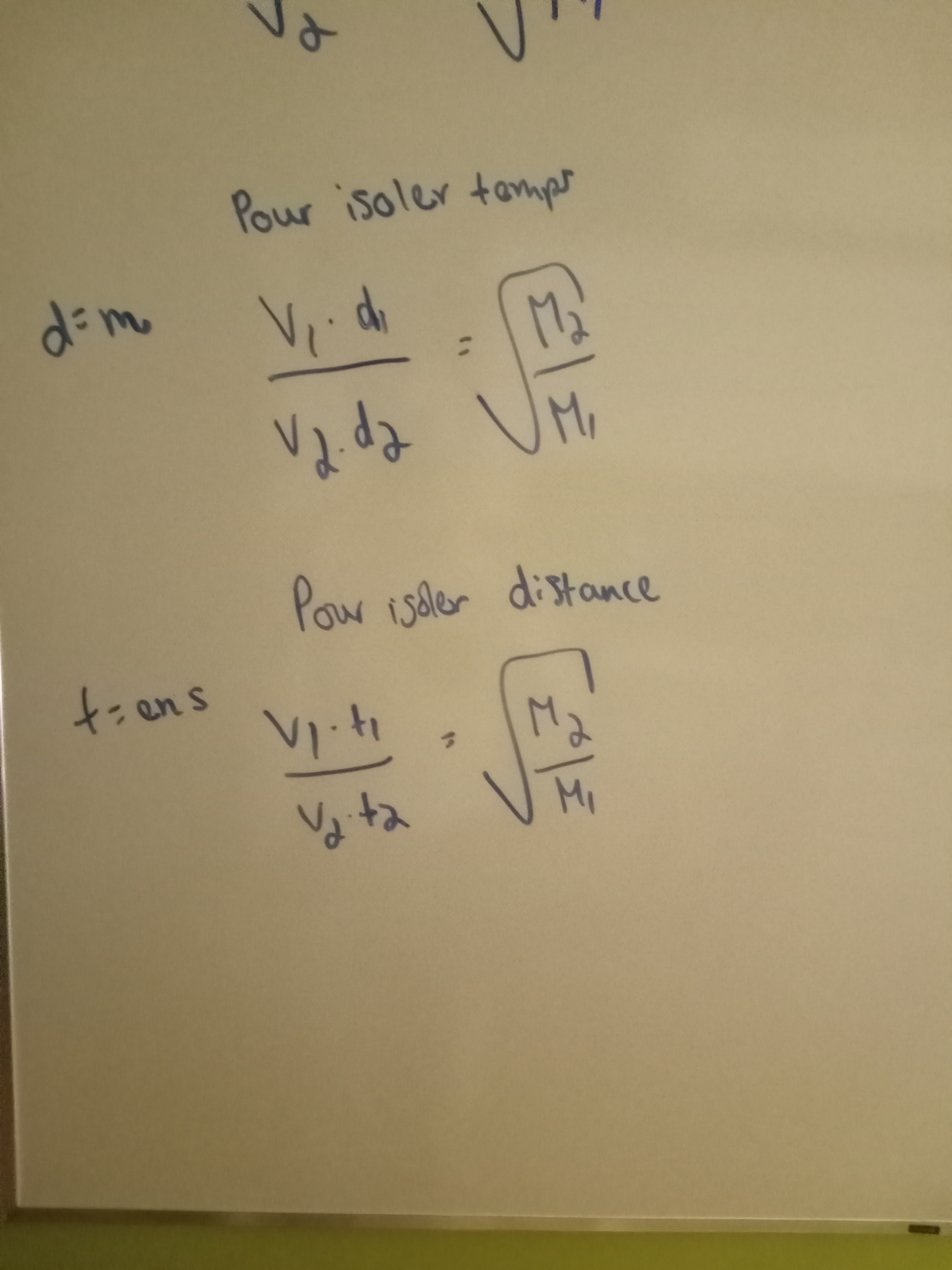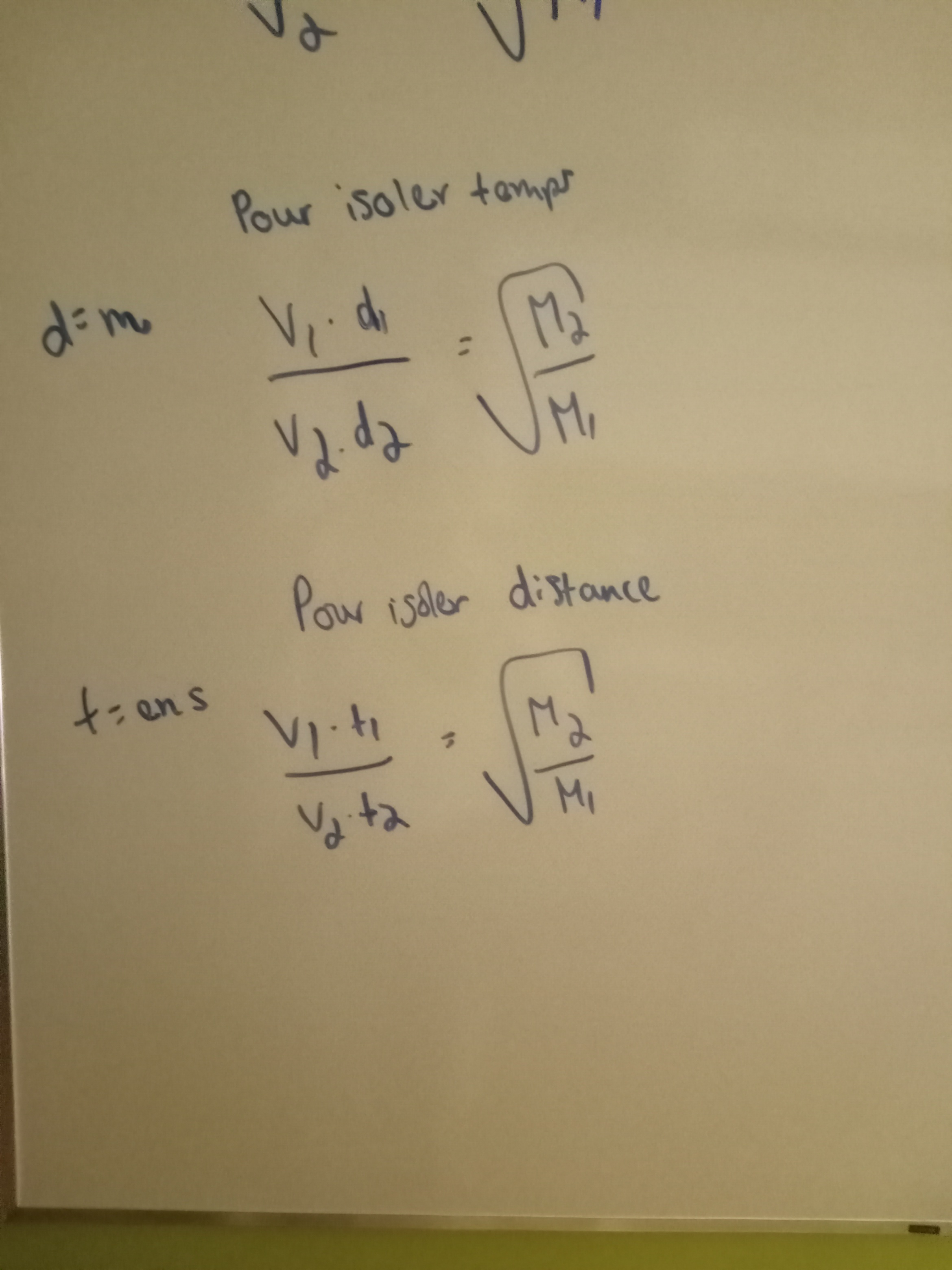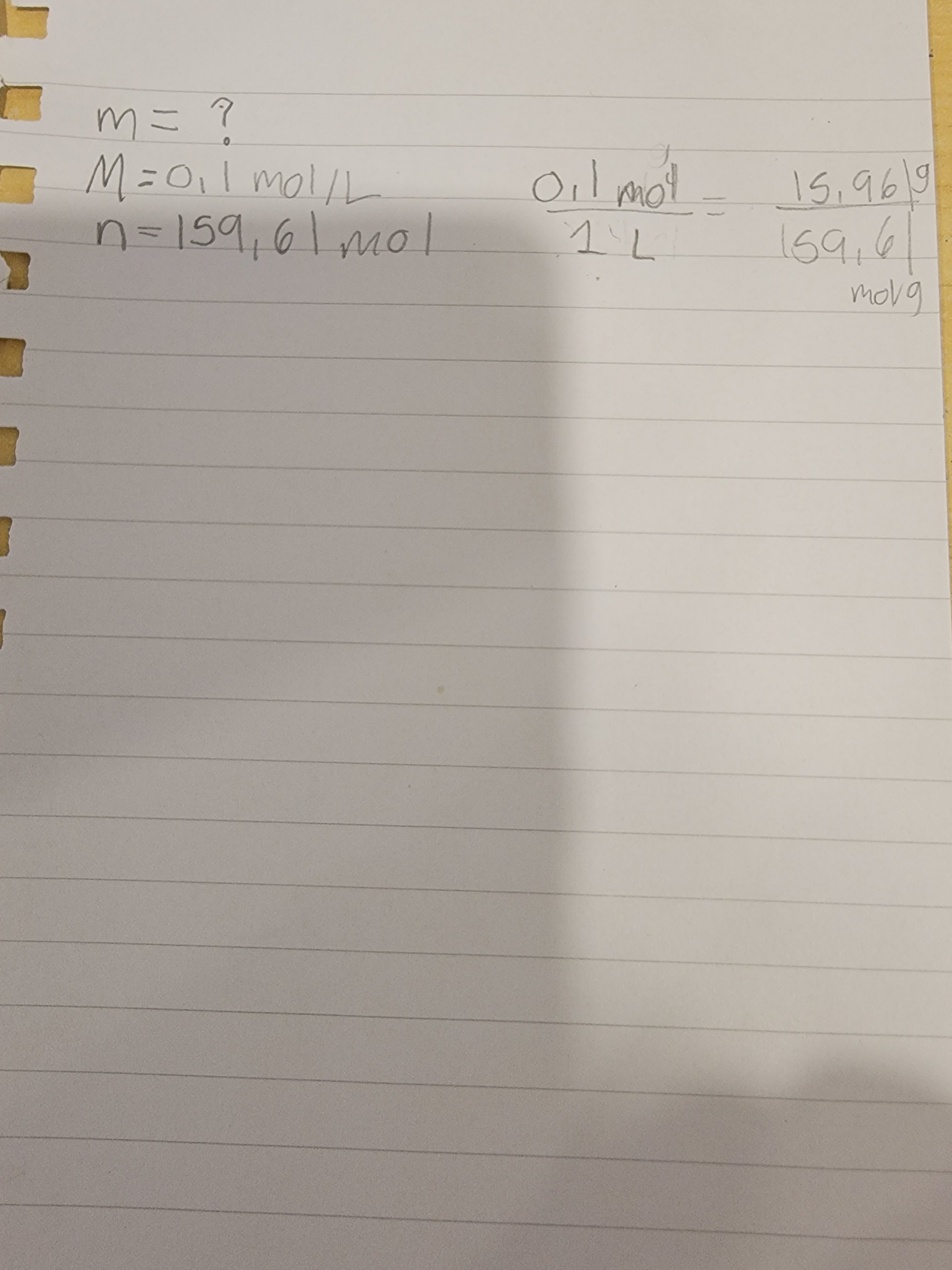Liste de discussions
-
Postsecondaire • 2a
Bonjour,
...
ex :
solution de HCl 37,25% (p/p)
Merci
-
Vérifiée par Alloprof
Postsecondaire • 2aUn liquide a une masse volumique de 5,2 g/mL. Quelle est le volume en kL (kilolitre) d’un échantillon de 95,783 kg ?
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aJe n’arrive pas à résoudre se problème…
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour!
...
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je fais un devoir de stoechiométrie. Il faut calculer le nombre de mol de dichlorure de mercure utilisé si 30,0 g de tétrachlorure d’étain sont produits au cours de cette réaction.
...
Donc, il faut trouver le nombre de mol de HgCl2 mais je ne comprend pas ou est le tétrachlorure dans la formule.
-
Vérifiée par Alloprof
Postsecondaire • 2aBonjour,
...
merci!
ps: ( 1 cm3 = 0,001L et pour le #7 HCl masse molaire =36,458 g/mol)
-
Vérifiée par Alloprof
Secondaire 3 • 2aBonjour,
...
Serait-il possible d'imprimer des images du site, en grande quantité, sachant que je garde sur les images la source grâce au logo d'Alloprof?
Merci d'avance.
-
Vérifiée par Alloprof
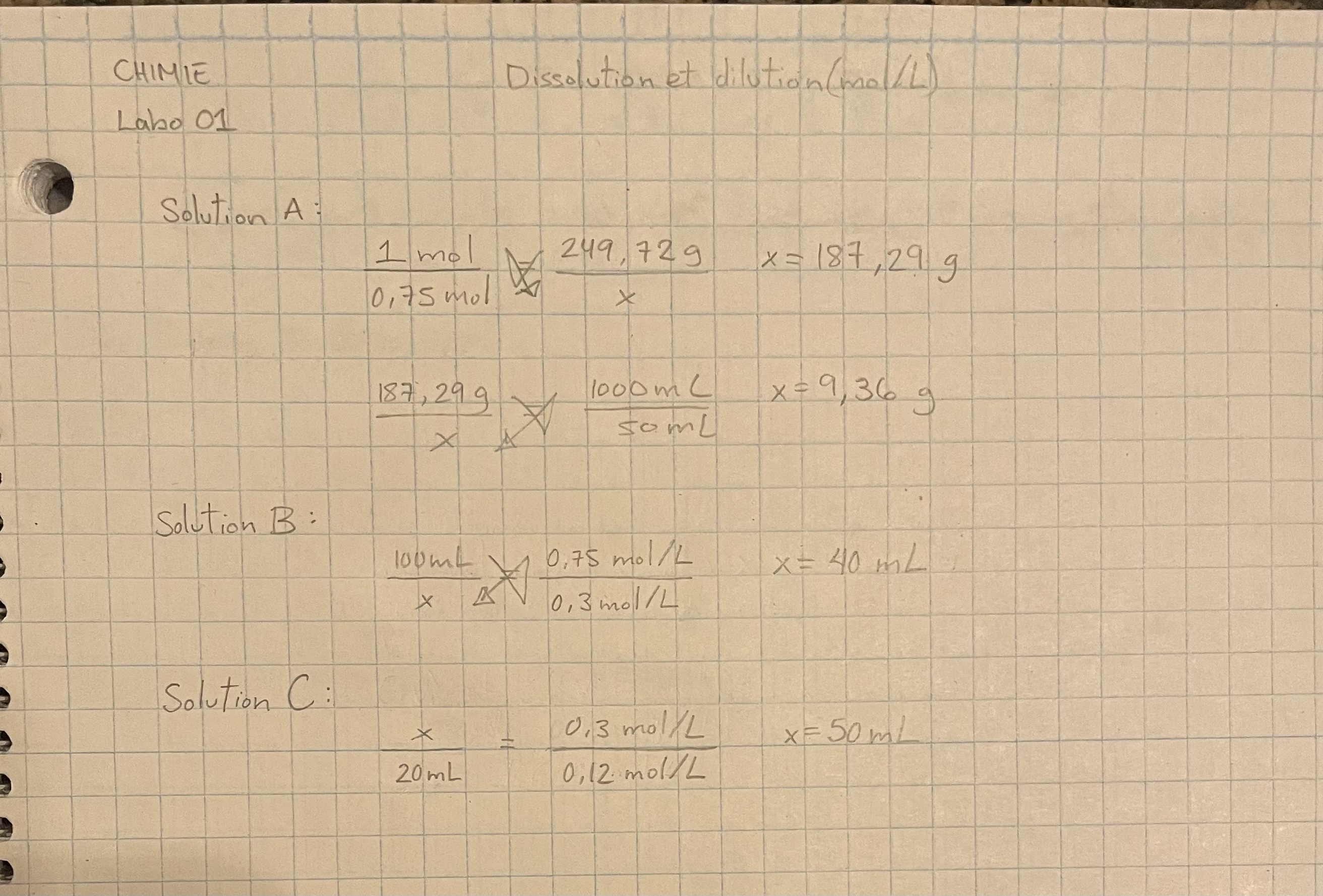
Secondaire 5 • 2abonjour! pouvez-vous vérifier si mes résultats sont bons svp?
...
Pour la solution B: 40 mL
Pour la solution C: 50 mL
Voici les informations…Voici mes démarches…Je ne suis pas sûr si j’ai fait les bons calculs…
Merci beaucoup et bonne soirée!
-
Vérifiée par Alloprof
Secondaire 5 • 2aDans mon labo on dit qu'un convoi compte 40 wagons de 12 m chacun et que la solution de HCL est située à l'une des extrémités du train alors que celle de NH3 se trouve dans le wagon de l'autre l'extrémité. À partir de ces données, je suis supposées être capable de trouver à partir de quel wagon le chlorure d'ammonium est apparu.
...
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je ne comprends pas comment réaliser ces numéros ni vraiment ce qu'ils concernent.
...
Merci d'avance!
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ'ai réessayé à nouveau avec vos conseils pour répondre aux questions 5 et 6 j'ai trouvé ces formules. Sont elles exactesLa première formule est pour le numéro 5 et l'autre pour le 6
-
Vérifiée par Alloprof
Secondaire 5 • 2aPour répondre aux questions 5 et 6 j'ai trouvé ces formules. Sont elles exactes?La première formule correspond à celle pour le numéro 5 et l'autre pour le numéro 6
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment résoudre ces questions?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour je voudrais comprendre pourquoi on utilise 0,12 mol dans le produit croisé à la place de 0,03 mol?
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je me demandais s'il s'agit des bonnes formules pour établir un lien entre le temps et la masse molaire et la distance et la masse molaire.
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour je ne comprend pas comment établir le lien entre la masse molaire et la distance. Je ne comprend aussi pas comment faire le lien entre la masse molaire et le temps.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je me demandais quelles sont les formules qui relient les masses molaires aux temps de diffusion de deux gaz, et ce pour parcourir une même distance. De plus, je me demandais quelle était l'équation qui pourrait relier les masses molaires à la distance parcourue par chacun des gaz, et ce, pour un même temps de diffusion. Je ne comprends aussi pas comment je suis supposée trouver le point de rencontre des deux gaz, qui ont une vitesse différente. Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 2aje l'ai fait comme ça, mais j'ai aycune idée
...
et pouvez vous svp m'aider seulement la première question ? merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aje ne sais pas si je suis dans la bon route de le daire comme ça...
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aj'ai fait de calculs, mais je ne sais pas si je les ai bien faits. merci
-
Vérifiée par Alloprof
Secondaire 4 • 2aBonjour,
...
Merci!!
-
Vérifiée par Alloprof
Secondaire 5 • 2aSalut, y a-t-il une différence entre le groupement phosphate de l'ADN et celui de l'ARN ? Si oui, laquelle ou lesquelles ?
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
...
-
Vérifiée par Alloprof
Secondaire 5 • 2asalut, c'est ma question. merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
...
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je dois faire créer 100 ml d'une solution du CuSO4 à 0,1 mol/L pour un laboratoire mais je ne suis pas sûre des démarches pour y arriver. Pouvez-vous m'aider?
...
Merci d'avance :)
-
Vérifiée par Alloprof
Postsecondaire • 2aBonjour, j'aurais besoin d'aide pour résoudre ce problème, merci!
...
-
Vérifiée par Alloprof
Secondaire 3 • 2aJ’ai une question! Comment on pourrait améliorer le protocole de ce laboratoire?
-
Vérifiée par Alloprof
Secondaire 3 • 2aJ’ai une question! Le pain est un aliment contenant de l’amidon. Quelle couleur prendrait le Lugol si on versait quelques gouttes sur une tranche de pain?
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ'ai besoin d'aide pour une questions s.v.p.
...