Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
J'aimerais bien savoir combien il y a d'électrons au maximum dans les orbitales p du niveau 3. Je dirais 6, mais pas sûr.
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour Alloprof! Est ce qu'à même température, tous les gaz peu importe leur nature ont la même énergie cinétique?
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonjour,
Je ne comprend pas très bien pourquoi une liaison ionique se brise lorsqu’elle est en présence d’eau.
-
Vérifiée par Alloprof
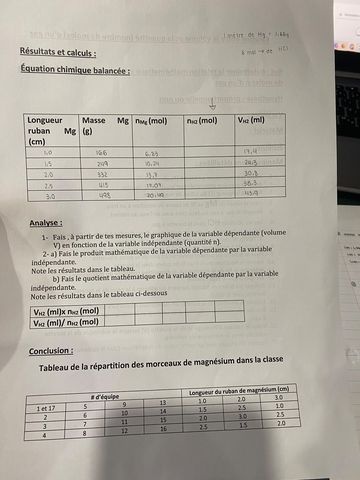
Secondaire 5 • 3aBonjour, j'ai fait un laboratoire en classe. Il faut que je fais mon rapport, mais il y a une chose qui m'empeche de cotinuer je ne comprends pas comme trouver le nombre de moles de H2 et je ne sais pas quelle est léquation balancée?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, est-ce qu'on peut mettre des paragraphes dans la conclusion d'un rapport de laboratoire en chimie ou ça doit être un texte continu ?
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonsoir,
Il y a quelque chose que je n’ai pas très bien compris. Est-ce que tous les ions qui existent sont mobiles ou non? Si non, qu’est ce qui explique la mobilité de certains ions?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je voulais savoir si on pouvait mentionner les unités de mesure utilisées dans un titre d'un tableau de résultat dans un rapport de laboratoire en chimie.
ex:Variation du volume en ML d’un gaz en fonction de sa température en Kmerci
-
Vérifiée par Alloprof
Secondaire 4 • 3aBonsoir, je ne comprends pas très bien la liaison covalente polaire de l’eau. Pourquoi l’échange d’électrons est-il plus près de l’oxygène et non au milieu?
Merci, bonne soirée!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je ne comprends pas pourquoi ´ reste 3 L dans la bouteille. Le gaz n’est-il pas supposé être tout expulsé? Merci
!
-
Vérifiée par Alloprof
Secondaire 5 • 3aPourquoi est-ce qu'un gaz refroidi ne changera pas de température ni de volume?
Merci :)
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour! la nature du gaz a-t-elle un impact sur le volume à différentes pressions appliquées? merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aEst-ce qu'un ballon gonflé à l'hélium s'élève dans les airs parce qu'il contient moins de molécules qu'un ballon gonflé à l'air?
Merci.
-
Vérifiée par Alloprof
Secondaire 4 • 3aquelles est la vitesse d'une balle de tennis possedant une energie cinétique de 100j et dont la masse estde 55g?
-
Vérifiée par Alloprof
Secondaire 2 • 3aEst ce que le mélange d'u jus jaune et d'un jus bleu est un changement chimique et est ce que c'est réversible ou pas.
Merci.
-
Vérifiée par Alloprof
Secondaire 1 • 3aUne bicyclette sa ce pèse en gramme ou kg?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
Dans un laboratoire sur la chaleur molaire, on me donne trois équation chimique : équation 1, équation 2 et équation globale. J'ai trouvé la chaleur molaire de l'équation 1 et de l'équation globale, et à partir de ça, j'ai trouvé la chaleur molaire(avec le calorimètre) de l'équation 2. Tout va bien, sauf que je n'arrive pas à trouver les variables dépendante et indépendante.
Voici les équations:
équation élémentaire 1: KOH(s) + H2O(l) → KOH(aq) + H2O(l)
équation élémentaire 2: KOH(aq) + HCl(aq) → H2O(l) + KCl(aq)
équation globale: KOH(s) + HCl(aq) → H2O(l) + KCl(aq)
Pouvez m'aider svp? Merci d'avance !
-
Vérifiée par Alloprof
Secondaire 2 • 3aSi un liquide jaune mélangé avec un liquide bleu produit un liquide vert, le changement de couleur n'est pas significatif; c'est-à-dire que du bleu et du jaune donne du vert. Ce changement de couleur n'est donc pas assez significatif et ne permet pas de savoir s'il s'agit d'un changement chimique.
est ce que c'est un changement physique et si on a les même propriétés caractéristique avant et après la transformation aussi si c'est irréversible ou pas
merci.
-
Vérifiée par Alloprof
Secondaire 5 • 3aJ'ai un problème: Al2(CO3)3 + Al2O3 + 3 CO2
Une quantité de 20,00g de cette substance se décompose dans un contenant scellé de 4,5 a une température de 120,0 degrés et une pression de 105,0 kPa. Quelle sera la pression finale dans le contentant lorsque tout les solide se sera décomposé?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Par quelle théorie cinétique des gaz je peux expliquer la variation de la valeur d'une constante dans une des lois simples des gaz ?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Présentement, j'étudie pour mon examen de chimie secondaire 5 qui est sur les comportements des gaz. Un des objectifs d'apprentissages est d'expliquer, à l'aide de la théorie cinétique de gaz, la variation de la valeur d'une constante dans une des lois simples des gaz. Je ne comprend absolument pas, j'ai fait des recherche, mais je ne trouve rien. Pouvez-vous m'aider?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour !
J'ai un examen de chimie demain et je voudrais m'assurer de tout maîtriser. J'ai tendance à être anxieuse ces temps ci. Avez-vous des exercices sur les lois simples des gaz et la loi générale de ceux-ci ?
Merci beaucoup de votre aide !
-
Vérifiée par Alloprof
Secondaire 5 • 3aEn fait il me demande pourquoi quand on a les 4 variables dans la formule la constante ne change jamais même si les variable changent, alors que si on mets juste 2 variable ensemble, la constante va changer!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, dans mon examen de Chimie secondaire 5, on m'a demandé d'expliquer pourquoi, dans la loi générale des gaz, la constante donné est toujours aléatoire dépendamment des différentes valeur des facteur tel que le volume, la quantité de gaz, la température et la pression.
Toutefois, dans la loi des gaz Parfait, on y mets les 4 variable en même temps. C'est-à-dire PV/NT qui sera toujours égale au même R (8.31). On m'a demander d'expliquer qu'est-ce qui influence ce changement. Je ne pouvais pas donner comme explication qu'on mettais les 4 variable en relation à la place de deux. J'ai besoin de trouver une autre explication.
-
Vérifiée par Alloprof
Secondaire 5 • 3aPourquoi V/T donne une constante différente alors que PV/NT= 8.31?
Quand toute les variables de gaz sont présente cela donne automatiquement 8.31
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, j'ai trouvé la chaleur molaire de l'équation 1 et de l'équation globale et en me demande, à partir des réponses précédentes, de trouver la chaleur molaire de l'équation 2. Comment procéder?
équation élémentaire 1: KOH(s) + H2O(l) → KOH(aq) + H2O(l)
équation élémentaire 2: KOH(aq) + HCl(aq) → H2O(l) + KCl(aq)
équation globale: KOH(s) + HCl(aq) → H2O(l) + KCl(aq)
Merci d'avance!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour je voulais savoir si ma réponse était bonne car dans le corrigé ça donne 8,95 3x10 à la 3 kPa mais ça me donne jamais la bonne réponse.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, voici un de nos laboratoires en chimie et les questions théoriques de ce laboratoire. Moi et ma partenaire ne comprennent pas comment répondre à ces questions
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, en fait, je ne comprends pas bien pourquoi lorsque le volume d'un gaz diminue de la moitié et la température absolue double, la pression du gaz doit multipliée par 4. Quelle est leur relation
-
Vérifiée par Alloprof
Secondaire 5 • 3abonjour. j'ai lu la page alloprof sur la loi de hess, mais je ne comprends pas trop comment on change les coefficients dans les équations. pour l'instant j'ai interchangé la 2e équation parce que le no2 est dans les réactifs, mais, par exemple, le o2 a un coefficient de 1/2 dans une des deux équations et de 1 dans l'autre, alors est-ce que je dois mettre 1/4 dans chaque vu qu'il n'y a qu'une demie mole de o2 dans le problème ? merci beaucoup pour votre aide :)
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
Comment fait-on pour calculer les incertitudes absolues et relatives d'une donnée convertie exemple, lorsque je converti 94,5 °C (Incertitude absolue: ± 0,5°C) (Incertitude relative: ± 0,5%) à 367,7 kelvins, quel sera l'incertitude absolue et relative de la donnée en kelvins?
Merci!