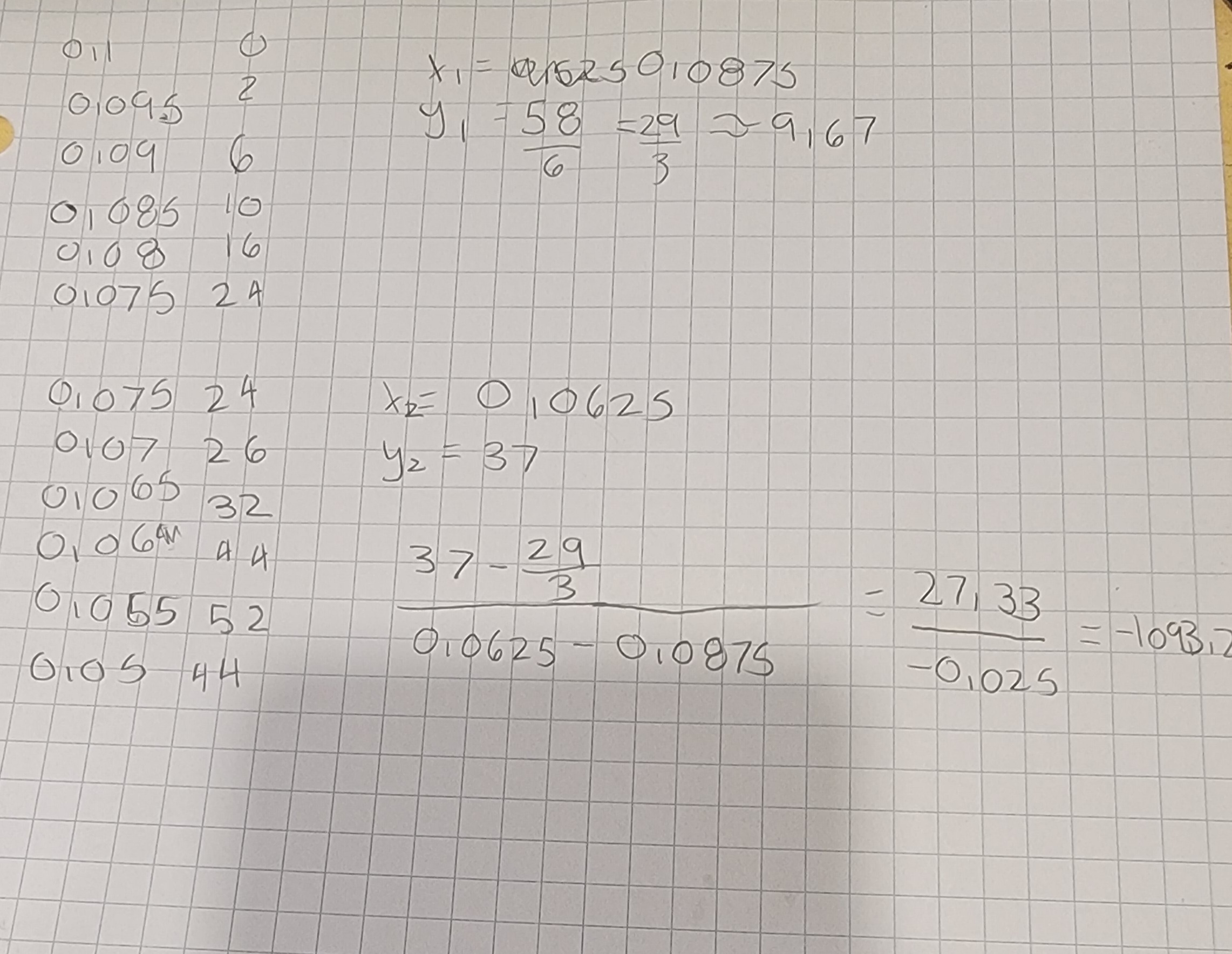Liste de discussions
-
Vérifiée par Alloprof
Secondaire 5 • 3aPouvez vous maider a trouver les reponses?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour!
Pourquoi la dissolution de CaCl2 sur des glaçons est exothermique, alors que celle de NaCl (sur des glaçons également) est endothermique?
Merci:))
-
Vérifiée par Alloprof
Secondaire 5 • 3aest-ce correct si je calcul la différence des Q afin de savoir si la réaction en temps que telle est exo ou endo? :) (Qfinal- Qinitiale)
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour Alloprof! Est-ce que sous le point de congélation, une substance peut quand même continuer de transférer de l'énergie thermique?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, mon professeur veut que nous utilisons la méthode du tableau pour la stoechiometrie pour ce numéro mais j'ai oublié comment le faire avec l'énergie. Pouvez-vous m'aider s'il vous plaît?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour Alloprof! Est-ce que la capacité thermique massique dépend de l'état physique de la substance?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, merci pour votre explication.
Voici ce que je ferais pour le CH2CHCH2OCH3
Je mettrais le ch2 à gauche, le ch au milieu, suivi du ch2, et à droite, je terminerais avec du ch3
Pour le ch3chbrcch, pourriez-vous svp m'indiquer comment faire ?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Je n'ai vraiment pas compris l'explication qui m'a été donnée. Pouvez svp m'aider avec la structure de Lewis du
1- CH3CHCH3COOH
2- CH2CHCH2OCH3
3- CH3CHBRCCh
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, quelle conclusion je pourrais tirer si mon milieu 1 le Q est positif et si mon milieu 2 le Q est négatif…?(en parlant des réactions exo et endo)
Si les deux Q sont négatifs?
Si les deux Q sont positifs?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Pouvez svp m'aider avec la structure de Lewis du
1- CH3CHCH3COOH
2- CH2CHCH2OCH3
3- CH3CHBRCCh
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 3aSi ma température du milieu 1, soit 25ml d’eau) est de 24° et que ma température finale en ajoutant 1g de l’hydroxyde de sodium est de 30°. Démontrer si cela est une réaction endothermique ou exothermique. Est-ce que ma température initiale de l’hydroxyde de sodium est de 6°C (30-24) et est-ce okay si je calcul sa variation de température avec ces données:
30°C - 6ºC = 24°C (variation de température de l’hydroxyde de sodium)
j’ai déjà regardé les fiches d’aides mais cela ne m’a pas aidé je voudrais une réponse directement reliée à mon problème
mon problème en résumé (ce que j’ai fais)
milieu 1:
Q: ?
m1: 25ml=25g
C: 4,19j/ g * ºC
Delta T : 30°C-24°C= 6°C
milieu 2:
Q?
M: 1g
C : 4,19 j/g * ºC
Delta T: 30°C - 6°C = 24°C
est-ce véridique? Je voudrais avoir concrètement se que je devrais faire…svp
*ensuite, j’appliquerais la formule q=mcdelta T*
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour je dois effectuer le calcul suivant mais je ne sais pas comment faire puisque je n’ai pas la capacité thermique du HCl et du NaOH.Quelle sera la température finale ?
Merci bcp
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour,
Quelle est l'insertitude d'une seringue de 140ml?
-
Vérifiée par Alloprof
Secondaire 5 • 3aSi ma température du milieu 1 est de 24° et que ma température finale en ajoutant de l’hydroxyde de sodium est de 30°. Est-ce que ma température initiale de l’hydroxyde de sodium est de 6°C (30-24) et est-ce okay si je calcul sa variation de température avec ces données: 30°C - 6ºC = 24°C (milieu 2)
j’ai déjà regardé les fiches d’aides mais cela ne m’a pas aidé je voudrais une réponse directement reliée à mon problème
mon problème en résumé:
Variation de température du milieu 1 : 30°C - 24°C = 6ºC
variation de température du milieu 2:
30°C - 6°C = 24°C
est-ce véridique?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je n’arrive pas à comprendre d’où provient l’énergie dans les transferts d’énergies lors des réactions chimiques
-
Vérifiée par Alloprof
Secondaire 5 • 3aj’ai un problème à résoudre en chimie :
Je mesure 25ml d’eau distillée. Je note la température et elle est à 24ºC. Ensuite, j’ajoute 1g d’hydroxyde de sodium à l’eau. Je note la température après, et elle est de 30°C. Sachant que la capacité thermique massique de l’eau est de 4,19, quelle est la quantité d’énergie du milieu 2?
ma qts est la suivante: est-ce que la masse du milieu 2 est de 25g + 1g = 26 g? Et est-ce que la variation de température pour les deux milieux est la meme?
je suis déjà allé voir la fiche sur les calculs calorimétries mais je n’arrive toujours pas à savoir si la masse 2 est 26g ou 1 g
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je me demandais comment faire un tableau de stœchiométrie avec l'énergie?
Merci d'avance :)
-
Vérifiée par Alloprof
Primaire 3 • 3ade quoi est composée l'eau
et quelle est la formule chimique de l'eau
-
Vérifiée par Alloprof
Secondaire 5 • 3aj’ai un problème à résoudre en chimie :
Je mesure 25ml d’eau distillée. Je note la température et elle est à 24ºC. Ensuite, j’ajoute 1g d’hydroxyde de sodium à l’eau. Je note la température après, et elle est de 30°C. Sachant que la capacité thermique massique de l’eau est de 4,19, quelle est la quantité d’énergie du milieu 2?
ma qts est la suivante: est-ce que la masse du milieu 2 est de 25g + 1g = 26 g?
-
Vérifiée par Alloprof
Secondaire 5 • 3aJ'ai un laboratoire a remettre, mais ma question serai de est ce que on peut chercher le Q du par exemple du NaOH avec l'eau.
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir!
Dans une burette à gaz (à l'envers avec un bouchon avec un trou) dans un bécher d'eau, lorsque deux réactifs réagissent et qu'un gaz est créé, est-il possible que du gaz s'échappe par le trou du bouchon si jamais de l'air y est rentré lorsqu'on a mis le bouchon et que l'air créé un passage pour que le gaz s'échappe du montage?
Merci
-
Vérifiée par Alloprof
Secondaire 4 • 3aSi delta T est négatif, c'est endothermique ou exothermique???
-
Vérifiée par Alloprof
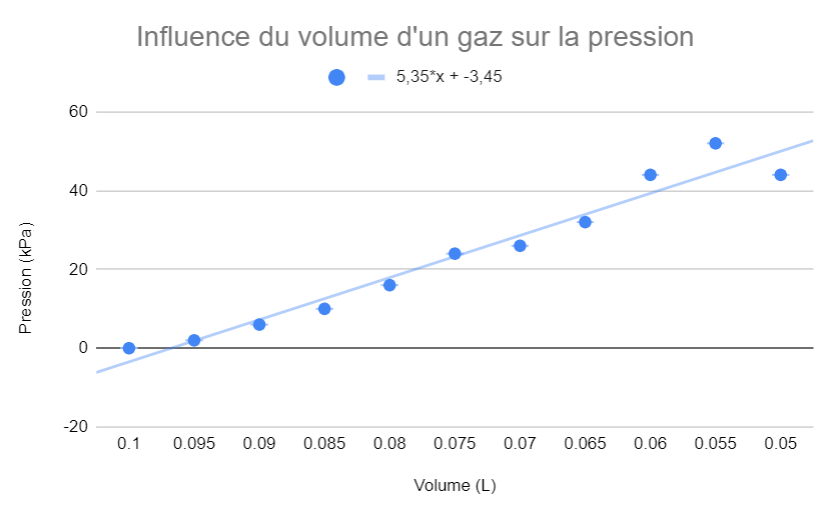
Secondaire 5 • 3aBonjour! Pourquoi exprime-t-on la relation entre le volume, la quantité de gaz et la nature du gaz( Loi d'Avogadro?) en fonction du nombre de particules de gaz et non en fonction de la masse du gaz? Merci beaucoup!
-
Vérifiée par Alloprof
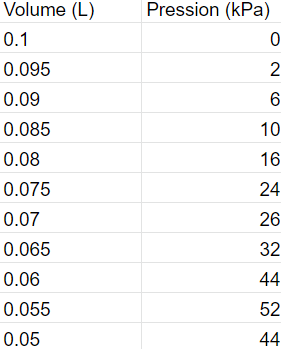
Secondaire 5 • 3aBonjour, je me demandais pourquoi je n'arrivais pas à la même réponse que la formule sur le graphique pour le m de la formule de la droite de régression? Ça m'a donner -1093,2. Je ne suis pas sûre laquelle est la bonne. :(
-
Vérifiée par Alloprof
Primaire 4 • 3aBonjour pourier vous maider avec votre
Sistem je ne comparant pa beaucoup......
merci!
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonsoir, j’ai besoin d’aide pour un devoir de chimie… J’ai regardé le lien suivant ->https://www.alloprof.qc.ca/fr/eleves/bv/chimie/la-loi-des-gaz-parfaits-c1009mais ne m’a aidé a résoudre le problème… Merci à l’avance
-
Vérifiée par Alloprof
Secondaire 5 • 3aAllo est-ce que quelqu'un peut m'aider avec cette question, merci!
Considérons l'équilibre suivant :
2 COF2 (g) ⇆ CO2 (g) + CF4 (g) Kc = 1,96
On introduit 0,372 moles de COF2 dans un contenant de 971 mL à 1000°C.
Quelle sera la concentration molaire de COF2 à l'équilibre ?
(Petit rappel mathématique : A2/ B2 = (A/B)2 )
-
Vérifiée par Alloprof
Secondaire 5 • 3aAllo, est-ce que quelqu'un peut m'aider avec cette question, merci!
On étudie la réaction suivante, à 1260K :
CO2 (g) + H2 (g) ⇆ CO (g) + H2O (g) Kp = 1,59
A l'équilibre P(H2) = 0,659 atm, P(CO2) = 0,320 atm et P(H2O) = 0,159 atm.
Quelle est la pression de CO à l'équilibre ?
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour, je ne comprend pas comment utiliser le volume molaire gazeux fans une formule.
-
Vérifiée par Alloprof
Secondaire 5 • 3aBonjour! Je comprend pas comment calculer la chaleur molaire de dissolution. Quelqu’un pourrait m’aider?