Liste de discussions
-
Secondaire 5 • 2a
est-ce que le gaz parfait réagit chimiquement? merci
-
Vérifiée par Alloprof
Secondaire 5 • 2asalut alloprof j'aurais une question
...
on prépare une solution en dissolvant 98,7g de AL(NO3)3 dans 879,3g d'eau. La solution présente un volume final de 648,2mL. Quelle est la masse volumique de la solution?
je ne comprends pas ce que je dois faire
-
Vérifiée par Alloprof
Secondaire 4 • 2aComment je sais si une dissociation d’électrolytes est possible ou non?
-
Vérifiée par Alloprof
Secondaire 3 • 2aJe ne comprends toujours pas pourquoi nous utilisons le Lithium dans les téléphones cellulaires ?
...
De plus, j'ai entendu que c'est réactif.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir! Est-il possible qu'il y ait plus d'une variable indépendante dans un laboratoire? Par exemple, dans une équation, est-ce que les variables indépendantes peuvent être les réactifs, tandis que les variables dépendantes sont les produits?
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aComment sait-on si l'on doit mettre le chiffre contenant le nombre d'atome en avant ou en petit après l'atome. Par exemple, disodium. Inscrit-on 2 Na ou Na2 ? Et pourquoi?
-
Vérifiée par Alloprof
Secondaire 5 • 2aJ'ai un problème en chimie que j'ai de la difficulté à résoudre:
...
Le premier contient de 0,151g de 02 et le deuxième contient 0,171g d'un gaz inconnu.
Quel est ce gaz inconnu?
J'ai de la difficulté à éssayer de trouver la masse molaire du gaz inconnu, est-ce je pourrais avoir de l'aide à ce niveau?
-
Vérifiée par Alloprof
Secondaire 5 • 2aDans un labo de chimie que j’ai à faire il faut que je calcul la température avec cette formule :
...
sauf que je me demandait s’il fallait mettre toujours la température en kelvin
exemple si je fait:
35ml/293k= 2,2/t2
t2= 18,42 k
sauf que dans mon labo il est impossible que j’ai fait arriver la température à -254 degré Celsius
alors je me demandais est ce que la température que j’ai trouver est vraiment en kelvin ou elle est en Celsius pour une certaine raison ?
-
Vérifiée par Alloprof
Secondaire 5 • 2aje ne comprend pas ce numéro pouvez-vous m’aider ?
-
Vérifiée par Alloprof
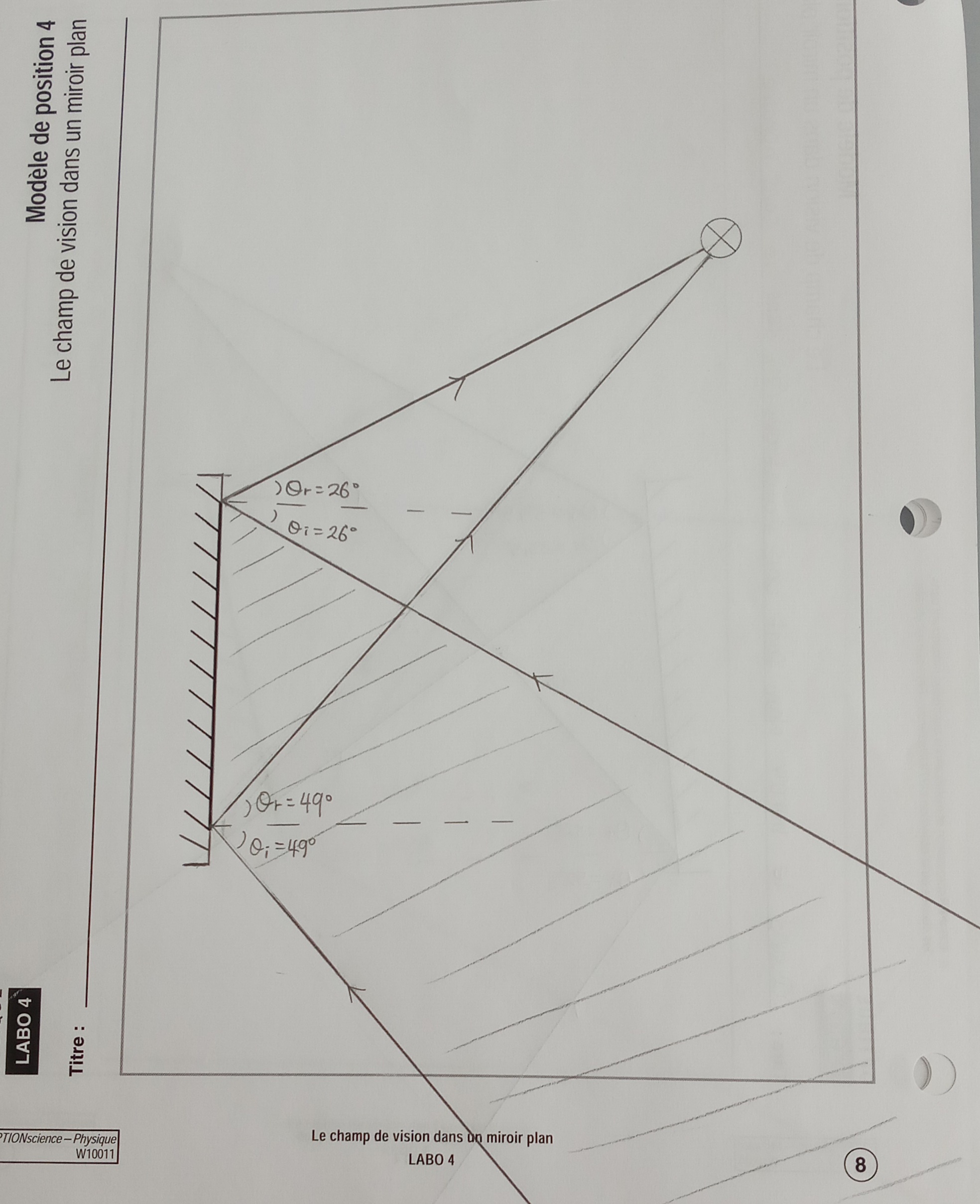
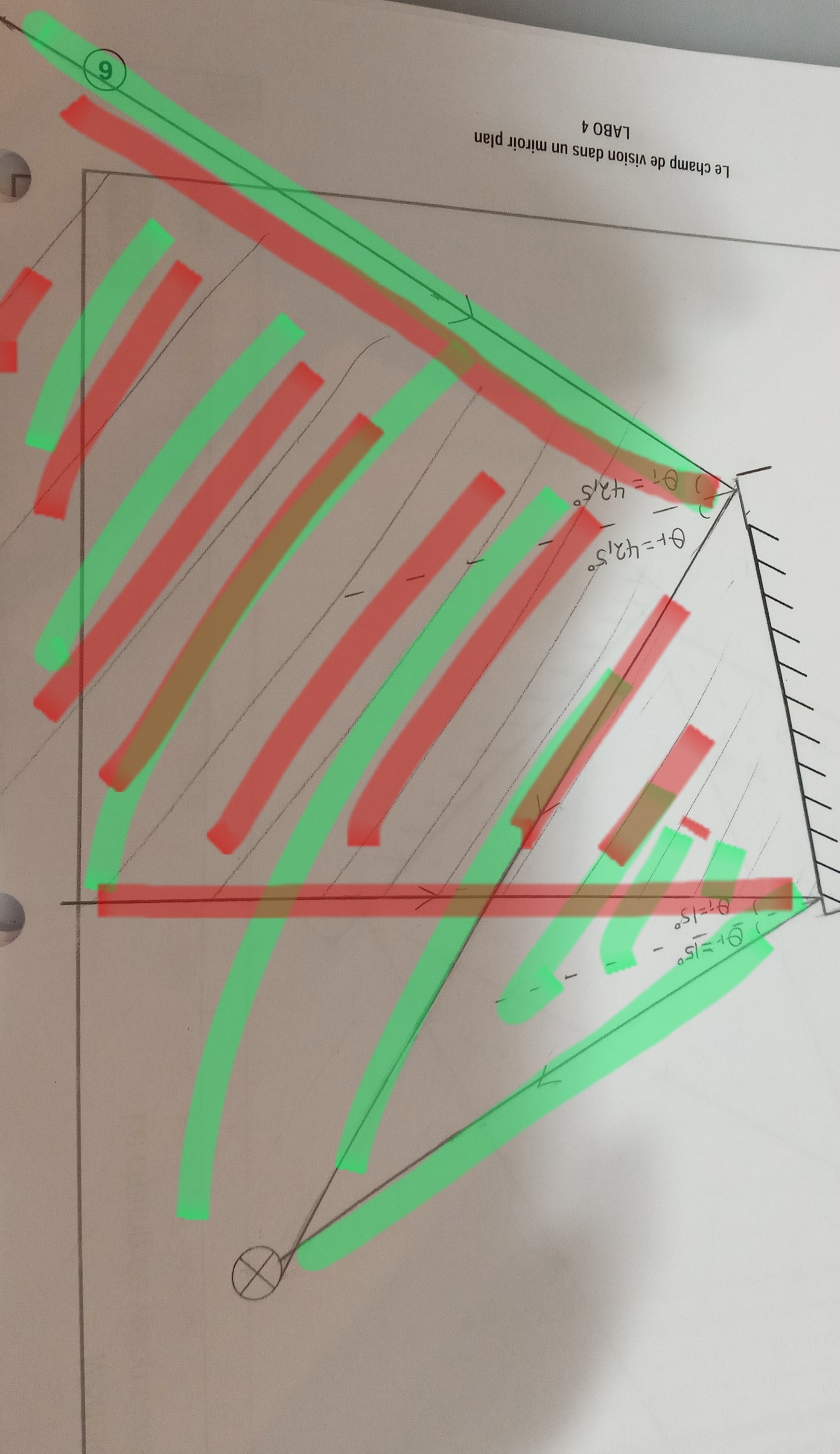
Secondaire 5 • 2aje ne sais pas si j'ai bien indiqué le champ de vision ici.
...
pouvez-vous me donner un truc facile de savoir où est le champ de vision? merci
-
Vérifiée par Alloprof
Secondaire 5 • 2aLaboratoire de Chimie : Variation du volume selon la température (loi de Charles) : Quelles sont les sources d'erreurs les plus fréquentes de ce laboratoire ? Il y avait des bulles de gaz sous le ménisque, alors le volume précis était difficile à mesurer. Exception de la fiabilité des instruments de mesure, quelles sont les autres sources d'erreur possible ? Variation de pression ? Inclinaison du cylindre gradué ? Merci de m'aider à éclairer les autres !
-
Vérifiée par Alloprof
Secondaire 5 • 2asalut,
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aPouvez-vous m'aider s'il vous plaît?
...
Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 2alors qu'il y a le même nombre de particules de deux types de gaz différents, est-ce que la pression exercée pour chacun de gazest égal à l'autre?
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aje voudrais savoir si j'ai fait des erreurs svp.
...
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour!
...
Merci!
-
Vérifiée par Alloprof
Secondaire 1 • 2aBonjour,
...
-
Vérifiée par Alloprof
Secondaire 3 • 2aBonjour!
...
En lisant l'article, je n'ai pu que trouver des propriétés physiques.
Merci !
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour alloprof!
...
Puis si une boîte de 1L de diazote et une autre boîte de 2L de dioxygène, aux mêmes conditions de pression et température, avaient des masse différentes?
C'est sur les loi simples des gaz.
-
Vérifiée par Alloprof
Secondaire 5 • 2aje ne comprend plus pas l’énergie continue des gaz et j’aurais besoin d’aide avec ce numéro
-
Vérifiée par Alloprof
Postsecondaire • 2aJ’ai bientôt un examen de chimie qui porte sur la nature de la lumière et le modèle atomique de Bohr et j’aimerais avoir de l’aide pour un numéro s’il vous plaît.
...
Une raie de la série de Balmer apparaît à une longueur d’onde de 486,1 nm.
a) Quelle est la différence d’énergie entre les deux niveaux en jeu dans cette raie d’émission?
b) Démontrer et expliquer quelle transition électronique produit cette raie d’émission.
Ce que j’ai pu trouver pour l’instant:
E = h • c/v
= 4,089 • E-19 J
Merci d’avance!
-
Vérifiée par Alloprof
Secondaire 5 • 2abonjour ! quel est le gaz dans ce phénomène et quel est son rôle ?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, je voulais savoir si l'échelle de température absolue est celle qui nous permettra de convertir de k en C
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, j'ai un rapport de laboratoire en chimie à rédiger et je voulais savoir si une hypothèse pouvait est longue et être soutenu par 2 lois.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour, j'ai une question de chimie. On a un graphique initiale (rouge), qui indique le volume en fonction de la température en Kelvin. Ensuite, on indique que la pression a augmenter, alors quelle serait le nouveau graphique, le vert ou le bleu?Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 2aEst-ce que le volume molaire est une propriété caractéristique des gaz?
-
Vérifiée par Alloprof
Secondaire 5 • 2aEst-ce que quelqu’un pourrait m’aider pour faire ce numero ? Je ne comprend pas
-
Vérifiée par Alloprof
Secondaire 5 • 2aPeut-on m'expliquer que sont les variables calculées et mesurées dans un rapport de laboratoire?
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonsoir , est ce que vous pouvez m'aider pour cette question svp !
...
Par une journée ensoleillée où la pression atmosphérique est de 102,7 kPa, le manomètre
à cadran d’une bonbonne de propane indique une pression de 0 kPa. Deux jours plus tard,
alors que le temps est pluvieux et que la pression atmosphérique a chuté, le manomètre
de la bonbonne indique une pression faible, mais supérieure à zéro. Expliquez ce phénomène.
-
Vérifiée par Alloprof
Secondaire 5 • 2aBonjour,
...
Mais disons qu'on a un gaz dans une seringue a un certain volume et température, si on tire le piston de la seringue pour augmenter son volume, est-ce que la température du gaz va changer puisqu'ils les deux variables sont directement proportionnel? Si ou comment est-ce possible.