Liste de discussions
-
Vérifiée par Alloprof
Primaire 3 • 7mJ'ai pas trop compris c'est fait de quoi l'eau?
-
Vérifiée par Alloprof
Postsecondaire • 7mBonjour, je suis présentement en train de faire on cahier de lab en chimie pour la synthèse d'acide benzoïque. On utilise du benzaldéhyde (on ajoute 15 ml du NaOH 10% jsp si c'est important ou non), du KMnO4 (agent oxydant) et le NaHSO3. la prof me demande d'écrire les équations qui y sont impliquées et de les équilibrer en gardant en compte l'oxydoréduction en milieu basique. J'ai aucune idée où commencer. J'aurais besoin d'Aide. Au départ, j'Avais de faire une réaction en chaine (ex.: Benzaldéhyde + NaOH = x, x + KMnO4 = y, etc...)
Est-ce qu'on peut me diriger vers le bon chemin?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 7mBonsoir, pourquoi ici ils ont diviser? Il ne faut pas plutôt multiplier?Merci
-
Vérifiée par Alloprof
Secondaire 1 • 7mBonjour, j'aimerai une réponse à ce problème, ou du moins comment le résoudre:Merci!
-
Vérifiée par Alloprof
Secondaire 5 • 7mBonsoir! Pourriez-vous m'aider avec ceci?Merci
-
Vérifiée par Alloprof
Primaire 6 • 7mJe ne comprends pas ce qu’est l’inertie
-
Vérifiée par Alloprof
Secondaire 5 • 7mBonsoir,
Est-ce que c’est correct qu’une équation contienne une fraction, même après les manipulations d’équations partielles lors de la résolution avec la loi de Hess ?
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 7mBonjour,
Je sais comment trouver l'enthalpie avec la loi de Hess mais je ne comprends pas comment trouver la variation de température la valeur de la chaleur molaire avec. Que faire ?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 7mBonjour,
Il y a un problème sur la loi de hess que je n'arrive pas à comprendre.
Voici la résolution selon mon enseigant:
3. Les deux équations suivantes représentent les réactions dans lesquelles le
dioxyde de carbone gazeux est produit lors de la combustion du carbone solide et
du monoxyde de carbone.
C (s) + O2 (g) → CO2 (g) + 394 kJ
CO (g) +
1 O2 (g) → CO2 (g) + 283 kJ
En utilisant ces deux équations, trouve combien de chaleur sera produite dans la
réaction suivante:
C (s) +1 O2 (g) → CO (g) + kJ
- Equation Globale:
2 C (s) + O2 (g) → 2 CO (g)
- Manipulation des équations partielles:
2 C (s) + 2 O2 (g) → 2 CO2 (g) ΔH= - 788 kJ
2 CO2 (g) → 2 CO (g) + O2 (g) ΔH= + 566 kJ
- Additionner les réactifs ensemble et les produits ensemble :
2 C (s) + 2 O2 (g) +2 CO2 (g) → 2 CO2 (g) + 2 CO (g) + O2
- Additionner les enthalpies pour avoir l’enthalpie de la réaction :
ΔH = - 788 kJ + 566 KJ = -222 kJ
2 C (s) + O2 (g) → 2 CO (g) + 222 kJ ou C(s) + (1/2) O₂(g) → CO(g) + 111 kJ
Ce que je ne comprend pas:
Pourquoi il y a 2 solutions? Comment on trouve l'équation globale? L'équation C (s) +1 O2 (g) → CO (g) + kJ n'est-elle pas l'équation de base? Je suis vrm mélangée..
Merci.
-
Vérifiée par Alloprof
Secondaire 5 • 7mBonjour,
En modifiant les équations partielles dans la lois de Hess, est ce que ça change quelque chose si j'écris: 2 NO2 (g) → O2 (g) +2NO (g) à la place de 2 NO2 (g) → 2 NO (g) + O2 (g)
en sachant que l'équation non midifié est: NO (g) +1 O2 (g) → NO2 (g) et que l'équation globale est: N2 (g) + O2 (g) → 2 NO (g)
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonsoir je sais que c'est tard mais j'aimerai savoir si quelqu'un aurait la gentilesse de m'aider à comprendre le principe de le chatelier pour le volet du changement de temperature et de pression
-
Vérifiée par Alloprof
Secondaire 2 • 8mÀ quoi sert une fiole?
-
Vérifiée par Alloprof
Secondaire 5 • 8mDans une réaction où aucun des réactifs n'est aqueux, où aucun produit ne contient de l'hydrogène ou de l'oxygène et où l'eau n'est pas indiqué au dessus de la flèche de réaction, est-ce que c'est possible pour le(s) réactif(s) d'être aqueux?
Par exemple si j'ai:
Na(s) + Cl2(g) → NaCl(?)
Le chlorure de sodium devrait être solide n'est-ce pas? Sinon d'où viendrais l'eau?
-
Vérifiée par Alloprof
Postsecondaire • 8mBonjour, j'ai une question pour mon cours de chimie organique.
J'ai de la difficulté à identifier si une substance est plus soluble dans du H2O ou du dichlorométhane.
Par exemple, pour le salicylate de méthyle, j'ai trouvé qu'il a une masse molaire (152,15 g/mol) plus près de celle du dichlorométhane que celle de l'eau, et qu'il est polaire. J'ai aussi trouvé que cette molécule peut faire des ponts hydrogènes avec l'eau. Ces informations m'indiquent des réponses opposées, donc je ne suis pas certaine de la réponse qui est juste.
J'ai le même problème avec le salicylate de sodium. Sa masse molaire est plus proche de celle du dichlorométhane, mais il peut faire des ponts hydrogènes avec l'eau.
Merci d'avance!
-
Vérifiée par Alloprof
Secondaire 3 • 8mBonjour
Dans les molécules où il y a 3 sortes d'atomes,certains atomes vont s'associer pour former quoi ?
Merci de m'explique
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonjour,
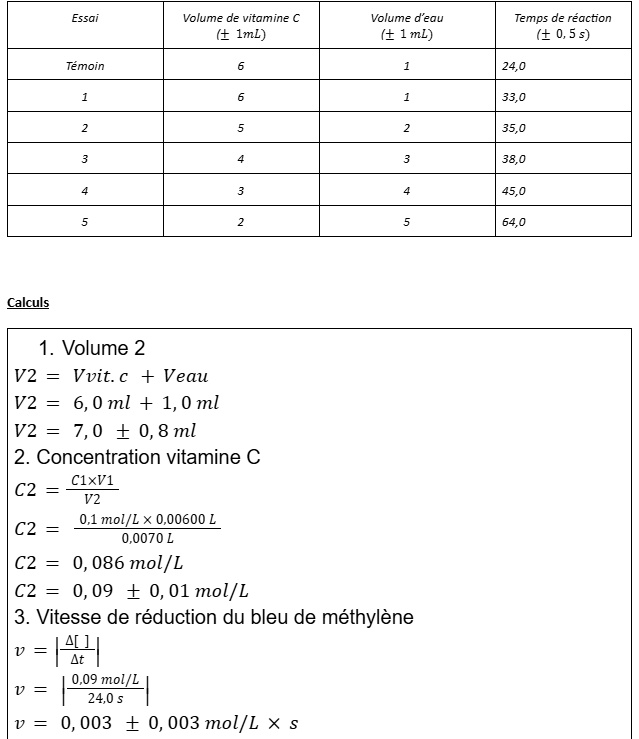
Je dois faire mon rapport de laboratoire sur la réduction du bleu de méthylène. Je ne comprends pas exactement les calculs que je dois faire, car dans l'exemple en classe, mon enseignante nous a fait calculer la concentration de vitamine C et ensuite elle a mis cette concentration / temps de réaction. Cependant, c'est la vitesse de réduction du bleu de méthylène en présence de vitamine C qu'on doit calculer.
-
Vérifiée par Alloprof
Secondaire 5 • 8mJe ne comprend pas ce qu'est l'ordre de réaction et la réaction globale. Pouvez-vous me l'expliquer ?
-
Vérifiée par Alloprof
Secondaire 3 • 8mBonjour
J'ai un synthèse de chimie à finir, j'ai fini les mots que je les arrivées mais j'ai pas arriver à finir le reste.
Je besoin qui me corrige qu'est ce que je le fais et de finir qu'est ce que il me reste.
Merci😊.
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonjour je ne comprend pas pourquoi l’énoncé c) est faux
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonjour je ne comprend pas le b) pouvez vous me l’expliquer?
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonjour!
Je ne suis pas sûre de comment justifier cela:
Le pourcentage d’erreur entre le ΔH en une seulement étape et en deux étapes est de 0%. Ce pourcentage s’explique entre autres par la nature des neutralisations faites. En effet, ce type de réaction se produit rapidement, ce qui réduit considérablement les pertes de chaleurs dans l’environnement. Ceci pouvant notamment être prouvé par le fait que nous devions observer vigoureusement le thermomètre afin de ne pas manquer les hausses de température. Pour ce qui est de la faible quantité de chaleur qui aurait tout de même pu s’échapper malgré la rapidité de la réaction, l’utilisation d’un verre en polystyrène aurais permis de limiter cette perte grâce à ses propriétés isolantes.
Or, pendant l'expérience, nous avons également produit une dissolution, alors comment elle n'a pas érroné les résultats? (le labo est en lien avec la loi de hess, réaction globa: neutralisation KOH (s), rx élémentaire: dissolution KOH(s), neutralisation KOH (aq))
merci
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonjour, je n'ai pas compris l'équilibre chimique au quotidien. Pouvez-vous m'aider svp.
-
Vérifiée par Alloprof
Secondaire 5 • 8mComment peut-on déterminer si une réaction chimique est réversible ou non à partir d'un diagramme énergétique?
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonsoir! Merci pour l'explication:https://www.alloprof.qc.ca/zonedentraide/discussion/121881/questionJuste pour être sûre, dans la première partie, on fait réagir 50ml HCl (aq) avec du KOH
dans la deux réaction on fait dissoudre la même quantité de KOH dans 50ml d'eau
puis dans la troisième, on fait réagir les 50mL d'KOH avec 50mL d'HCl
Pour ces deux dernières partie, est-ce que la quantité d'eau reste bel et bien idem à la réaction numéro 1 (notre reaction globale)?
Merci
-
Vérifiée par Alloprof
Secondaire 5 • 8mBonsoir, nous avons travaillon sur un rapport de laboratoire dans lequel nous devons déterminer de la chaleur molaire d’une reaction globale.
En laboratoire, nous avons eu deux partie
la première KOH (s)+HCl (aq)→KCl (aq)+H2 O (l). (nous avons déterminer la chaleur molaire de la neutralisation de KOH en observant le delta T de l'eau)
La deuxième était composé de deux réaction
1) dissolution de KOH solide
2) neutralisation du KOH en solution aqueuse.
Pour ces deux réactions, nous avons déterminer le delta H du KOH a partir du delta T de l'eau.
Maintenant que cela est dit, le problème est en soi les variables. Il nous faut déterminer Variable indépendante, Variable dépendante et la Constante.
Or, nous n'avons aucune idée.
Pourriez-vous nous aider? Merci
-
Vérifiée par Alloprof
Primaire 6 • 8mDe quoi est fait le slime et ses ingrédients svp.
-
Vérifiée par Alloprof
Secondaire 5 • 8mje ne comprend pas la formule pour calculer la vitesse générale d'une réaction en chimie de sec.5
-
Vérifiée par Alloprof
Secondaire 5 • 8mje ne comprend pas la vitesse de réaction des gaz
-
Vérifiée par Alloprof
Secondaire 5 • 8mJe comprend pas cette question, pourquoi il y aurait une différence entre la loi de hess et le bilan énergétique? (voir image)
-
Vérifiée par Alloprof
Secondaire 5 • 8mQuelle est l'incertitude d'une masse molaire ?