Secondaire 3 • 2a
Bonjour, je ne comprends pas vraiment cet exercice, est-ce que vous pourriez m'aider svp? Merci d'avance!
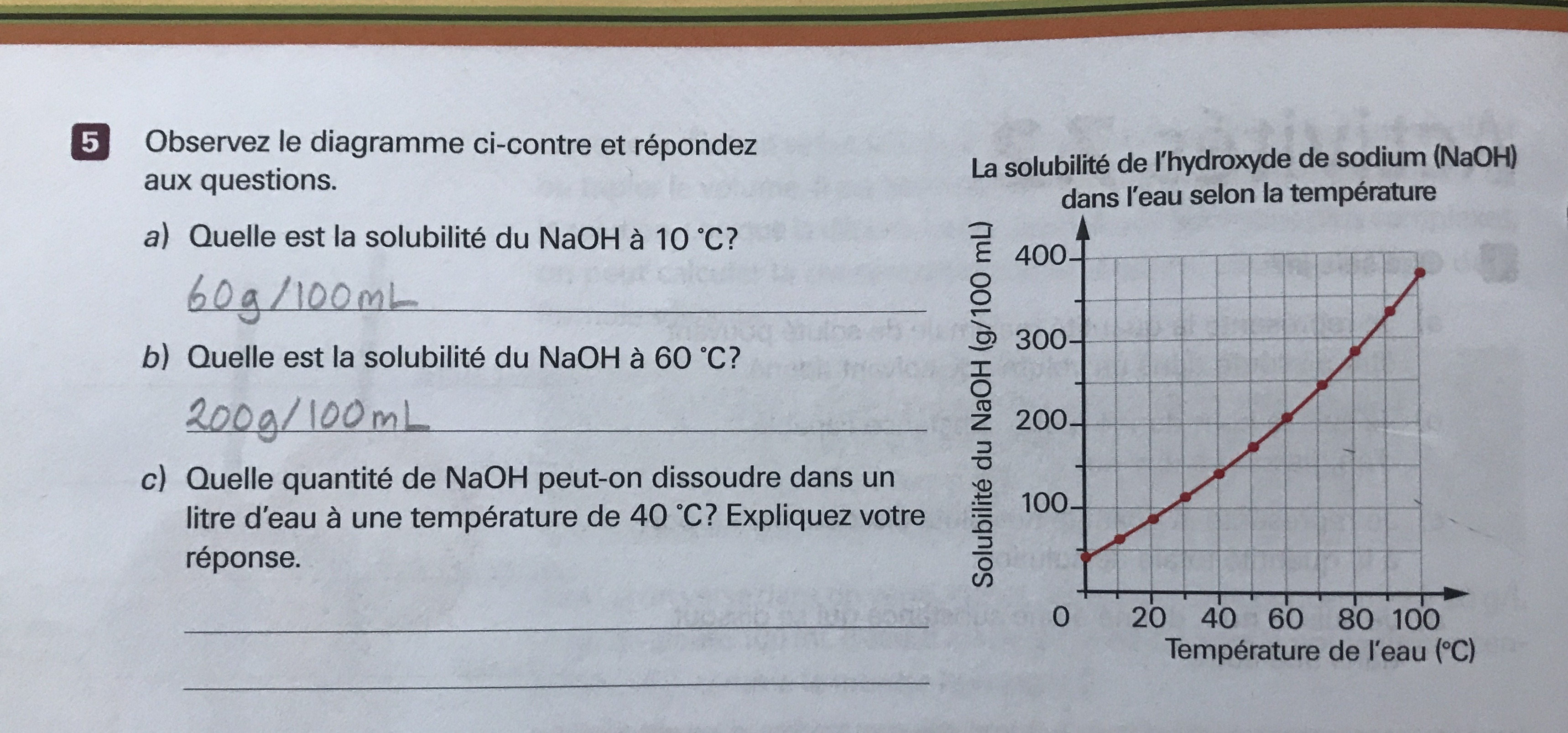
Quelle quantité de NaOH peut-on dissoudre dans un litre d'eau à une température de 40ºC? Expliquez votre réponse.






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Merci pour ta question!
Tu as bien compris et réussi la partie a) et b) de la question.
Quant à la partie c), il faut trouver la masse de NaOH qui peut être dissoute dans 1 L. Pour ce faire, il faudra appliquer une variante de la formule de la concentration (C = m/V) :
$$ m = C•V $$
• m : masse (g)
• C : concentration (g/L)
• V : volume (L)
Cependant, avant même d'appliquer cette formule, tu dois d'abord trouver la solubilité du NaOH à 40 °C, c'est-à-dire, environ 140 g/100 mL. Ensuite, tu dois convertir cette concentration en g/L pour pouvoir utiliser la formule. Puisque 100 mL rentre 10 fois dans 1 L, tu peux simplement multiplier par 10 la concentration que tu avais obtenue. Ainsi, il ne te reste qu'à appliquer la formule :
$$ m = C•V $$
$$ m = \frac{1400\:g}{1\:L}•1\:L = 1400\:g $$
Cette fiche du site d'Alloprof explique les concentrations en g/L :
N'hésite pas si tu as d'autres questions!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!