Secondaire 4 • 4a
bonsoir, j’ai 19 exercices à faire sur la nature d’une liaison. la façon de trouver la différence d’électronégativité entre deux éléments et de dire de quel type de liaison il s’agit, reste encore flou à mes yeux, alors je me demandais s’il était possible de me faire un exemple pour commencer.
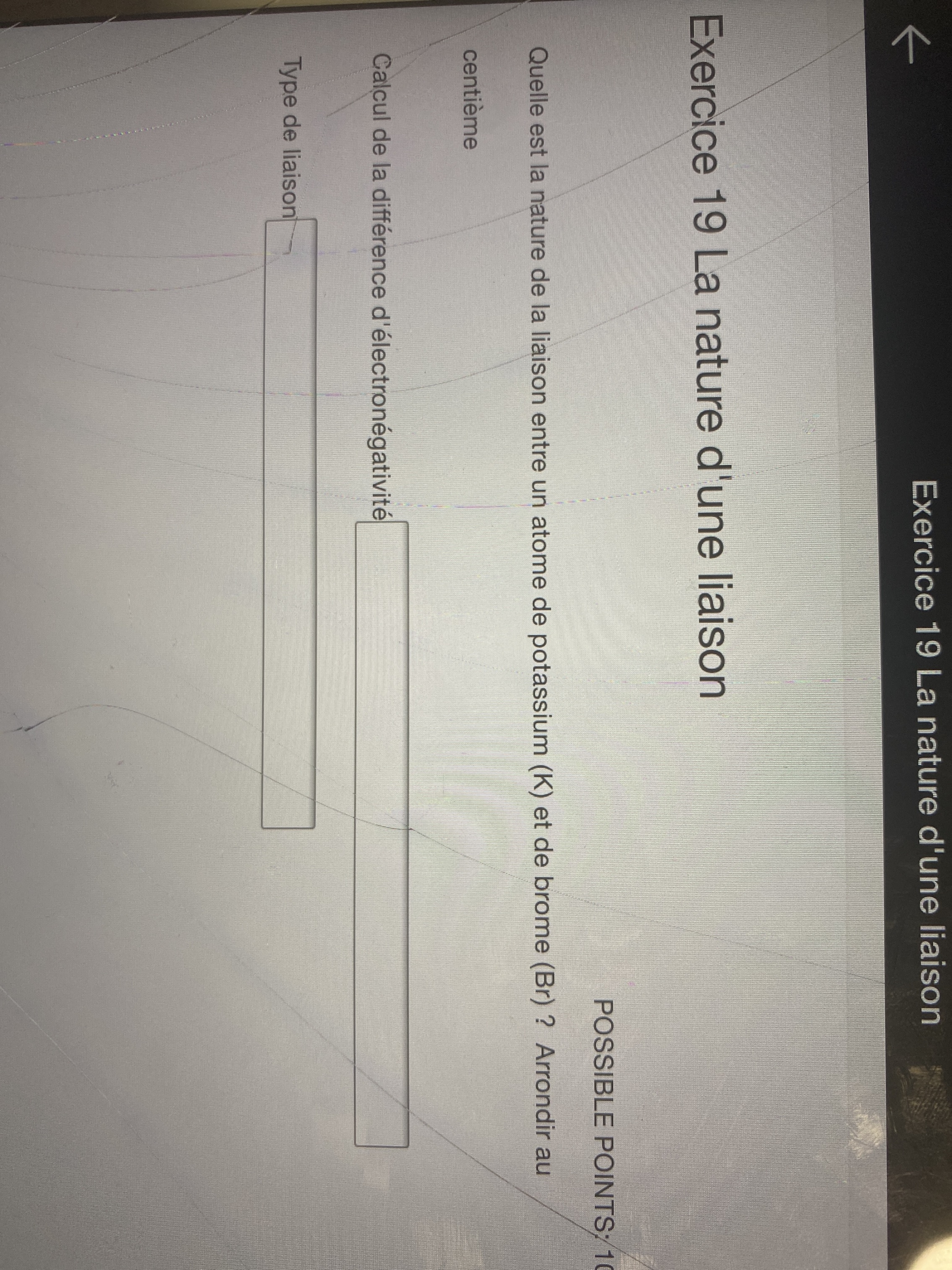
voici le a)
évidemment, il faut arrondir sa réponse au centième et utiliser l’échelle de Pauling.






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour AbafarBrave,
Merci pour ta question, il est vrai qu'il peut être difficile de s'y retrouver entre les concepts d'électronégativité et de liaisons!
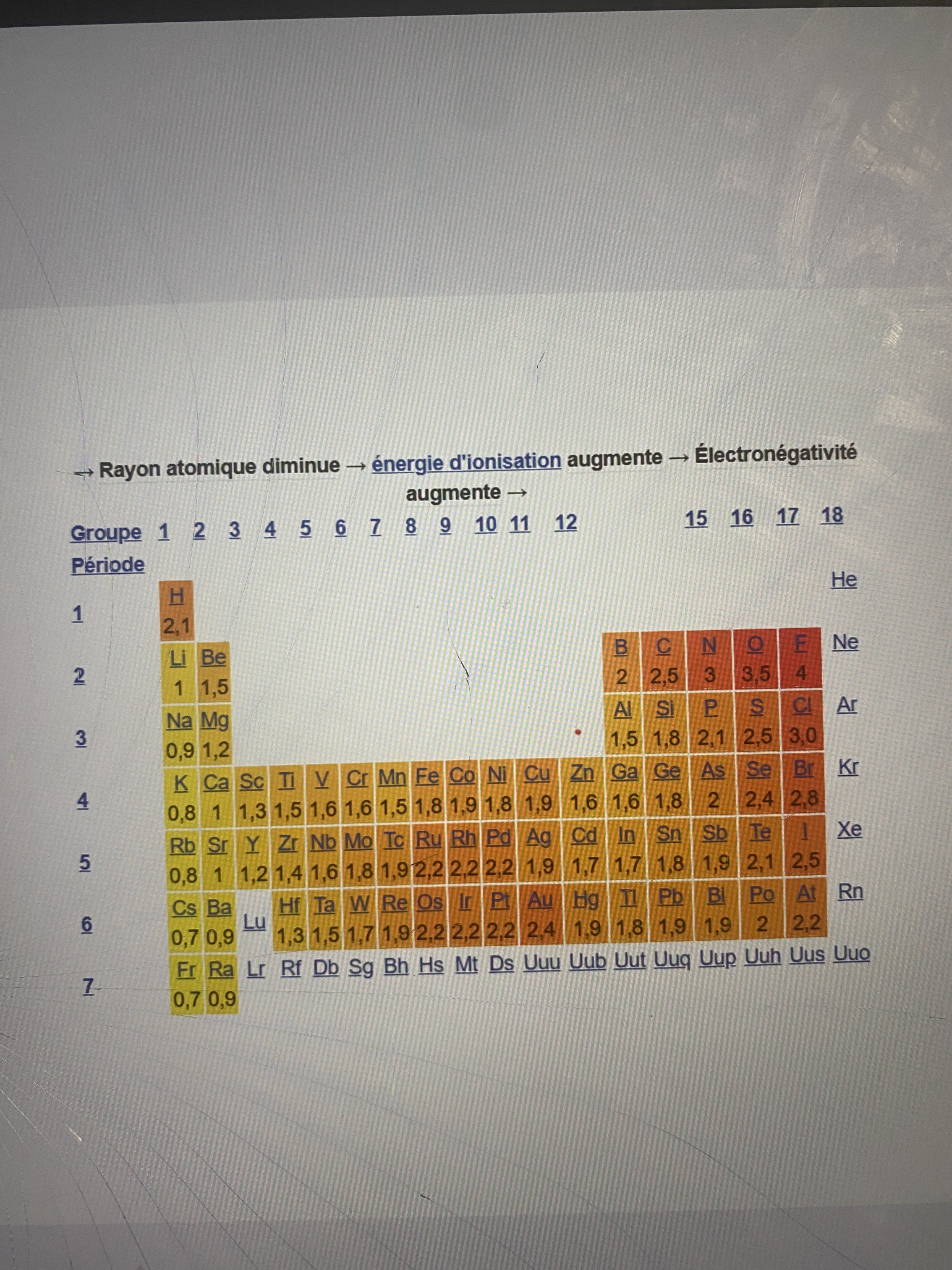
Tout d'abord, souviens-toi que l'électronégativité est une valeur de force, celle avec laquelle le noyau d'un atome va attirer les électrons de sa dernière couche électronique. Donc, un atome très électronégatif, avec par exemple une électronégativité de 3,5, sera, en quelque sorte, tissé serré. Il sera donc particulièrement difficile pour un autre atome d'arracher un électron de l'atome fortement électronégatif. À l'inverse, il sera facile pour cet atome électronégatif d'arracher les électrons d'un autre atome. Comme tu peux voir sur ton échelle de Pauling, l'électronégativité est représentée par un chiffre de 1 à 4, et augmente de gauche à droite et de bas en haut dans le tableau périodique.
Voici la page d'Allô Prof qui explique en détail d'électronégativité: https://www.alloprof.qc.ca/fr/eleves/bv/sciences/la-periodicite-des-proprietes-s1583.
Or, ces "arrachements" d'électrons ont pour but de former des liaisons chimiques entre les atomes. On distingue deux types de liaisons: la covalente et l'ionique. (Cette page d'Allô Prof en traite plus en détail: https://www.alloprof.qc.ca/fr/eleves/bv/sciences/les-liaisons-covalente-et-ionique-s1070).
La liaison ionique survient lorsqu'un atome transfert un électron à un autre. On peut donc dire que la liaison ionique survient lorsqu'un atome électronégatif "arrache" les électrons d'un autre. En ce sens, dès que la différence d'électronégativité entre deux atomes est supérieure à 1,7, l'atome le plus électronégatif va arracher un ou des électrons de l'autre atome: la liaison sera ionique.
La liaison covalente survient lors d'un partage d'électrons entre deux atomes. Il n'y a donc pas d'arrachement d'électrons, ce qui s'explique par le fait que la différence d'électronégativité entre les deux atomes n'est pas assez grande. En ce sens, dès que la différence d'électronégativité entre deux atomes est inférieure à 1,7, la liaison sera covalente.
Donc, à titre d'exemple, dans ton exercice, pour connaître la différence d'électronégativité entre le K et le Br, il faut soustraire leurs valeurs d'électronégativité sur l'échelle de Pauling. (On soustrait toujours la plus grande valeur par la plus petite pour avoir une valeur positive). Puisque cette différence est de 2, ce qui est supérieur à 1,7, il s'agirait d'une liaison ionique.
N'hésite pas si tu as d'autres questions:)
Kylan
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!