Les solutions
Secondaire 3
Une solution est un mélange homogène composé d'un solvant et d'un ou plusieurs solutés.
Une solution aqueuse est une solution dans laquelle le solvant est l'eau.
Habituellement, les solutions sont sous forme liquide. On ne peut pas y distinguer les différents constituants du mélange. Une solution ne doit avoir qu'une seule phase autant d'un point de vue macroscopique (à l'oeil nu) que d'un point de vue microscopique (au microscope).
Dans un mélange d'eau et de sucre, le résultat du mélange, l'eau sucrée, est une solution, car on ne peut pas distinguer les constituants du mélange (autant à l'oeil qu'au microscope) et le mélange laisse passer la lumière.
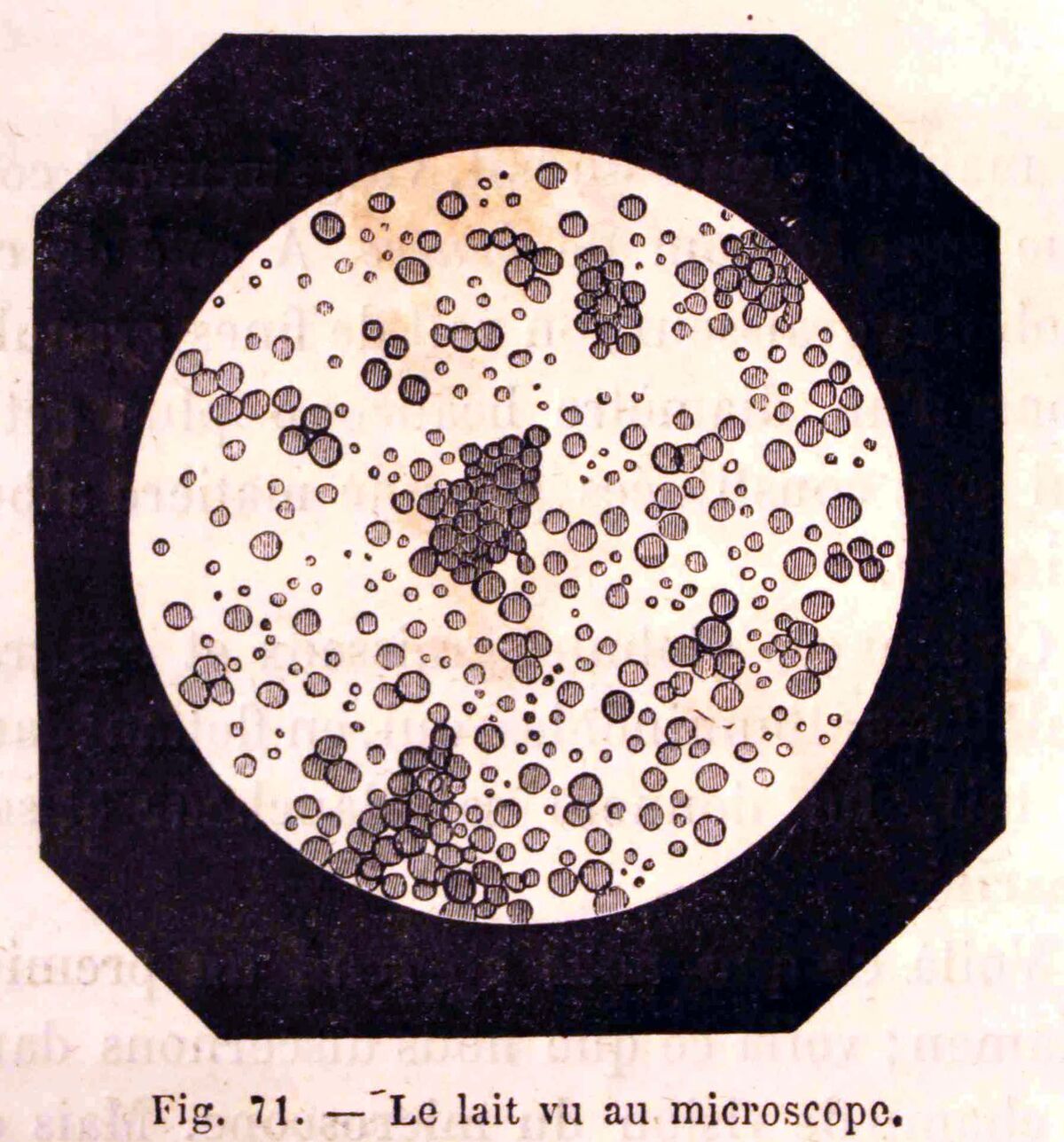
Toutefois, le lait n'est pas une solution. Bien que d'un point de vue macroscopique, il n'est pas possible de distinguer les constituants, il est possible de voir certains des éléments formant le lait lorsqu'il est observé au microscope.
Il existe également des solutions solides, mieux connues sous le nom d'alliage. Un alliage est un mélange homogène de plusieurs solides.
Une médaille de bronze est un alliage de cuivre et d’étain.
Le soluté
Le soluté est la substance qui est dissoute dans le solvant.
Dans une solution d’eau sucrée, le sucre serait donc le soluté.
Le solvant
Le solvant est la substance présente en plus grande quantité dans une solution.
C’est dans le solvant que l’on peut dissoudre le soluté.
Dans une solution d’eau sucrée, l’eau serait donc le solvant.
Attention!
Il peut y avoir plus d'un soluté dans une solution. Toutefois, il n'y a qu'une substance qui agit en tant que solvant.
Dans l'urine, plus de 3 000 composants sont présents. L'eau, qui compose 95 % de l'urine, est le solvant, alors que tous les autres composants (urée, minéraux, etc.) sont des solutés de l'urine.
Le plasma est également composé d'eau (environ 90 %), ce qui en fait le solvant. Les solutés du plasma sont les sels, les lipides et les hormones.
Le tableau suivant présente différents exemples de solution selon les différents états de la matière.
| Classification des solutions | |||
| État physique de la solution | État du soluté | État du solvant | Exemples |
| gaz | gaz | gaz | air (mélange principalement d'azote et d'oxygène) |
| liquide | gaz | vapeur d'eau dans l'air | |
| solide | gaz | neige carbonique dans l'air | |
| liquide | gaz | liquide | oxygène dans l'eau |
| liquide | liquide | alcool dans l'eau | |
| solide | liquide | sucre dans l'eau | |
| solide | gaz | solide | hydrogène dans le palladium |
| liquide | solide | mercure dans l'or | |
| solide | solide | carbone dans l'acier | |
Dans cette page