Secondaire 5 • 2a
Bonjour,
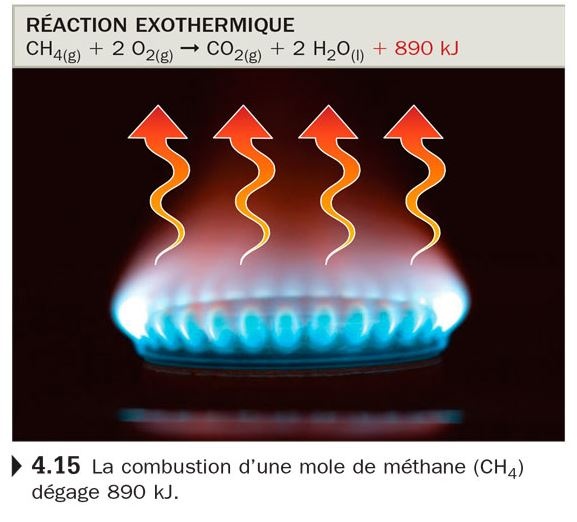
Pourquoi dans cette réaction exothermique on indique +890 kJ? (Ce n'est pas censé être -890kJ, car l'énergie associé à une réaction exothermique est négatif.)
Merci et bonne journée! :)






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut OrAutonome2754,
Merci pour ta question!
D'un point de vue de la variation enthalpie (ΔH), une réaction exothermique correspond à une énergie ''négative''. Par contre, lorsqu'on écrit une réaction chimique, un conserve l'énergie positive, mais sa position définie si la réaction est endo ou exo. Si l'énergie est avec les réactifs, il faut ajouter de l'énergie au mélange pour obtenir une réaction. Il s'agit alors d'une réaction endothermique. Toutefois, si l'énergie est dans les produits, il y a production d'énergie. Il s'agit donc d'une réaction exothermique.
Voici une fiche à ce sujet si tu veux en savoir davantage:
J'espère que ça t'aide et n'hésite pas à nous réécrire si tu as d'autres questions!
Anthony B.
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!