Secondaire 5 • 2a
BONJOUR JOYEUX NOËL ET UNE BONNE ANNÉE A TOUS LES PROFS !! JE SUIS EN SECONDAIRE 5 ET J'AI Fait CET EXERCICE SVP ME DIRE SI JE L'AI BIEN FAIT ET POUR L'EXERCICE NUMÉROS 2 ET 3 JE NE LE COMPRENDS PAS J'AI MÊME LUE LES NOTE DE COURS DE ALLO PROF ET TOUJOURS JE NE COMPRENDS PAS SI VOUS POUVEZ M'AIDER AVEC LE NUMÉRO 2 ET LE 3 JE FAIS ESSAYER DE LE FAIRE TOUT SEUL MERCI.







Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Salut GrenatTurquoise4148,
Merci pour ta question!
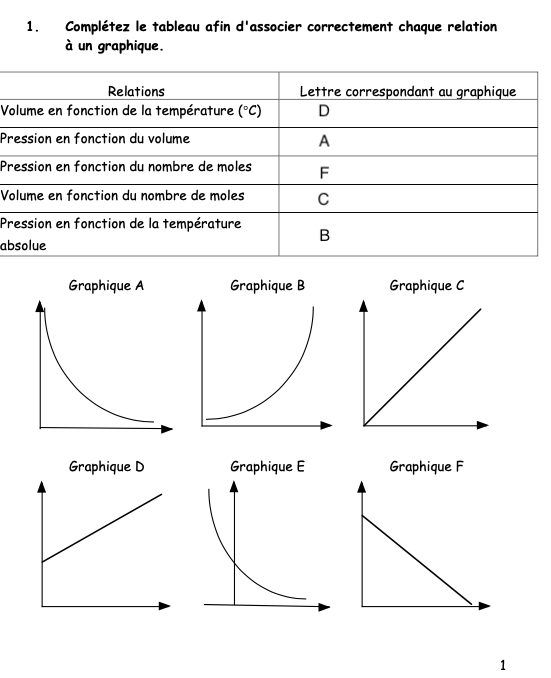
Pour ce qui est de la question #1, tu sembles avoir fait les bonnes associations! Si tu veux en savoir plus sur ces relations, tu peux consulter les différentes formules dans mon explication précédente.
Je vais te faire la question #2 en exemple, mais je vais te laisser faire la question #3 par toi-même.
La première étape est d'identifier les données du problème. D'abord, nous avons que dans les poumons, la pression est de 98,0 kPa, le volume est de 500 mL et que la température est de 37°C. Également, on sait qu'à l'extérieur la pression est de 700 mm Hg et que la température est de 20°C. Dans ce problème, on cherche le volume d'air inspiré selon les conditions extérieures qui te sont données.
La formule qui unit les différentes valeurs que nous avons et le volume est la loi des gaz parfaits, voici la formule :
Ce contenu est protégé par le droit d'auteur. Toute reproduction à l'extérieur des forums Alloprof est interdite et pourra être considérée comme une violation du droit d'auteur.
Maintenant pour ce qui est des calculs, il est possible de trouver la quantité d'air dans les poumons à l'aide de cette formule. Si tu convertis les unités des valeurs dans ceux de la formule, tu arrives à 0,019 mole (R = 8,314 kPa L / mol K). Ensuite, tu dois trouver à quoi correspond le volume de cette quantité d'air selon les conditions extérieures. Si tu réutilises la loi des gaz parfaits avec les données de l'extérieur et la quantité de moles que tu viens de trouver, tu vas obtenir le volume d'air inspiré. Cette valeur est nécessairement inférieure à 0,5 L, car les poumons ne se vident jamais entièrement lors de la ventilation. Voici une fiche sur la loi des gaz parfaits si tu veux en savoir davantage:
J'espère que ça t'aide et n'hésite pas à nous réécrire si tu as d'autres questions!
Anthony B.
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!