Secondaire 4 • 3a
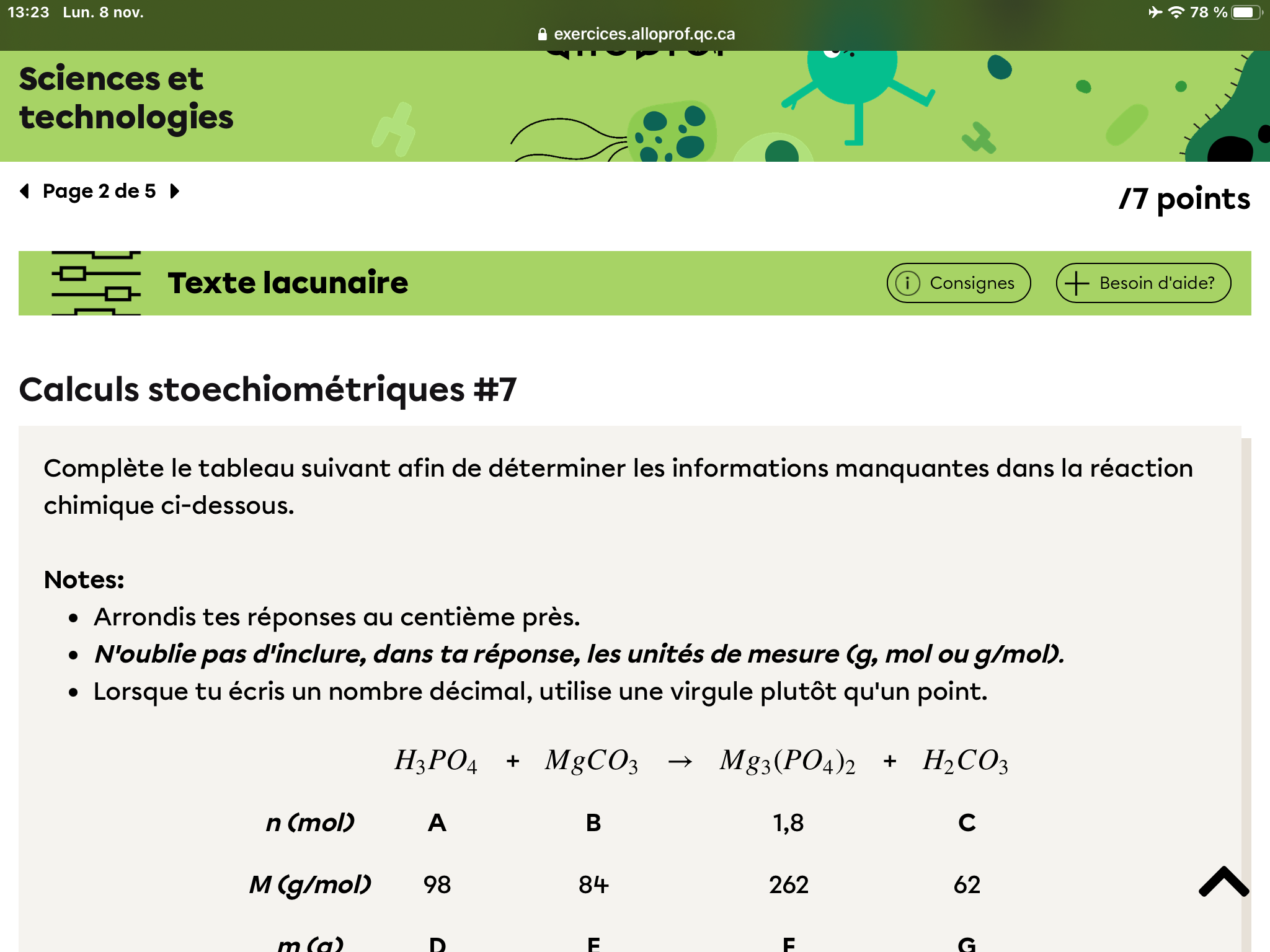
Bonjour, j’essaie d’équilibrer cette équation dans le but de faire mon calcul stœchiométrique de la manière dont vous l’avez expliqué, mais on dirait que les coefficients ne correspondent pas. Si possible me donner l’explication de ce problème, ou si l’exercice est erroné, le corriger,
merci beaucoup






Explication d'Alloprof
Cette explication a été donnée par un membre de l'équipe d'Alloprof.
Bonjour Opale Agile!
Merci de faire appel à nos services 😉
Pour équilibrer cette équation chimique, utilisons la méthode selon la molécule la plus complexe, c’est-à-dire celle qui contient le plus d'atomes. Dans notre cas, c'est la molécule \( Mg_3(PO_4)_2 \).
On peut alors commencer à faire le bilan des atomes à partir de cette molécule. Elle comprend 3 atomes de magnésium (Mg), 2 atomes de phosphore (P) et 8 atomes d'oxygène (O).
Comme les réactifs comprennent seulement 1 atome de magnésium et 1 atome de phosphore, on multiplie donc la molécule \(MgCO_3 \) par 3 et la molécule \(H_3PO_4 \) par deux.
À partir de là, il suffit de continuer le bilan d'atomes en observant le nombre d'atomes de chaque sorte des deux côtés de l'équation et d'ajuster en multipliant les molécules jusqu'à l'équilibre.
Pour réviser les démarches à suivre pour cette méthode, tu peux suivre le lien suivant:
J'espère que cela t'aidera!
Suggestions en lien avec la question
Suggestion en lien avec la question
Voici ce qui a été trouvé automatiquement sur le site, en espérant que ça t’aide!